| Top 車山高原 車山高原お知らせ 車山ブログ
|
 |
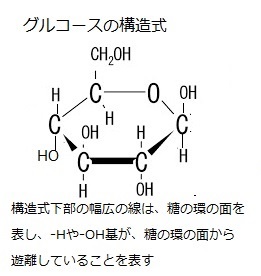 (CH2O)nという一般式で表される単糖は、最も簡単な糖(sugar)である。nは通常3から6の整数である。それ以上加水分解されない糖類で、複数の糖が脱水縮合して多糖を作る時に単量体となる。
(CH2O)nという一般式で表される単糖は、最も簡単な糖(sugar)である。nは通常3から6の整数である。それ以上加水分解されない糖類で、複数の糖が脱水縮合して多糖を作る時に単量体となる。単糖の化学式により、単糖や単糖からできた多量体は炭水化物と呼ばれる。例えばグリコース(ブドウ糖)の化学式はC6H12O6である。この化学式だけでは、グルコース分子を完全に定義できない。同じ数の炭素・水素・酸素原子が揃っても共有結合の仕方でいろいろな構造分子ができるからである。
グルコース分子は、炭素原子を6個もつ六炭糖(hexose;héksous)の一種で、生細胞の代謝で主要な役割を果たす。動物細胞ではグリコゲン、植物細胞ではデンプンという多量体で貯蔵される。
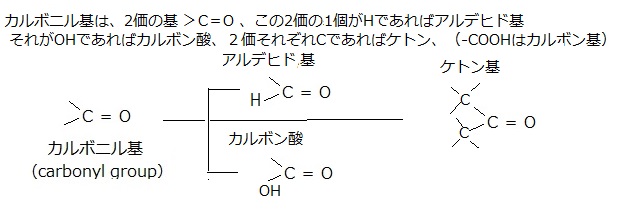
メチル基(-CH3)・ヒドロキシ基(-OH)・カルボキシ基(-COOH)・カルボニル基 ( >C=O;二重結合の基)・ホスホリル基またはリン酸基(-PO32-)・アミノ基(-NH2)などお決まりの原子の組み合わせが、有機分子に頻繁に現れる。カルボニル基(>C=O)の2価の炭素原子に炭化水素基が、それぞれついたものがケトンである。炭化水素基には、メチル基CH3-・エチル基C2H5-・(ノルマル)プロピル基(CH3)2CH-・フェニル基C6H5-・ナフチル基C10H7-などがある。
 水は極性結合を持つので、親水性物質に対しては優れた溶媒となる。
水は極性結合を持つので、親水性物質に対しては優れた溶媒となる。H2O ⇌ H+(水素イオン)+OH−(水酸化イオン)
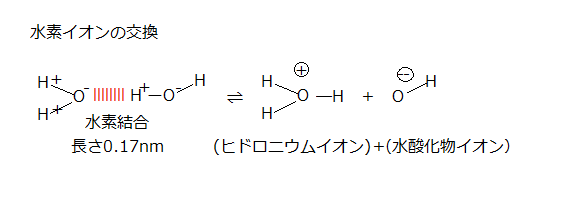
正電荷を持つ水素イオン(H+)は、1つの水分子から別の水分子へと移れる。そのため2通りのイオン種ができる。
2H2O ⇌ H3O+(ヒドロニウムイオン) + OH−
この可逆反応は速いので、水素イオンは絶えず水分子間を行き来する。
純水な水は、いつも等濃度のヒドロニウムイオンと水酸化イオンが含まれて、どちらも10-7M(pH=7)である。 水素イオンのモル濃度を水素イオン濃度といい、H+で表す。また、水酸化物イオンのモル濃度を水酸化物イオン濃度といい、OH−で表す。 純水では、水素イオン濃度と水酸化物イオン濃度は等しく、25 ℃では次のような濃度となる。
H+=OH−=1×10-7 mol/L
H+= 10- n mol/L のとき、pH = n
酸性はpH<7、中性はpH=7、塩基性はpH>7で表される。
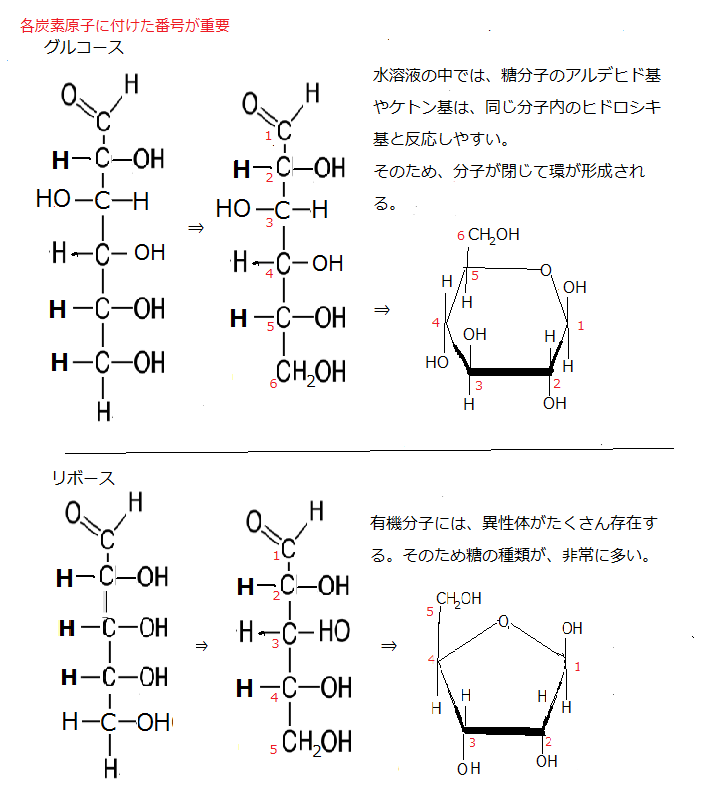
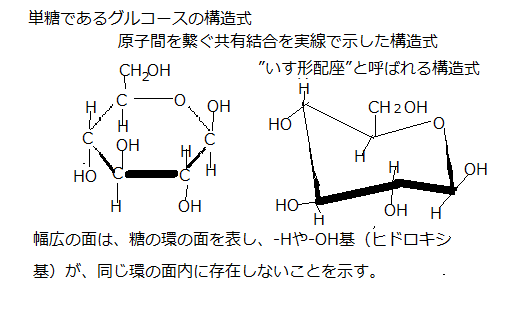 グルコースは、1つの-OH基の向きが変わるだけで、別の単糖、例えばマンノースやガラクトースに変わる。化学式は同じだが構造が異なる分子を異性体という。右手と左手は鏡写しの関係である。しかし、平面的にも立体的にも、重ね合わせることはできない。特にこのような鏡像関係にある異性体分子を光学異性体という。
グルコースは、1つの-OH基の向きが変わるだけで、別の単糖、例えばマンノースやガラクトースに変わる。化学式は同じだが構造が異なる分子を異性体という。右手と左手は鏡写しの関係である。しかし、平面的にも立体的にも、重ね合わせることはできない。特にこのような鏡像関係にある異性体分子を光学異性体という。単糖の仲間には、同一の原子の種類と数が一致しながら、原子の空間配置が異なる異性体が多数存在する。
例えば、グルコース・ガラクトース・マンノースは、同じ化学式(C6H12O6)でありながら、1個か2個の炭素原子に付く基の配置が異なるため、互いに異性体関係となっている。
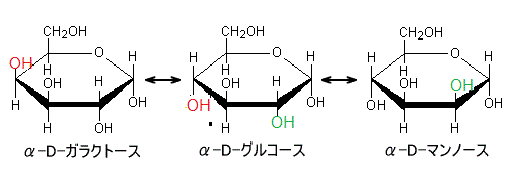 この程度の糖の僅かな違いでは、その化学的性質上の差異は余り生じない。しかし、酵素などのタンパク質は、この僅かの差異を見分けるので、生物にとって重要な役割を担うことになる。
この程度の糖の僅かな違いでは、その化学的性質上の差異は余り生じない。しかし、酵素などのタンパク質は、この僅かの差異を見分けるので、生物にとって重要な役割を担うことになる。アルデヒド基やケトン基は、分子が環状になるヒドロキシ基を持つが、そのヒドロキシ基の位置が2通りある。それが高速で入れ替わる。この2つをαとβと位置付けて、「αヒドロキシ」「βヒドロキシ」と呼ぶ。これらが別の糖と結合したとたんに、α形かβ形のどちらかに固定される。
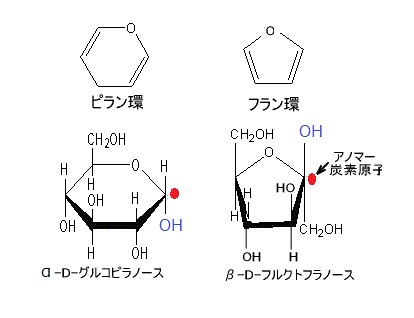 単糖からできた炭水化物の安定な環状構造はピラン環またはフラン環に似ている。
単糖からできた炭水化物の安定な環状構造はピラン環またはフラン環に似ている。フラン (furan) は、化学式C4H4O で表される、4個の炭素原子と1個の酸素原子から構成される5員環の複素環式芳香族化合物である。
ピラン (pyran) は、化学式 C5H6O で表される、5個の炭素原子と1個の酸素原子を含む6員環のエーテル化合物である。
アノマー(anomer)とは、炭水化物のフラノース(furanose)やピラノース(pyranose)が、それぞれフラン型、ピラン型の環状構造を形成して立体異性体となる関係を示す化学用語である。
フラノース環は、4つの炭素原子と1つの酸素原子を頂点として5員環持つ、炭水化物の総称である。頂点にある酸素の右側の1つの炭素(C-1炭素)がアノマー炭素原子(anomeric carbon atom)となっている。
ピラノースは、5つの炭素と1つの酸素を頂点として6員環を構成し、酸素の右側の1つの炭素(C-1炭素)がアノマー炭素原子となる。いずれもアノマー炭素原子付近にヒドロキシ基が結合している。
炭水化物(糖)分子と別の有機化合物とが脱水縮合して形成する共有結合をグリコシド結合(glycosidic bond)と言う。植物では熟した果実中に多いグルコース(ブドウ糖)がその例であるが、ヒドロキシ基の位置には、2通りあり、高速で入れ替わっているが、その違いを表記する為にα-またはβ-の接頭辞が使用される。C-1炭素のヒドロキシ基がアノマーの下部に結合すればα-D-Glucoseであり、上部に結合すればβ-D-Glucoseと呼ばれる。単糖類には、DとLの光学異性体があるが、天然に存在するグルコースはD-グルコースである。
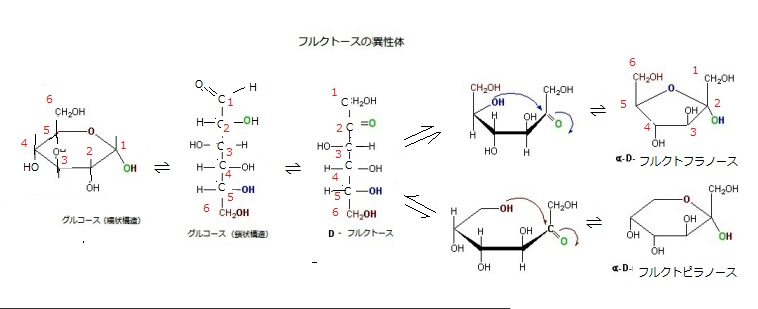
 フルクトース(果糖)は、甘い果実や蜂蜜中に多量に存在する。ベリー類・メロン、ある種の根菜にも多量に含まれ、精液にも微量だが混和している。
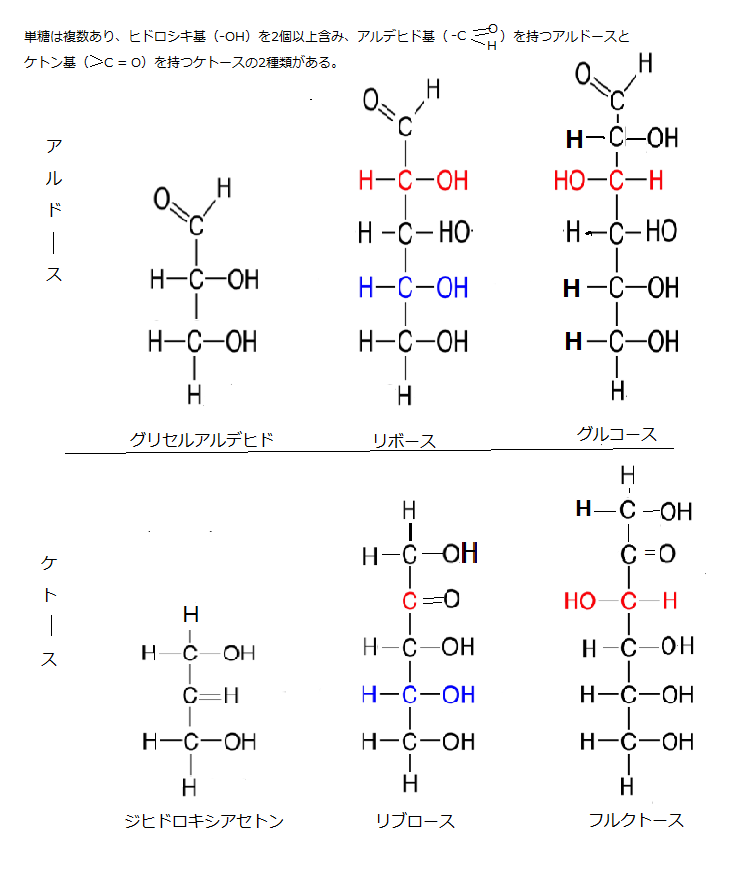
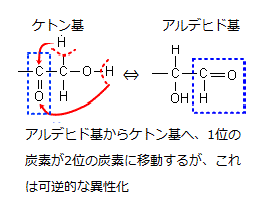
フルクトース(果糖)は、甘い果実や蜂蜜中に多量に存在する。ベリー類・メロン、ある種の根菜にも多量に含まれ、精液にも微量だが混和している。フルクトースは6炭素のポリヒドロキシケトンである。単糖は、単一のポリヒドロキシアルデヒドまたはポリヒドロキシケトンといわれる。水に溶けやすい白い結晶性の固体で、甘味があり、化学的にはカルボニル基の型と炭素数で、ポリヒドロキシアルデヒドであるアルドース(aldose)とポリヒドロキシケトンであるケトース(ketose)の2種類に分類できる。それは、単糖の化学構造の可逆的再配置、つまり異性化により、カルボニル基の「C=O」で、炭素と二重結合する酸素の1個が、グルコースの1位の炭素から2位の炭素に移動し、単糖はアルドースからケトースへと変わっていくことになる。
「基」とは、「functional group」 で、有機化合物の性質を特徴づける原子団を意味する。置換基は、化合物の系統やその命名の際に、参考にされる構造式により、母体化合物との対として理解されている。主体となる構造を母体と呼び、異性体を示す原子団を置換基と呼ぶ。化合物の特性や反応性に着目した場合には官能基と呼ぶ。
そして炭素を含む置換基は、アルデヒド基かケトン基であるため、直鎖の単糖を2つに分けられる。アルデヒド基を含む単糖をアルドース(aldose) 、ケトン基を持つ単糖をケトース(ketose) と呼ぶ。それは酸素原子と二重結合でつながっている炭素を末端に持つものをアルドース、内部に持つものをケトースと見分けられる。環状になった単糖は6員環のものをピラノース、5員環のものをフラノースと呼ぶ。
単糖には多くの誘導体がある。誘導体とは、基本的な化学構造の一部が変化したもので、特に単糖の誘導体を誘導糖と呼ぶ。グルコースなどの単糖の誘導体では、ヒドロキシ基が、他の基で置き換えられる。カルボキシル基(-COOH)に置き換わりグルクロン酸、アミノ基(-NH2)に置き換えられるグルコサミン、水素原子をアセチル基(-CH3CO)で置き換えるN- アセチルグルコサミンなどになる。
単糖が重合してオリゴ糖や多糖になったものや、重合によらない糖リン酸・デオキシ糖・アミノ糖・糖アルコール・アスコルビン酸などの誘導体もある。単糖の誘導体も生物に様々に重要な役割を果たしている。しかも生物の根源に関わっている。