| Top 車山高原 車山高原お知らせ 車山ブログ
|
 |
 |
| 目次 |
| 1)自由エネルギーと活性化エネルギー |
| 2)酵素と熱運動 |
| 3)代謝と活性運搬体との関係 |
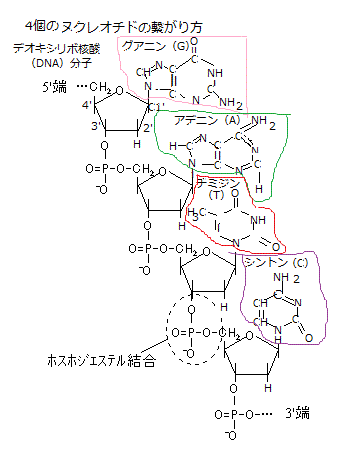
 生体高分子の合成には、エネルギーの投入が必要である。細胞の水を除いた質量、つまり乾燥重量の殆どは、単量体が酵素触媒による縮合反応でつながった巨大分子で占められている。その逆反応である高分子の分解には、酵素が触媒する加水分解反応によって行われる。
生体高分子の合成には、エネルギーの投入が必要である。細胞の水を除いた質量、つまり乾燥重量の殆どは、単量体が酵素触媒による縮合反応でつながった巨大分子で占められている。その逆反応である高分子の分解には、酵素が触媒する加水分解反応によって行われる。加水分解はエネルギー的に起こりやすいが、その逆の生合成反応はすべてエネルギー的に起こりにくく、エネルギーの投入が必要となり、はるかに複雑である。
しかし、酵素または触媒によって、Y→Xの反応の活性化エネルギー(activation energy;特定の化学反応進行のために分子が必要とするエネルギー)が下がるときには、逆反応のX→Yでも活性化エネルギーは同じだけ下がる。酵素はどちらの向きの反応も同じ割合で加速するので、反応の平衡点や標準自由エネルギー変化(△G O)は変わらない。
熱力学第1法則は、「エネルギーは生成消滅することはないが、形態の変化はできる」が、宇宙エネルギーの総量は、常に一定であると言う。植物は、この熱力学を活用して、光合成により太陽エネルギーを、ATPなどの諸々の生成エネルギーや、糖などの小さな有機分子に変換する。
熱力学第2法則は、「化学反応は、宇宙全体の乱雑さが増す方向に起こり、乱雑さは仕事に使えるエネルギーが熱として放出されるときに増す」と言う。細胞と同様、酵素も熱力学第2法則に従い、酵素はエネルギー的に起こりやすい、「宇宙全体の乱雑さが増す方向」に反応を加速させるので、エネルギー的に起こりにくい反応を無理やり起こすことはできない。
ところが、細胞は、成長し、分裂するためだけでなく、単に生存するためにも不可欠である、レベルの高い秩序を生み出し、小さな単純な分子から、エネルギーに富んだ分子を作らなければならない。この過程でエネルギーの投与が必要になる。酵素は、触媒作用を推進し、生命を持続するのに必要な特定の化学反応を加速させる。
この反応は、一方向にのみ進行し、煙と灰が、温まった大気から水と二酸化酸素を回収して、再び紙に戻ることはない。紙の化学エネルギーの大半は、熱となって大気に散っていき、エネルギーが生成消滅することがない宇宙から失われることはないが、分子のランダムな熱運動として散るため回収は不可能になる。
同時に紙の分子や原子も構造を失い拡散する。このように仕事をしたり、化学反応をしたりした際に、エネルギーが失われたときに、熱力学では「自由エネルギー」が放出されたと言う。この放出は、エネルギーと紙に蓄えられたていたときに出来上がっていた秩序の減少を意味する。つまりは、化学反応は「自由エネルギー」の減少の方向だけに進み、その反応が自発的に進むのは、「下り坂」方向で、それが「エネルギー的に起こりやすい」方向になる。
定温・定体積の条件下で、化学反応が、細胞内で起こり乱雑さが生じるとすれば、反応分子の結合エネルギーが変化し、熱が放出されることにより細胞周辺で乱雑さが増すか、あるいは、細胞内の長い鎖状の分子がばらばらになり、また、結合の回転を妨げていた相互作用がなくなるなど、その反応により細胞内の秩序が下がった場合である。
「自由エネルギーfree energy(G)」は、細胞内程度の定温下で、分子が持つ仕事に使えるエネルギーであるが、細胞を構成する分子は、振動・回転・運動のエネルギーと、原子間の結合で蓄えられたエネルギーを持っている。
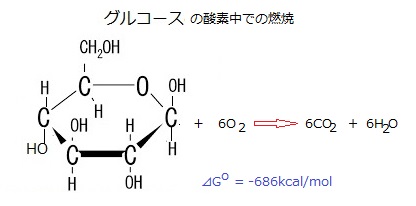 ただ自発的な反応が、素早い反応とは限らない。「自由エネルギー変化(ΔG)」が負であっても、それだけで反応が直ぐに起こるとは限らない。グルコースの酸素中での燃焼は、エネルギー的には非常に起こりやすい反応でも、酵素による加速がなければ、何百年経っても起こらない。酵素が反応を触媒し加速させるが、反応の△G0は変えられない。
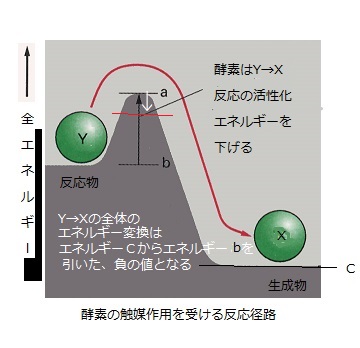
ただ自発的な反応が、素早い反応とは限らない。「自由エネルギー変化(ΔG)」が負であっても、それだけで反応が直ぐに起こるとは限らない。グルコースの酸素中での燃焼は、エネルギー的には非常に起こりやすい反応でも、酵素による加速がなければ、何百年経っても起こらない。酵素が反応を触媒し加速させるが、反応の△G0は変えられない。通常の条件で、炭素がエネルギー的に取り出しやすい形態は、CO2であり、水素ではH2Oである。その一方で、生物が作る分子は比較的安定した状態にあり、そのためエネルギーを新たに加えなければ、より低いエネルギー状態には戻れない。つまり、分子が化学反応によって低エネルギーの安定した状態に移るためには、そのエネルギー障壁を越えるための活性化エネルギー(activation energy)を、周辺から求めなければならない。細胞内では酵素(enzyme)と呼ばれるタンパク質が、自ら触媒する特定の活性化エネルギーの障壁を大きく下げ、効率の高い触媒をする。
酵素は、基質(substrate)と呼ばれる1個か2個の分子と固く結合し、基質間の化学相互作用を進めるために必要な活性化エネルギーのレベルを大きく下げて、それを保持する。活性化エネルギーを下げる能力のある物質を触媒(catalyst)と呼ぶ。活性化エネルギーが低下すると、反応が起こりやすくなるばかりか、触媒により、基質と周囲の分子とのランダムな衝突のうち、エネルギー障壁を乗り越えるものの割合が著しく増え、その化学反応の速度も、酵素がない場合と比較して1014(100兆)倍に上がることもある。
基質分子が化学反応を起こすには、その反応の活性化エネルギーの障壁を越えるエネルギーが当然必要で、生体反応では、その条件を満たすには酵素の触媒が不可欠である。それでも、反応するのに十分な高いエネルギー状態に達する基質分子は、ごく少数である。ところが、基質分子が様々な大きさのエネルギーを持つため、周囲の分子との衝突で、飛び跳ね、振動し、回転をしながら、その波に押されるようにして、低くなった活性化エネルギーの障壁を越えて反応を引き起こす。
酵素の働きにより、通常、その細胞内温度では起こらない化学反応が可能となる。酵素の選択性は高く、個々の酵素が関わる基質が行ういくつの反応のうち、通常、特定の反応の1つしか加速しない。こうして、酵素は細胞内の種々の分子が、それぞれ特定の反応径路に入っていけるよう方向付けをし、細胞に必要な化合物だけを作る。酵素には、活性部位があり、そこに1つないし2つの基質が結合して、酵素―生成物複合体を作る。その後、生成物が酵素から離れるため、次の基質分子と結合して反応を繰り返すことができる。酵素はまた、他の触媒と同様、反応に参加し基質を生成物に変えるが、自身には変化が生じないため、何回でも働ける。
 熱力学第2法則により、化学反応は、宇宙全体の乱雑さが増す方向に起こり、乱雑さは仕事に使えるエネルギーが熱として放出されるときに増す。この「自由エネルギーfree
energy(G)」と呼ばれる化学反応には、ある状態から別の状態への分子形態の遷移が伴うので、化学や生物では「自由エネルギー変化free energy
change. ΔG (デルタG)」と言う用語を使う。
熱力学第2法則により、化学反応は、宇宙全体の乱雑さが増す方向に起こり、乱雑さは仕事に使えるエネルギーが熱として放出されるときに増す。この「自由エネルギーfree
energy(G)」と呼ばれる化学反応には、ある状態から別の状態への分子形態の遷移が伴うので、化学や生物では「自由エネルギー変化free energy
change. ΔG (デルタG)」と言う用語を使う。分子集団で見れば、ΔGは、これらの分子が反応したときに、宇宙全体に生み出される乱雑さの尺度である。定義の「エネルギー的に起こりやすい反応」とは、自由エネルギーが減少して乱雑さを増すような反応である。「負のΔG」をもつ反応と言える。
縮められたバネが元の長さに戻るのは、蓄えられていたエネルギーが熱として放出されるからである。
反対に、エネルギー的に起こりにくい反応は、宇宙に秩序を生み出す、このような反応は「正のΔG」を持ち、例えば2個のアミノ酸からペプチド結合ができる反応は、自発的には起こりえない。そのためには、より大きな「「負のΔG」を持つ別の反応と共役して、全体のΔGが負になる場合に限って起こりえる。生命が存在できるのは、酵素がエネルギー的に起こりにくい反応を、エネルギー的に起こりやすい反応と共役させ、生物としての秩序を生み出すからである。
ΔGは、反応時に起こる自由エネルギーの変化を言うが、「Δ」は、差を表す。
例えば A + B → C + D の反応では、ΔG = (C + D)の自由エネルギー ―(A + B)の自由エネルギー
ΔGは、反応で生じる乱雑さの量の尺度となり、反応による細胞内の秩序の変化量と、放出された熱による周囲の秩序の変化量の和である。
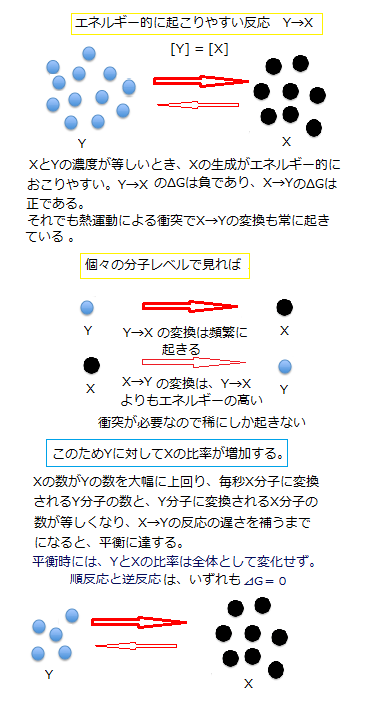
化学反応の進行は、個々の分子に蓄えられたエネルギーだけでなく、反応混合物の分子の濃度にも依存する。エネルギー的に起こりやすいY→X反応の進行につれ、生成物Xの濃度は増加して基質Yの濃度は減少する。基質と生成物の相対濃度がこのように変わると、YとXの比率が縮み、当初の起こりやすいΔGが、次第になくなってくる。Yをさらに加えない限り、反応は遅くなりいずれは停止する。
ΔGは、生成物が蓄積し基質がなくなるにつれ変化するので、化学反応は一般的に、進行すると平衡equilibrium状態に達する。この時点で、順方向と逆方向の反応速度が等しくなり、基質と生成物の濃度に実質的な変化が生じなくなる。化学平衡にある反応では、ΔG =0であり、反応は進むことも戻ることもなく、仕事はなされなくなる。
このような完全な化学的平衡状態は、生命の実体とはかけ離れている。生命ある細胞は、栄養分の補給や不要物の除去など、絶え間なく物質を周囲と交換し、完全な化学的平衡状態になるのを避けている。細胞内での複雑な代謝では、ある反応の生成物が次の反応の基質となって、次々と吸い上げられるので、反応の多くは非平衡状態にある。順反応と逆反応の速度が等しくなる濃度に生成物と基質が達することはめったにない。
目次へ
細胞質ゾルには、酵素も基質も比較的少ない量しかない。その環境で典型的な酵素は、毎秒1,000個の基質分子を捕らえて反応させている。酵素は、1秒間の何千分の1という短時間で生成物を放して、次の基質と結合している。その一方で、細胞質ゾルは、様々な形と大きさの分子で非常に混み合っている。その中で、分子は素速く動き、混雑している細胞質ゾル内で相手を見つけている。
分子は、熱エネルギーで絶えず運動し、そのランダムな動き(拡散diffusionという)で、細胞質ゾル内を効率よく探査している。細胞質ゾル内の溶液中の各々の分子は、毎秒膨大な数の分子と衝突し互いに跳ね返っているので、個々の分子の進む向きは刻々変わる、でたらめ状態になる。それで「ランダム歩行(random walk)」と呼ぶ。基質となる小有機分子は、平均0.2秒で10㎛も拡散する。
酵素などの巨大分子は、他の様々な巨大分子(基質)と相互作用するせいか、細胞質ゾル内を比較的ゆっくり拡散するが、小分子は、素早く拡散している。
巨大分子のタンパク質は、小分子と比べ細胞質ゾル内の拡散が非常に遅いので、酵素が基質と出合う頻度は、基質分子の濃度に依存する。豊富な基質であれば、約0.5mMの濃度で存在している。細胞質ゾル内の純水の濃度は、55Mであるから、水分子105個につき基質物質は1個と随分少ない。それなのに基質に対応する酵素の結合部位に毎秒50万回も衝突する。
ある物質の分子量がMである場合、この物質のMgには、分子が6×1023個含まれている。この量を1M(モル)と言う。単位記号は、mol、化学反応に参加し得る分子の数を表す方法として化学では広く使われている。陽子や中性子1個の質量は、約1 / 6×1023 gである。水素原子には中性子はなく陽子を1個だけ含むため、原子量は1で、1gの水素には、6×1023×1個の原子が含まれていることになる。この膨大な数6×1023個により、化合物の日常的な量と、その構成単位となる原子や分子の数とを関連付けられるようになる。ある物質の分子量がMである場合、この物質のMgには分子が6×1023個含まれることを基準として、この量を1モルと呼び、単位記号をmolとした。通常、モル濃度(mol/L)で表し、分子が6×1023個含まれている1 molには、炭素が12g、グルコースでは180g、塩化ナトリウムは58g含まれる。炭素は陽子6個と中性子6個を有し原子量は12であるから、12gの炭素には6×1023×12個の原子があるからである。1Mの溶液には、1リットルあたり1molの物質が溶けている。1mMは、0.001mol/Lである。ミリグラム (mg) は、質量の単位で、0.001gに相当する。
例えばグルコースの1モル溶液(1M)には180g/l、1ミリモル溶液(1mM)には180mg/lのグルコースが含まれている。
酵素と基質が何度も出合う内に、酵素―基質複合体ができあがり、両者の間で弱い結合がいくつも生まれ、会合状態は安定する。弱い相互作用には、水素結合・ファンデルワールスvan der Waals引力・静電引力がある。それは、ランダムな熱運動で分子が解離するまで持続する。酵素と基質が的確に適合すると弱い相互作用が数多く形成され、双方が互いに固く保持され、基質物質に共有結合を形成するか結合を切断するかの時間が生じる。分子の衝突や解離の速さ、結合の形成と切断の速さを知れば、酵素による触媒反応の実測値が出せる。
2つの酵素と基質の分子の表面が適合しなければ、共有結合は殆どできず、結合エネルギーは熱運動エネルギーより小さいので、2つの分子は接触するやすぐさま解離する。これにより酵素と不適切な基質との不適合な会合を回避している。
カルボニックアンヒトラーゼ(炭酸脱水酵素)は、非常に反応速度が高い酵素で、気体のCO2を水に溶けやすい炭酸水素イオン(HCO3-)に素早く変換する。
CO2 + H2O ⇆ HCO3- + H+
カルボニックアンヒトラーゼは、呼吸によって組織内に発生したCO2を効率よく肺へ送り、素早く排出するための極めて重要な酵素である。反応を触媒するには、酵素は先ず基質と結合しなければならない。基質は反応して生成物に変わる。その直後も酵素は結合したままであるが、その後、生成物が解離し拡散する。酵素は新たな基質分子との反応に入る。この反応速度に影響する基質の濃度は、カルボニックアンヒトラーゼの活性部位に、CO2が衝突する頻度に影響されるため、この酵素がどれだけ速く生成物HCO3-を放出して、次のCO2と結合できるかに関わっている。この酵素は、活性化エネルギー障壁を低くするため、反応を起こすに足るエネルギーを持つCO2分子の濃度が高まることになる。カルボニックアンヒトラーゼにより、分子数が107倍となり、反応の速度は107倍と高くなり、最大時には毎秒105個のCO2分子が水和される。
目次へ
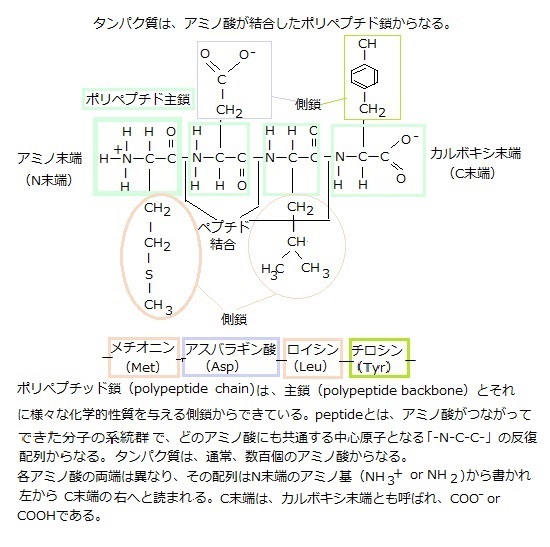 植物細胞も動物細胞も、有機分子の化学結合に蓄えられた化学エネルギーを必要とする。その有機分子は、植物が光合成により栄養源として生合成した糖や、動物が食べた大小の分子の混合物などを言う。生物は、これらをエネルギー源として誕生し、成長して子孫を増やす。そのためには、エネルギーを利用可能な形で取り出さなければならない。
植物細胞も動物細胞も、有機分子の化学結合に蓄えられた化学エネルギーを必要とする。その有機分子は、植物が光合成により栄養源として生合成した糖や、動物が食べた大小の分子の混合物などを言う。生物は、これらをエネルギー源として誕生し、成長して子孫を増やす。そのためには、エネルギーを利用可能な形で取り出さなければならない。生物は、有機分子の構造を変えることで、必要なエネルギーを、食物の酸化と言うエネルギー的に起こりやすい反応で、放出されるエネルギーを、一時的に貯蔵する。
代謝とは、生命維持活動に必要なエネルギーや、生存に必要な有機分子を生合成するために起こる化学反応や物理反応の総称と言える。非生物の様々な反応と決定的な違いは、生物が持つ固有な性質は、「乱雑さを増すのが常の宇宙で、秩序を生み出し、それを維持する能力である」。
生体内の細胞は、無限とも思える化学反応の連続で、代謝の要求に応えて、必要な分子を生合成している。それにより生じたアミノ酸・糖・ヌクレオチド・脂質などの小さな有機分子を、分解し修飾して細胞に必要な小分子を作り出している。
細胞は、これらの小さな有機分子から、タンパク質や核酸など、生物ごとに、更には個体ごとに際立った特徴を形成する多種類の巨大分子までも生成する。真核細胞の大きさは、5から100 ㎛に過ぎないが、こうした反応を毎秒数百万回も行う化学工場なのだ。しかも、細胞内で起こる化学反応の大半は、非生物の自然界では、通常、もっと高温の条件下でしか起こらない。
このため、細胞内で素早く反応させる働きをする酵素と呼ばれるタンパク質を活用する。ここの酵素は、ある基質分子が関わる膨大な反応の内、1つだけを加速させる。その加速が「触媒」である。酵素が触媒と反応すれば、次々と連結し、結果、前の反応の生成物が次の反応の出発物質となる。この長い一連の反応径路を、「代謝経路」と呼ぶ。それが互いに繋がり合い、反応の複雑な網目模様を構成する。
触媒作用により、細胞は生存に関わる「代謝metabolism」を厳密に調節する。この生命科学の中核となる細胞内の化学反応には、2つの連動が生じている。1つが食物を小分子に分解する径路(異化catabolism)であり、細胞に使いやすい形態のエネルギーや構成材料として欠かせない小分子を供給する。もう一つが、異化作用によって蓄えられたエネルギーを用いて細胞を形成する分子を合成する同化anabolism(生合成biosynthesis)径路である。この2つの連動が細胞の代謝なのである。
生物細胞は、それを構成する分子組織を含めて、あらゆるレベルで秩序を維持するだけでなく、新たに秩序を作り出している。この生命の有り様は、環境からエネルギーを受け取り、化学結合のエネルギーに変える分子機構に支えられ、その命ある組織の構成材料を、常時、入れ替え循環させると言う見事な仕組みで形態を保っている。体の構成する原子が、10年経つうちに殆ど入れ替わったとしても、体の基本構造は変わらない。
 太陽エネルギーは、日光の電磁エネルギーを細胞内の化学結合エネルギーに変換する光合成によって生物界に入る。
太陽エネルギーは、日光の電磁エネルギーを細胞内の化学結合エネルギーに変換する光合成によって生物界に入る。植物・藻類や一部の細菌を含む光合成生物は、日光から得たエネルギーを用いて、糖・アミノ酸・ヌクレオチド・脂肪酸などの構成材料となる小分子を合成する。これら小分子は、タンパク質・核酸・多糖・脂質など、植物体を形成する巨大分子に変換される。
光合成は2つ反応からなる。日光エネルギーが特定の小分子に捕らえられて、活性運搬体であるATPとNADPHと言う特殊な分子に、化学結合エネルギーとして一時的に蓄えられる。動物が呼吸する空気中の酸素(O2)は、この光合成の第1段階で、通常の草本類は、土中の水分子(H2O)を分解して放出する。
この段階の光合成反応は、
日光エネルギー + CO2 + H2O → 糖 + O2 + 熱エネルギー
と進むが、実は、この間には多くの異なる酵素が関与する反応で、あることが省かれている。
糖は、当然、CO2やH2Oよりも複雑な分子なので、この反応は細胞内の秩序を高めている。
熱力学第2法則により、「細胞内の秩序を増すには、無秩序がそれより多く増加する必要がある」。この反応式には、酵素の関与ばかりか、いろいろな段階で熱を発生させ秩序を乱している、化学的物理的変化の説明を欠いている。
第2段階では、活性運搬体が、空気中の二酸化炭素(CO2)の炭素原子から糖と有機分子を作る炭素固定を進行させる。この光合成により植物とそれを食餌とする動物にも必須となる化学結合エネルギーと有機物質を生合成する。
地球上に最初に誕生した祖先細胞は、光合成や細胞呼吸をする能力はなかった。しかも細胞呼吸が可能になるまで十分な酸素を含んだ大気となるためには、何十億年もの光合成生物の活動が必要であった。強力な証拠により、光合成が呼吸より先に登場したと見られている。
植物細胞や動物細胞は、ATP・NADPH・糖などの有機化合物に蓄えられた化学結合エネルギーを、発生・成長・種の保存のために、利用可能な形に変えて取り出さなければならない。これが酸化で、いわば制御された燃焼を行う。
地球上の大気には、酸素が21%含まれている。酸素の存在が前提にあれば、エネルギー的に最も安定しているのが炭素ではCO2であり、水素ではH2Oである。細胞は、糖などの有機分子の炭素原子と水素原子を酸素と結合(酸化)させ、それぞれが、CO2とH2Oに変えてエネルギーを獲得する。この過程を呼吸(respiration)と言う。
光合成と細胞呼吸は生物界にあっては、相補関係にある。日光エネルギーを利用して大気中のCO2の炭素原子から糖と有機分子を作る。これらの分子は他の生物の食物となる。O2を用いて食物分子を細胞による呼吸で酸化し、その炭素原子をCO2のかたちで大気中に放出する。この過程で、生物は、生存に必要な使いやすい化学結合エネルギーを得る。
食物の酸化のようなエネルギー的に起こりやすい反応で放出されるエネルギーは、細胞が必要とするすべての分子の合成など、エネルギー的に起こりにくい反応を進めるために使われるまで、一時的に貯蔵される。そのエネルギーは、通常、活性運搬体に化学結合エネルギーとして蓄えられる。運搬体は有機分子で、どれもエネルギー的に大きい共有結合を1以上持つ。それが素早く拡散して、そのエネルギーを生成した場所から生合成biosynthesisやエネルギーを必要とする細胞活動の場所に運搬する。
活性運搬体activated carrierは、細胞が使えるかたちでエネルギーを蓄え、やがて細胞内でエネルギーを運ぶ「シャトル」となり、食物分子の分解(異化)によるエネルギーの発生と、エネルギーを必要とする大小の有機分子の生合成(同化)とをつなぐ仲介役となって働く。
活性運搬体は、エネルギーを変換しやすい形態、つまり容易に転移する化学基や高エネルギーの電子として蓄えている。生合成反応では、エネルギーと基の両方の供給源となる。活性運搬体で最も重要なのは、ATPとそれによく似たNADHとNADPHの3種類である。
 生体内では、共役反応coupled reactionによって、エネルギーが捕らえられる。即ち、エネルギー的に起こりやすい反応が、エネルギー的に起こりにくい反応を引き起こし、活性運搬体などの有用分子が作られる。
生体内では、共役反応coupled reactionによって、エネルギーが捕らえられる。即ち、エネルギー的に起こりやすい反応が、エネルギー的に起こりにくい反応を引き起こし、活性運搬体などの有用分子が作られる。 共役反応には、酵素が必要で、細胞内のエネルギー運搬体すべての基礎となっている。coupled(kʌ́pəld)とは、組になっている二つ、二人、一対の意味である。
酵素は、食物の酸化のようにエネルギー的に起こりやすい反応と、活性運搬体の生成のようなエネルギー的に起こりにくい反応を共役させる。それにより、酸化反応で発生した熱は、活性運搬体の高エネルギー共有結合に蓄えられたエネルギー分だけ減少する。その蓄えられたエネルギーは、細胞内のどこか別の場所で起こる化学反応に使われる。
酸化によって放出されたエネルギーで、細胞の殆どのATPが作られる。特に重要なのが糖である。植物は光合成によって大気中のCO2から糖を作り出す。動物は植物や他の生物を食べて、糖や糖に化学変換される有機分子を摂取する。とはいえ、糖を分解してエネルギーを得る過程は、動植物とも極めて似ている。生物の細胞は、糖分子を分解し酸化してCO2とH2Oにするとき、糖に蓄えられた化学結合エネルギーから有用なエネルギーを取り出す。この過程が細胞呼吸cell respirationである。
この反応で放出されるエネルギーが、ATPやNADHという活性運搬体に、高エネルギー化学結合して蓄えられる。この共有結合が加水分解されたとき、大量のエネルギーを放出する。ATPやNADHは、生合成に必要な化学基や電子の供給源にもなる。
動物細胞では、細胞内のミトコンドリアで起こる「クエン酸回路」という一連の反応に入る。その際に大量のNADHが生じる。NADHは、生合成に必要なエネルギーと電子を供給する。その高エネルギー電子は、ミトコンドリア内膜にある酵素群、電子伝達系をたどる。ここで電子の移動に伴って放出されるエネルギーが、酸化的リン酸化、即ちATPの生成と分子的酸素(O2ガス)の消費という過程を引き起こす。
核酸(DNAとRNA)・タンパク質・多糖の合成は、いずれも縮合反応を起こす単量体から1つずつ分子の端を付け加えていく方法で合成される。その際に両端から水分子を構成する原子を奪い、その水分子を外す。その付加に先立って、単量体を活性化させるために、高エネルギーのヌクレオシド三リン酸を消費する。どの場合も、縮合の際には、ヌクレオシド三リン酸の加水分解で供給されるエネルギーを利用している。しかし、核酸以外には、最終生成物にリン酸基は残っていない。ATP加水分解のエネルギーと高分子合成はどのようにして共役しているのだろうか。これに対して核酸・タンパク質・多糖の3種類の生体高分子の逆反応では、いずれも水の付加、加水分解だけで起きる。
酵素が触媒する合成径路は、グルタミンの合成に似ている。まず、縮合反応で外れる-OH基が、別の分子と高エネルギー結合を作って活性化させる。しかし、ATPの加水分解とタンパク質や多糖の合成とを結ぶ機構は、グルタミン合成の場合よりかなり複雑である。これらの巨大分子の生合成径路では、一連の高エネルギー中間体を経て最終的な高エネルギー結合ができ、これが縮合の段階で開裂する。
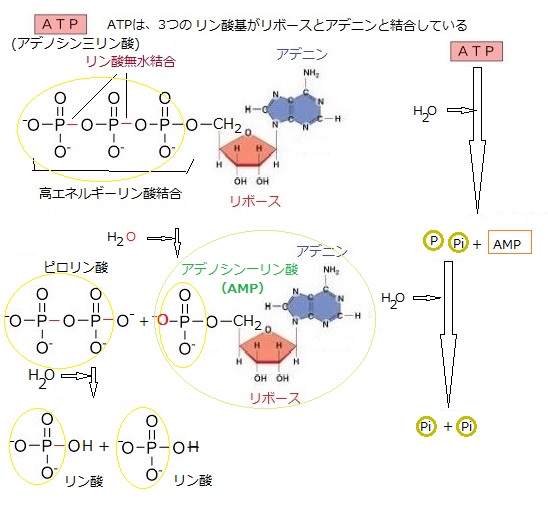
1つの活性運搬体が、生合成を押し進める能力には限界がある。例えば、ATPがADPと無機リン酸(Pi)に加水分解される反応のΔGは、全反応物の濃度に依存し、細胞内の普通の条件では、-11ないし-13kcal/molである。適切な反応径路があれば、原理的には、この加水分解でΔGが+10 kcal/mol程度までの反応なら起こせるということである。しかし生合成反応の中には、-13kcal/molでも足りないものがある。そんな場合には、ATPが加水分解してピロリン酸が生じ、その後の溶液中でピロリン酸がリン酸基に加水分解される径路もある。加水分解が2回続いて起こる。2回とも、水分子H2Oの酸素原子が生成物に取り込まれるが、水素原子は解離して、遊離の水素イオンH+となる。
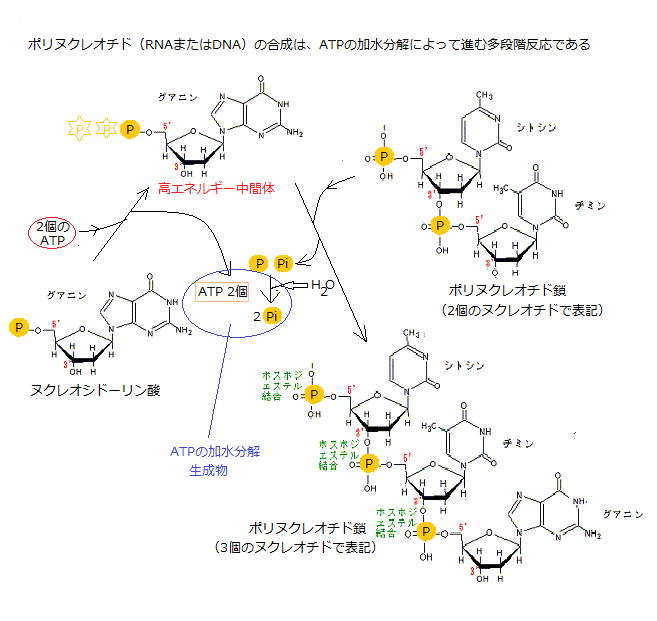
ATPはまずAMPとピロリン酸(PPi)に加水分解され、その後ピロリン酸が溶液中で加水分解される。こうすると、全体で約-13kcal/molの△Gが得られる。こうして進む例として核酸(ポリヌクレオチド)、RNAまたはDNA合成に関わる反応で、ATPの加水分解で進む多段階反応である。
ヌクレオシドーリン酸が、末端のリン酸基を2個のATP分子から続けて受け取り活性化する。これにより高エネルギー中間体として形成されたヌクレオシド三リン酸は、遊離状態で溶液中にあった後、伸長中のRNAかDNAの末端と反応してピロリン酸基を放す。ピロリン酸基の無機リン酸への加水分解は非常に起こりやすく、反応全体がポリヌクレオチド合成に向かう補けになる。
目次へ