 |
| |
|||||||||
|
|||||||||
| デモクリトスは、紀元前470年頃~370年頃の古代ギリシャの哲学者で、エーゲ海北岸に位置するアブデラに生まれた。およそ百歳まで生きた、人類史上もっとも進歩的な思想家であった。 デモクリトスは、近代物理学の力を借りることなく、すべては原子でできていると言う着想を得た。デモクリトスは、物質の基本構成要素に、ギリシャ語の「atomos(分割できない)」にちなんで「原子(アトム)」と言う名を付けた。その説には、「素粒子」と言う概念のルーツがあった。 アリストテレスが、デモクリトスの着想を、その著書「生成と消滅について」で引用している。「物質の欠片は何であれ、個別の、それ以上には分割できない有限個数の小片から構成される。そのそれぞれの小片には、それ以上は小さく分けようがないと言う意味で、有限の寸法がある。その小片が原子である」と、粒子加速器もなかった時代に、物理の基礎となる、物体は原子から成り、物体は原子の運動や分離などにより変化するとした量子化学の理論の骨格にまで達していた。 「万物は原子からなる」と言う短い一文から、宇宙に関する膨大な情報までも読み取れるほど科学は進化していた。 |
|||||||||
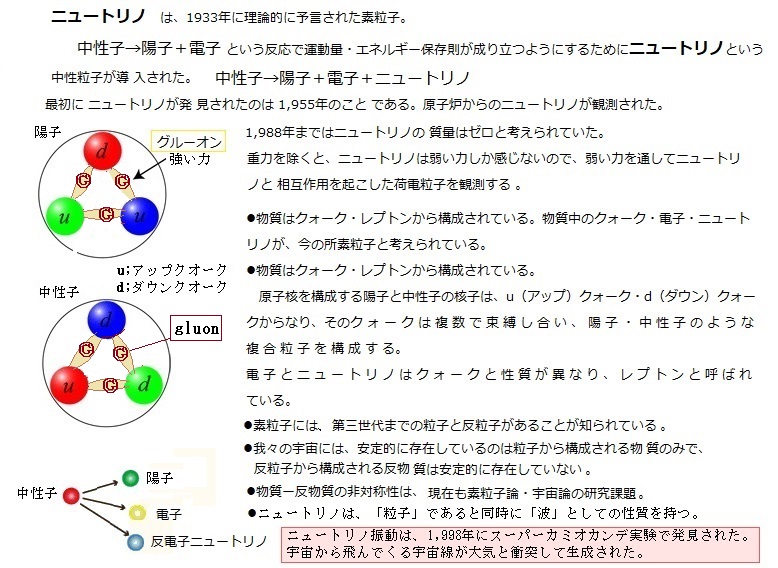
| 1)素粒子の発見 素粒子は、宇宙にあるものすべてを構成する基本単位で、そのすべての性質は、素粒子の性質から生じている。現代の科学力では、少なくともそれ以上基本的なものに還元できない。そのため、原子は素粒子に含めない。1897年、「電子」が発見され、1911年には「原子核」が、1919年に「陽子」が、1932年には「中性子」が、1964年、「陽子」や「中性子」を構成する「クォーク」という「素粒子」の存在が予言され、1969年にはアメリカの加速器実験で「クォーク」の存在が証明された。 物質の究極の構成要素は、「クォーク」と「レプトン」であると考えられ、いずれも「世代generation」と呼ばれる、くり返し構造がある。  原子は電子eと陽子、中性子からできており、陽子と 中性子はさらに小さなアップクォークuとダウンクォー クdでできている。このe・u・d が、人の体を作る素粒子であり、宇宙
を飛び交う電子ニュートリノνeもまた素粒子である。 原子は電子eと陽子、中性子からできており、陽子と 中性子はさらに小さなアップクォークuとダウンクォー クdでできている。このe・u・d が、人の体を作る素粒子であり、宇宙
を飛び交う電子ニュートリノνeもまた素粒子である。素粒子には、素粒子物理学が 「世代」と呼ぶくり返し構造がある。 「d・u・e・νe」が第1 世代の素粒子であり、安定していて、この宇宙の構成要素となっている。このそれぞれの素粒子と電荷やスピン(素粒子の「自転」のような性質、粒子が持つ固有の角運動量)などあらゆる性質がまったく同じだが、素粒子の質量だけが重い第2世代の粒子の組「ストレンジクォークs・チャームクォークc・ミューオンμ・μ(ミュー)ニュートリノνμ」と、質量が さらに重い第3世代の組「ボトムクォークb・、トップクォークt・タウ粒子τ・τ(タウ)ニュートリノντ」が存在する。素粒子標準理論では、ボトム・クォークやタウ粒子は第3世代の粒子であるが、第3世代の粒子が崩壊するときには、第3世代より軽い第1世代や第2世代の粒子に壊れる。 2012年、大型ハドロン衝突型加速器 Large Hadron Collider (LHC)で発見され たヒッグス粒子が、「質量を与える粒子」と言われのは、エネルギーを持った「ヒッグス場」が、ヒッグス場ひとつで、物質を形成している物質粒子と、素粒子の力を媒介する粒子の両方に質量を与えていると考えられている。このヒッグス粒子の性質からも、標準理論の枠内にあり、3世代から先はないと考えられている。 ヒッグス粒子Higgs bosonと言う呼び名は、これを発案した複数の物理学者の一人にちなんで付けられた。光子が磁場を作るように、このヒッグス粒子は、「ヒッグス場」と言う場を作り、空間のいたるところに、そのヒッグス場を満たす。 粒子は、そのヒッグス場と相互作用することで質量を獲得する。第3世代のトップクオークのように重い粒子はヒッグス場と強く結びつき、電子のような軽い粒子は弱く結びついている。この粒子が質量を獲得するメカニズムを、ヒッグス・メカニズムと呼ぶ。 高エネルギー加速器研究機構の「東京大学、ATLAS日本グループ」は、2018年6月7日、フランスとスイスの国境にある欧州合同原子核研究機関 (CERN) の大型ハドロン衝突型加速器 (LHC) で、もっとも重い素粒子である第3世代のトップクォーク対とヒッグス粒子が同時に生成される反応を初めて観測した、と発表した。この反応が起こる確率は、誤差の範囲内で標準理論におけるヒッグス機構の予想と一致しており、トップクォークの質量がヒッグス機構と一緒に生成されるという、極めて稀にしか起きない反応を、かなりの精度で捉えることができたのである。最も重く、他の素粒子と比べて数桁も大きな質量をもつトップクォークも同機構で生成されたため、力を伝える素粒子ばかりでなく、物質を形作る素粒子の質量の起源もヒッグス機構だったことが分かり、ヒッグス機構の全貌解明に向けた大きなマイルストーンmilestone(プロジェクトを完遂するために重要な中間目標地点)となった。 現在では、原子は素粒子に含まれず、それを構成する陽子や中性子も素粒子ではない。1930年代に発見された新粒子の大半は、宇宙線の観測で発見された。しかも、粒子加速器が使えるようになった1950代以降でさえも変わらず成果を挙げ続けている。 地球大気に突入する一次宇宙線は、宇宙に起源する宇宙線で、超新星の爆発や太陽表面の爆発などで発生した高エネルギーの粒子である。約90%が陽子、約8%がアルファ粒子(ヘリウムの原子核)、その他の粒子が約1%含まれている。一次宇宙線空気中の酸素分子や窒素分子と衝突し 、その高エネルギーに依り原子核を破壊し、中間子と呼ばれる新たな粒子を多数作り出す。 一次宇宙線は、大気分子の原子核と衝突しては核反応を起 こし、その都度にエネルギーを与え、それに反比例して持っていたエネルギーを徐々に奪われる。最終的には、地上 に到達する前に二次粒子を発生させながら消滅する。 その生成された中間子もまた高速で周りの原子核に衝突しさらに多数の中間子を生み出し、粒子の数をねずみ算的に増幅しながらエネルギーを落としていく。このうち寿命が短いものはすぐに「崩壊」し、最終的には、1,000億個もの比較的エネルギーが低いミューオン・ニュートリノ・中性子・ガンマ線や電子・陽電子となって地上に降り注ぐ。 宇宙で発生し高エネルギーの一次宇宙線が、大気と衝突し反応して生じる大量の粒子となって地表で検出される二次宇宙線である。この二次宇宙線のシャワーが、「空気シャワー」で、ミューオンやニュートリノ、陽電子などは、「空気シャワー」の観測により発見された粒子である。宇宙線研究は素粒子物理学の発展に大きく貢献をしてきた。 1964年、陽子や中性子を構成する「クォーク」という「素粒子」の存在が予言され、1964年に、マレー・ゲルマンとジョージ・ツワイクが発表したクォークモデルでは、アップクォーク・ダウンクォーク・ストレンジクォークの3種類で構成されていた。1965年には、シェルドン・グラショーとジェームス・ビョルケンによって4種類目のクォークであるチャームクォークの存在が予言された。1969年にはアメリカの粒子加速器の実験で「クォーク」の存在が実正された。1973年には、小林誠と益川敏英によって、クォークが3世代6種類存在し、未発見のトップクォークとボトムクォークの存在が予言された。 ボトムクォークは1977年に、トップクォークは1995年に、実験でこれら3世代6種類全てのクオークの存在が実証された。2008年、小林誠と益川敏英は、この功績によりノーベル物理学賞を受賞した。同様に、素粒子の電子の仲間である「レプトン」も6種類あるとされた。すべて20世紀の発見であった。 現在では、水素などの物質に関わる素粒子は、宇宙全体の4%しかなく、正体不明の暗黒物質が23%、暗黒エネルギーが73%と大部分を占めていることが明らかになった。 「地球とリンゴの大きさの比は、リンゴとリンゴの中の原子の大きさの比とほぼ等しい」 地球をE、リンゴをA、原子をaとすると、E:A≒A:aとなるほどの小ささで、それでも多くの量子の中では、原子が最大の大きさとなる。通常、実際の原子半径は約10-10m=1Å=1/100億mである。 さらに実験をしてみると、原子核は原始の質量の大部分、99.98%以上を占めていながら、そのサイズは非常に小さく、原子の体積の僅か千兆分の一である。 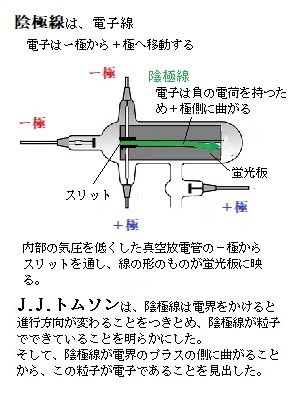 1897年、物理学者であるJ.J.トムソンJoseph John Thomsonは、ケンブリッジ大学で新しい放電管を使用した陰極線の実験により、陰極線の正体が電子であることをつきとめ、電子の存在を明らかにした。
空気を抜いて放電管(蛍光管に似たもの)の両端に電極を置き、内部の気圧を低くし真空度を上げていくと、陰極に近いガラス壁が発する陰極線が、スリットを通して緑色の光の「線」となって蛍光板に映る。トムソンはさらに放電管の中の空気を抜き、中の気圧を下げて陰極線を計測しようと試みた。 1897年、物理学者であるJ.J.トムソンJoseph John Thomsonは、ケンブリッジ大学で新しい放電管を使用した陰極線の実験により、陰極線の正体が電子であることをつきとめ、電子の存在を明らかにした。
空気を抜いて放電管(蛍光管に似たもの)の両端に電極を置き、内部の気圧を低くし真空度を上げていくと、陰極に近いガラス壁が発する陰極線が、スリットを通して緑色の光の「線」となって蛍光板に映る。トムソンはさらに放電管の中の空気を抜き、中の気圧を下げて陰極線を計測しようと試みた。その結果、トムソンは、陰極線は電界をかけると進行方向が変わることにより、陰極線が粒子であることを突き止めた。しかも、陰極線が電界のプラスの側に曲がることから、この粒子が負の電荷を帯びていることを見出した。これが契機となって、その粒子がどんな原子の内部にも潜んでいることを知り、その粒子を「電子electron」と名付けた。電子はすべて負の電荷を帯び、電子の質量は極めて小さく、原子の質量の二千分の一しなないことなどを明らかにした。 トムソンにより、質量が非常に小さい、負の電荷を帯びた電子が、原子の内部に少なからず存在し、原子は通常、電気的に中性であり、全体的には電荷を持たないが、原子から電子を奪うと、原子は電子と逆の正電荷を帯びる。つまり原子の「イオン化」である。 原子の内部には、電子の負電荷と同量の正電荷が含まれていることまで分かった。1904年、J.J.トムソンは、正の電荷は原子の内部に均等に広がり、負の電荷の電子はレーズンパンの干しブドウように均一に、原子の内部に配置されているとする「原子モデル」を提唱した。 この「原子モデル」はともかく、電子の画期的な発見によりトムソンは、「現代素粒子物理学の父」と呼ばれる。これらの功績から、1906年、J.J.トムソンはノーベル物理学賞を受賞した。 1909年、ラザフォードとその教え子は、アルファ(α)粒子を薄い金箔に打ち込むと、ごくわずかではあるが後方にも散乱されることを発見した。ニュージーランド出身で、イギリスで活躍した物理学者であり、化学者のラザフォードが、「ラザフォード散乱」による原子核の発見と、原子核の人工変換などの業績により「原子物理学の父」と呼ばれる。 1919年、ラザフォードは、窒素を酸素に人工的に変換することに成功した。人工的に原子核を変化させることを「原子核変換」という。原子核に核子(陽子、中性子)や他の原子核を衝突させることで、陽子と中性子の組み合わせが変わり、異なった原子核が生成される。 水素原子は、たった1個の陽子 protonの原子核と1個の電子からできている。水素原子から電子が1個剥ぎ取られた水素イオンは、水素の原子核、すなわち陽子である。  ラザフォードは、原子によるα 線の散乱実験の一環として、窒素ガスの中に放射性物質を置き蛍光物質上の発光を調べたところ、時々、α粒子とは考えられない方向に非常に明るい発光を観測した。これは、高速のα
粒子が原子の原子核に衝突して、 何か「不明の」 高エネルギーの 荷電粒子が飛び出したと考えた。精密に解析した結果、この不明な粒子が水素イオンと同じ物であることが分かった。 ラザフォードは、原子によるα 線の散乱実験の一環として、窒素ガスの中に放射性物質を置き蛍光物質上の発光を調べたところ、時々、α粒子とは考えられない方向に非常に明るい発光を観測した。これは、高速のα
粒子が原子の原子核に衝突して、 何か「不明の」 高エネルギーの 荷電粒子が飛び出したと考えた。精密に解析した結果、この不明な粒子が水素イオンと同じ物であることが分かった。このラザフォードによる原子核の人工変換の実験によって、陽子が原子核を構成する粒子の1つであることが明らかになった。 (窒素の原子核;原子番号7) + (ヘリウムの原子核;原子番号2) → (酸素の原子核; 原子番号8) + 陽子(水素イオンH+;原子番号1) この核反応には9個の陽子と9個の中性子が参加している。しかも、水素の電子は、エネルギー準位の低いK殻に1個あるだけである。そのため、これを失ってH+イオンになりやすい。原子番号が1より小さい、つまり原子核に陽子がない元素は存在しないため、イオン化しても原子番号は1である。 原子核は崩壊によって他の原子核へと変化する。すべての原子核が崩壊するのではない。しかし、中性子数と陽子数のバランスによっては、核力によって原子核を維持することができなくなる。このため、中性子と陽子の数の組み合わせが適切でない原子核は、時間の経過とともに放射線を出して他の原子核へと変化する。ただ、崩壊する原子核と崩壊しない原子核がある。それぞれを、「放射性同位体」、「安定同位体」と呼ぶ。 核種とは、原子番号・質量数・エネルギー状態によって特徴づけられる原子核あるいは原子の種類である。原子番号が同じで質量数の異なるものを同位体といい、原子番号・質量数が同じでエネルギー状態の異なるものを核異性体と言う。 炭素の同位体には、炭素8から炭素22まで15種類が知られており、そのうち2種類、炭素12と炭素13が安定している。長寿命の放射性同位体である炭素1414Cの原子核は、6個の陽子と8個の中性子からなるが、β崩壊して窒素1414N、その原子核は7個の陽子と7個の中性子となる。半減期は5,700年である。これにより年代測定に利用される。 ある種の原子核は不安定で、ある時、電子(β線;原子核から放出される電子で、ベータ粒子とも言う)を放出して別の元素の原子核になる。その過程で、ある粒子が自然に壊れて別の複数の粒子ができることを「崩壊する」と言う。例えば、通常の水素は1Hであり1Hであるが、3重水素は、陽子1個と中性子2個を持つ。3重水素がβ崩壊して、ヘリウム3(3He)になる。ヘリウム3の原子核は、陽子2個、中性子1個で、通常のヘリウムより中性子が1個少ない。 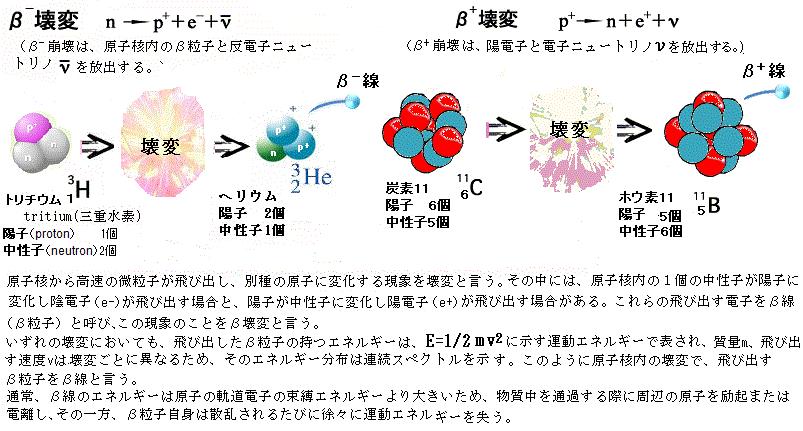 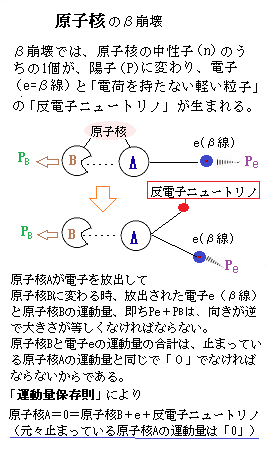 このように、β崩壊は、止まっている原子核が電子1個と別の粒子の原子核に分かれる反応と考えられていた。しかも、崩壊後の観測でも確認されている反応でもある。ところが、放出された電子のエネルギーが、崩壊のたびに異なっていることも観測されていた。 このように、β崩壊は、止まっている原子核が電子1個と別の粒子の原子核に分かれる反応と考えられていた。しかも、崩壊後の観測でも確認されている反応でもある。ところが、放出された電子のエネルギーが、崩壊のたびに異なっていることも観測されていた。つまり、元の原子核をA、崩壊後の原子核をB、放出される電子をe(β線)とすれば、実験結果では、電子eのエネルギーが一定しないのである。物理学の基本原理では、崩壊前後でエネルギーと運動量は、同一で保存されていなければならないはずだ。もし電子eがある運動量Peで放出されたとすれば、崩壊で生まれた別の原子核Bは、反対方向に電子eと同じ運動量PBで放出されなければならない。と言うのも、元々止まっていた原子核Aの運動量は0なので、Bとeの運動量の合計は、「運動量保存の原則」により0のはずだ。しかし、実験結果では、崩壊後の電子eと原子核Bのエネルギーの合計は、崩壊ごとに違っていた。 1930年、ヴォルフガング・パウリは、原子核は電子eと別の原子核Bの2つの粒子だけでなく、電子eと別の原子核Bばかりでなく、それから「未知の軽い電荷を持たない粒子」の3つに壊れる、と言う仮説を立てた。 パウリの提案により、1934年に、エンリコ・フェルミは、β崩壊の理論を完成させた。「原子核を構成する中性子nうちの1個が陽子Pに変わり、同時に電子e(β線)と電荷を持たない軽い粒子が生まれる」。 イタリア人のフェルミは、この「電荷を持たない軽い粒子」を「ニュートリノneutrino」と名付けた。「中性neutral」と言う文字に「(質量が)小さい」を意味するイタリア語の接尾語「-ino」を加えた造語であった。正確には「反電子ニュートリノ」である。 フェルミは、電荷を持たないニュートリノが、どのくらいの頻度で反応するかも予言したが、物理学の理論として認められるには、実験によりその存在が示されなければならない。 1950年代にフレデリック・ライネスとクライド・コーワンが、核分裂反応に伴って大量のニュートリノが放出されることに着目し、原子炉で生成されるニュートリノを観測することに成功した。 原子炉の中では、ウランに中性子が当たって核分裂する際に生じるエネルギーを利用して電力を作り出す。核分裂で生じた原子核の多くはβ崩壊をしており、そのためニュートリノが大量に放出されている。彼らは、それに着目し、原子炉近くに「液体シンチレータ」と言う特殊な液体が入った測定器を置き、ニュートリノと僅かに起こる反応の観測に成功した(シンチレータとは、放射線に励起して発光する特殊な物質の総称)。 ライネスは、この発見から約40年後の1995年、ニュートリノの発見でノーベル物理学賞を受賞した。コーワンの方は、可哀そうに1974年に亡くなっていた。 1920年、ラザフォードは、英国王立協会の講演で中性子の存在を予想している。中性子は、陽子と電子が水素原子を形成する場合よりも更に密接に核子として結合している。電荷が0で質量は水素原子にほぼ等しい。つまり陽子と同じ質量と考えていた。 ラザフォードが使ったアルファ粒子は、ラジウム元素の放射性崩壊、つまり放射線を放出しながら、重い原子からより軽い原子に変わる際に飛び出す+2の電荷を持つ荷電粒子線である。 ラジウム元素はキュリー夫妻により1898年に発見され、ラテン語の放射能にちなんでラジウムと命名された。ラジウムは、アルファ崩壊してラドンになる。その放射性崩壊の際、原子核から放出される粒子は、陽子2個・中性子2個からなるヘリウムの原子核そのもので、それがアルファ粒子である。 加速器は作られていない時代、ラジウムは、アルファ粒子を加速する天然の加速器であった。アルファ線は物質中を直進する。ラザフォードの研究により、アルファ線が電子よりも十分重いため(約7,000倍)、軌道電子であれば何回衝突してもアルファ線の方が曲がることがないことが知られていた。しかも、小さなエネルギーでありながら、非常に短い量子的波長を持つため、原子の内部を深く探知できる優れた能力がある。 1906年に、アルファ線は細いスリットslit(隙間)を通したとき真空中では直進するが、スリットに金箔を張ると、それによってわずかに「前方錯乱」されてビームbeamが広がることが分かっていた。ラザフォードはガイガーとマースデンの協力を得て、1908年から1913年にかけてアルファ線の物質中での「前方錯乱」を精密に測定していた。これはあくまでも万全を期するためであるが、入った方向へ戻る「後方錯乱」する粒子もあるかチェックした。すると8千回に1個の割合で、アルファ粒子が、アルファ線源の方に戻ってきた。 ラザフォードの回想録には、「それはまるで、15インチの砲弾を、1枚の紙切れに向けて発射したら、砲弾があなたの方に戻ってきて命中したようなものだ」と、つまり、原子の内部には、正の電荷を帯びた重いアルファ粒子を跳ね返すほどのものがあったのである 薄い金箔(空気圧下で換算して約0.4mm)を反射板として重ねていくと、最初は枚数に比例して反射されるアルファ線の数は増加していくが、20枚ほど(空気圧下で8mm)で飽和に達した。また、反射されるアルファ線の数は反射金属板の原子番号が大きいほど増加した。この実験の積み重ねは、多くの示唆に富むものであった。 19世紀の終わりから20世紀にかけて、直径10-8㎝位しかない原子の内部にも構造があることが分かってきた。1897年、J.J.トムソンが負の電荷を持つ粒子(電子)を発見して、「ブドウパンのような原子モデル」を提唱した。 ジャン・ペランは、1890年代は陰極線の研究を行っていた。1901年、原子核の周りを電子が回っている「核―惑星モデル」を発表した。 長岡半太郎は1904年、中央に正電荷を帯びた原子核があり、その周りを土星の輪のように多数の負電荷を帯びた電子が周回すると言う「土星型原子モデル」を発表した。 ラザフォードは、アルファ線の物質中での「後方錯乱」の実験によるデータから、ペランや長岡の予想より、原子核は極めて微小で、その微小な領域に原子の質量の殆どが集中していることを突き止めていた。 1904年に、J.J.トムソンが提唱した「レーズンパン」の原子モデルでは、アルファ粒子の「後方錯乱」の現象を説明できないほどの、「後方錯乱」が起きる、原子の核心部に極めて微小な領域、つまりアルファ粒子が8千回に1個の割合で跳ね返すほどの極限領域に、原子全体の質量と正の電荷が集中しているからである。これが「原子核」が明確に表現された瞬間であった。 また、原子内の電子は、中心部に密集する正の電荷を帯びる原子核の周囲を回っていたのだ。正の電荷の原子核と負の電荷の電子が引き合って原子を一つまとめている。さらに実験を重ねると、原子の質量の99.98%以上が原子核に集中しているのに、そのサイズは余りにも極小で、その体積は原子の体積のわずか千兆分の1であった。 しかし、ラザフォードの飛ぶ抜けた原子論であっても、最も巨視的な観点から観察される太陽系と同様に、原子の世界でも「ミニチュア太陽系モデル」として、古典的物理学の法則が成り立っていると考えていた。しかし、ラザフォードの実験によるデータは、現代の物理学を席巻する「量子化学」を誕生させる契機となった。 目次へ |
|||||||||
| 2)量子力学の父と呼ばれるニールス・ボーア 「量子力学の父」と呼ばれるニールス・ボーアNiels Henrik David Bohrは、1,885年、北欧三国のひとつデンマークに生まれた。デンマーク・スウェーデン・ノルウェーの三国は、民族的にはゲルマン人の一系統のノルマン人(ヴァイキングの子孫)であり、かつては連合王国でもあって関係が深く、特に北欧三国と呼ぶこともある。 フィンランド共和国の圧倒的多数は、ウラル語族のフィン人である。ウラル語族は、北アジアのシベリア中北部、北ヨーロッパ、東ヨーロッパに話者地域が分布する語族である。北欧三国とは民族的な繋がりが弱いようだ。 ニールス・ボーアの父親はコペンハーゲン大学の生理学教授であった。 アインシュタインは6歳年上になる。 アインシュタインは、ニールス・ボーアに 「あなたは本当に、神がサイコロ遊びのようなことに頼ると信じますか?」 それに対して、ニールス・ボーアは、切り返して 「あなたは、物の性質をいわゆる神の問題に帰するときには、注意が必要だと思いませんか?」 こう答えたのが、アインシュタインと20世紀の科学を代表するもう一人の天才物理学者ニールス・ボーアである。しかも、アインシュタインがノーベル物理学賞を受賞した翌年1,922年に、同賞を受賞したのがニールス・ボーアであった。 「量子」の概念は1900年にマックス・プランクが初めて導入したが、その発展の初期に最も貢献したのが、他ならぬアインシュタインである。アインシュタインの有名な仕事は相対論や重力論だが、1921年にノーベル賞を取ったのは「光量子仮説に基づく光電効果の理論的解明」に対してであり、その翌年の22年には、ボーアが「元素の周期律の理論」の業績でノーベル賞を受賞した。 その後、「元素の周期律の理論」で予測されていた新元素が、ボーアの研究所で発見され、ハフニウムと命名されている。ボーアは、後に、原子力爆弾も作れる「原子核の液滴模型」を生み出した。1940年、母国がドイツ軍に占領され、一家でスウェーデンに逃れた。その後息子の A.N.ボーアとともにイギリスやアメリカで原子爆弾開発に協力した。 アインシュタインは、ナチス・ドイツから亡命して間もない1939年、アメリカ大統領フランクリン・D・ルーズベルトに宛てた、原子爆弾の開発を求める2ページにわたる書簡に署名し送った。アインシュタインは、ナチス・ドイツが核エネルギーを使って、「 船で運ばれ港で爆発すれば、この種の爆弾ひとつで、港全体ならびにその周囲の領域を優に破壊する」ことを懸念していると書いていた。そして、「ドイツは、ドイツが接収したチェコスロバキアの鉱山からのウランの販売を停止しています」と危機をあおっている。この書簡が、広島と長崎に投下された原爆の開発「マンハッタン計画」へとつながった。アインシュタインは、ルーズベルトに警告したが、当時、ウランが都市ごと壊滅させるような強力な爆弾となりうるということは、新聞などで一般にも知られていた。後に、ドイツの原爆開発が、それほど間近に迫っていなかったことを知り、この書簡は「大きな誤り」だったと認めた 。 ボーアは1,912年、当時マンチェスター大学で研究していたラザフォードを訪ね、4ヵ月ほどその地に滞在するつもりであった。そこでラザフォードが、原子は「ミニチュア太陽系モデル」と言う説には、それまでの物理法則によれば、成立し得ない重大な欠点があることを知った。 ボーアは、原子核の周りを高速で円運動している電子は、そのエネルギーすべてを瞬時に電磁波として放出するため、1秒の10億分の1の100万分の1の10分の1と言う瞬時に、電子の軌道から原子核まで距離がゼロになる。電子はくるくると螺旋を描きながら、即時に原子核に墜落する。 つまりニュートン物理学に基づくマクスウェル(19世紀を名実ともに代表する最も偉大な物理学者。電磁場の理論の提唱と気体運動論の研究という二つの領域で後世に多大な影響を与えた)が作り上げた精緻な電磁気学の方程式は、原子の世界では成立していない。ラザフォードの原子モデルが誤りなのか、ニュートン以降の物理学の法則では答えが出せないのではないか、と極めて困難な問題に直面した。 ボーアをはじめてする当時の原子構造研究者の苦闘は、「量子力学」の言葉すらない時代に,それをどう説明するかにあったと言える。ボーアが辿り着いた原子の構造は、「原子核の周りを公転運動するn 個の電子のリングが軌道している」というものであった。しかし、このような構造では「周回する電荷は、電磁波を放射し運動エネルギーを失うため、電荷は安定して円軌道に留まれない」というやっかいな「不安定性」の問題が起こる。それでも、現実の原子や、ラザフォードの実験でも、そんなことは決して起こらない。これが当時の原子構造に取り組む研究者を悩ませていた主要な課題の一つであった。  そんな問題を解決する最初のステップが、水素原子の発光スペクトルにあった。エネルギーを与えられた原子は、その原子固有の振動数で発光する。水素原子を真空管のなかに少しだけ入れて放電させると光を発するが、その波長は、バルマー系列と呼ばれ、水素原子の線スペクトルのうち可視光から近紫外の領域にあるものである。水素原子からの輻射される電磁波の波長は整数m、n(n>
m> 0)を含むことから解るように、不連続で飛び飛びの値 となる。 そんな問題を解決する最初のステップが、水素原子の発光スペクトルにあった。エネルギーを与えられた原子は、その原子固有の振動数で発光する。水素原子を真空管のなかに少しだけ入れて放電させると光を発するが、その波長は、バルマー系列と呼ばれ、水素原子の線スペクトルのうち可視光から近紫外の領域にあるものである。水素原子からの輻射される電磁波の波長は整数m、n(n>
m> 0)を含むことから解るように、不連続で飛び飛びの値 となる。原子のスペクトル線それぞれの、電子のエネルギー準位間の遷移は、吸光・発光により説明される。水素原子の線スペクトルのうち、可視光の領域に現れるものとして以下の4つの線が確認され命名されていた。それぞれHα線(656.28nm)、Hβ線(486.13nm)、Hγ線(434.05nm)、Hδ線(410.17nm)。 原子はプラスの電荷を持つ原始核と、マイナスの電荷を持つ電子からなるが、電荷を持つものの間に働くクーロン力Coulomb force(静電気力)は、本質的に、極めて強力である。二つの荷電粒子間に働くその力は、粒子間の距離の2乗に反比例し、双方の電荷の積に比例する。それが電磁気学の基本法則であり、クーロンの法則Coulomb's lawと呼ばれる。 電荷の符号が正負であれば引力となり、同じであれば斥力が働く。 しかし、万有引力の質量を電荷に変え、万有引力定数をクーロンの比例定数に変えるだけであるが、万有引力の式では質量がマイナスになることはない。そのため、万有引力の場合は斥力が働かない。 電荷はマイナスもありうることから大きな違いが生じる。私たちの身の回りある物質は、プラスの電荷とマイナスの電荷が、厳密に同じ数だけ存在するため、互いの力を打ち消し合って平静な均衡を保っている。 しかし、このバランスの背後には、粒子間の激しい力の相克が潜んでいる。この静寂状態にある物質に光が入射すると、光を受けた電子が振動し励起状態になり、外側の軌道へジャンプし、原子同士・分子同士の結合状態が変わり、物質本来の激しい本質が露呈される。  物質の本性は、その安定したバランスが失われ励起状態になった時に初めて明らかになる。 光合成色素系のカロテノイドやクロロフィルによるエネルギー移動は、太陽光の吸収から反応中心までの励起エネルギーの運搬過程を示す。光が励起状態に関与する場合でも、従来提唱されていた電子交換相互作用ではなく、クーロン相互作用であることが最近、明らかにされている。 物質の本性は、その安定したバランスが失われ励起状態になった時に初めて明らかになる。 光合成色素系のカロテノイドやクロロフィルによるエネルギー移動は、太陽光の吸収から反応中心までの励起エネルギーの運搬過程を示す。光が励起状態に関与する場合でも、従来提唱されていた電子交換相互作用ではなく、クーロン相互作用であることが最近、明らかにされている。植物は、光合成により、光のエネルギーを使って、空気中の二酸化炭素と地中の水から、炭水化合物など豊富な有機化合物を生成する。 動物界は、植物が供給する有機化合物に頼り生命を維持している。 その一方、光のエネルギーによるテクノロジーは、未だ人類の能力では捉えきれずにいる。 1913年2月、ボーアは知人から水素スペクトルに関するバルマー公式のことを耳にする。ボーアは後年、「この式を知るやいなや、あらゆるものがおさまる所におさまった」と語っている。 当時、注目されて始めた量子は、粒子性(物質の性質)と波動性(状態の性質)を併せ持つ、特殊な存在である素粒子であるため、原子の内部にある電子も波動性があり、その軌道もある種の特殊な条件を満たすものに限られるのが存在する。 弦楽器や管楽器は比較的澄んだ音の周波数frequency分析してみると、色々な周波数が含まれていることが分かる。しかも、それを構成しているいくつかの周波数が、簡単な整数比となっている。 特に、多くの音は基本となる周波数と、それに倍数する周波数となっている。これらを一般の波動では基本波fundamental waveと高調波harmonic waveと言う。 音の場合では基音fundamental pitchと倍音harmonic tone とも言う。基音と倍音の混ざり具合、つまり強度分布が音色toneを決めることになる。人の声も、基音と倍音が完全な整数比になっている。 原子に結合している電子も、量子力学的な性質によって、とびとびの状態にある。その状態をエネルギー準位energy levelと呼び、エネルギー準位の中で、最もエネルギーの低い状態を基底状態ground state、 それ以外の状態を励起状態excited stateと言う。これらのエネルギー準位は、原子核から外側に向かって 量子数と呼ばれる自然数(n =1, 2, …)で番号づけられている。これが「倍音軌道」であり、それぞれの軌道はある種のエネルギーによって特徴づけられている。 「電子が振動すると光を含めた電磁波が生まれて、周囲に広がる」。 電子が速く振動すると振動数の大きな電磁波が起こる。逆に電子がゆっくり振動すれば、振動数の小さな電磁波ができる。 電子をより速く動かすには、より高いエネルギーが必要になる。高いエネルギーによって作られた電磁波は、やはり高いエネルギーを持っている。 振動数が大きい(波長が短い)電磁波ほど、エネルギーは高くなる。 一般的に「電子が振動すると、振動する電波と磁場が交互に発生し、高速度で空間に伝わっていく。これが電磁波である」と、実際の可視光付近の電磁波では、磁場が電子に与える影響は殆ど無視できほどである。ここでは、 「電子が振動すると、振動する電場が生まれて、その電場が波のように空間に伝わっていく。これが光(を含めた電磁波)である」 「電場とは電気的な力が働く場所」、物理学では「場」とは「空間が持つ性質」のことを言う。例えば電場に電子などの荷電粒子(電荷を持つ粒子)を置くと、その粒子は電気的な力を受ける。この「電場の振動が伝わる波」が、「光(電磁波)」になる。 電場の振動を伝える光は、何も介さずに無限の空間を、衰えることのない光速で進んでいける。 電子が振動すると電場の波=光(電磁波)が発生し周囲に伝わる。そこに別の電子があると、「光を受けると、電子が振動を始める」。その光を受けて、更に別の電子が振動し連鎖する。ただし、電子を振動させるためには、光が適度な振動数で振動していなければならない。その適度な振動数を「固有振動数」と言う。 「固有振動数に一致する振動数の光(電磁波)が来ると、電子はその固有振動数で振動する。これを共鳴または共振と呼ぶ」。 音叉の場合は、振動を伝える光の代わりに音が果たしている。 電子が、基底状態や励起状態、電離状態の間を移り変わる際には、光の放出や吸収が起こる。光を放出したり吸収したりして基底状態や励起状態、 電離状態の間を移り変わることを遷移transitionと呼ぶ。 基底状態や励起状態は、とびとびのエネルギー準位になっているので、それらの間を電子が遷移する際に放出・吸収される光のエネルギーも、とびとびになる。つまり、変化前の状態のエネルギーを E1、 変化後の状態のエネルギーを E2、そして 放出または吸収される光の振動数をνとすれば、 hν=E1 - E2 という関係が成り立つ(h はプランク定数)。この結果、原子のスペクトルは、 とびとびの線スペクトルになる。 一番低い基音は、人の耳が主として受け取る音であり、エネルギーが最も低い音である。電子の運動では、原子核に一番近い軌道にある時の波動が「基音」に当たる。その最低エネルギー状態の軌道上にあれば、電子はエネルギーを放出できない。それは電子が取り得る運動状態の中で、最もエネルギーが小さいため、これより低いエネルギーのものは存在し得ないからである。この特別な軌道の状態が「基底状態」なのだ。 これが量子論の特徴の1つで、原子が崩壊して消滅しないでいられるのは、量子的な波としての運動により支えられているからであり、ありうる限り最も低いエネルギーの状態、「基底状態」が存在するからである。 ボーアは、プランクとアインシュタインが導いた光のエネルギーに関する式 Ε=nhν (光子のエネルギー Eは振動数νに比例する。その比例定数をプランク定数 h といい、プランク定数 h = 6.63×10-34 J/s、「n」は定常状態にある「量子数」で、波長の整数倍である) に注目して、光のエネルギーがとびとびに決まるなら、電子のエネルギーもとびとびに決まっている考えた。 こうして、1913年3 月には、この年発表される三部作の最初の論文が完成した。 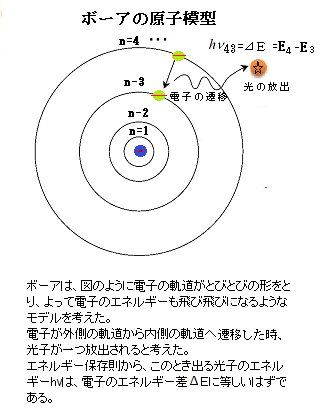 図にボーアの原子模型を示した。原子核を中心として同心円状に安定した電子軌道が不連続に存在し、ボーアはこれらを「定常状態」と名付けた。それらの軌道のエネルギーは増加順にEn(n
= 1,2,3 ⋅⋅⋅) と表記され、特にn = 1 の軌道を「基底状態」と呼び、最低エネルギーE1 を持つとした。円軌道の不安定性については、ボーアはそれまでの電磁輻射に関する知識を反古にし、単に「基底状態は安定である」と言明して破綻を回避した。 図にボーアの原子模型を示した。原子核を中心として同心円状に安定した電子軌道が不連続に存在し、ボーアはこれらを「定常状態」と名付けた。それらの軌道のエネルギーは増加順にEn(n
= 1,2,3 ⋅⋅⋅) と表記され、特にn = 1 の軌道を「基底状態」と呼び、最低エネルギーE1 を持つとした。円軌道の不安定性については、ボーアはそれまでの電磁輻射に関する知識を反古にし、単に「基底状態は安定である」と言明して破綻を回避した。原子は、その原子に特有ないくつかのエネルギー準位(定常状態エネルギー状態を言う)を持っている。 最もエネルギーの低い状態を基底状態、それ以外の状態を励起状態と言う。エネルギーの低いものから、第1励起状態、第2励起状態(n =1, 2, …)と呼ぶ。 原子内の電子は、光を吸収することによってエネルギーを手に入れ、より高いエネルギー準位へと移動する。一方、エネルギー準位の低い方へ原子が移動する時は、光を放射することによってエネルギーを外に出す。この様に、光を放出したり吸収したりしてエネルギー準位が移り変わる事を、遷移と呼ぶ。 電子は、高い軌道から低いエネルギーの軌道へ遷移することができる。その際に、電子は、ある決まった量の光のエネルギーを放出する。それが出発点と終着点となる2つの軌道のエネルギーの差となる。人の目には、2つの軌道の組み合わせに特徴的な色が見える。ボーアは、この「原子の量子論」を使い、放出された光子の波長を算出した。 原子が放出する光は、明瞭なスペクトル線として観測できる。スペクトル線は、水素ガスを高温に熱した時に放出される明るい光を、分光器を通せば観察できる。ボーアが導き出した式を使って計算した波長は、分光器を通した実際のスペクトル線の波長とまさしく一致した! 原子内の電子は、まさしく「ボーア軌道」を運動していた。 ボーアが用いた原子模型は、電子が粒子として円軌道を周回するもの、後にド・ブ ロイが提唱した粒子を物質波として捉えると、異なる描像が見えてくる。1923 年、ド・ブロイは「運動量p を持つ粒子は、λ = h/p の波長を持つ物質波と捉える事ができる」という考えを示した。原子核を 中心として同心円状に安定な電子軌道が不連続に 存在し、ボーアはこれらを「定常状態」と名付けた。それらの軌道のエネルギーは増加順にEn (n = 1,2,3 ⋅⋅⋅) と表し 、特にn = 1 の軌道を「基底 状態」と呼び、最低エネルギーE1 を持つとした。前述の円軌道の不安定性については、ボーア は、単に「基底状態は安定である」と言明して破綻を回避した。 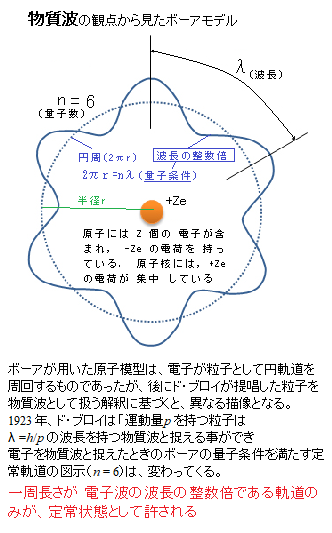 一方、n ≥ 2 の定常状態は準安定であり、電子はそこからそれより低い状態へと降りてゆける。例えばEa からEb (a > b)に降りるような遷移である場合には、プランク定数h
を用いて、ボーアの量子条件を物質波として表すと 一方、n ≥ 2 の定常状態は準安定であり、電子はそこからそれより低い状態へと降りてゆける。例えばEa からEb (a > b)に降りるような遷移である場合には、プランク定数h
を用いて、ボーアの量子条件を物質波として表すとEa − Eb = hνab で与えらえる振動数νab を持った光子1個放出される。原子が光子を1 個吸収した場合には,その逆向き の遷移が起こる。これは、現在の分光学の根幹をなす概念「スペクトル線 は系が2 つの定常状態間を遷移する際に放出され る輻射に対応する」で語られる。 ボーアが用いた原子模型は、電子が粒子として円軌道を周回するものであったが、後にド・ブ ロイが提唱した粒子を波として扱 う解釈に基づくと、異なる構図となる。1923 年、ド・ブロイは「運動量p を持つ粒子はλ = h/p の波長を持つ物質波と捉える事ができ、 n h / 2π =h rn / λ ⇔ 2π rn = n λ となる、とした。 ボーアの量子条件は、物質波の観点から「軌道の一周長さが 電子波の波長の整数倍である軌道のみが、定常状態として許される」と 理解される。 電子が波であるなら、円周の長さは、波の波長の整数倍でなければならない。電子が「波」として円軌道で周期性を保つためには、一周して戻ってきた時に元に戻らなければならない。一周して元に戻るには円周の長さが、波長の整数倍(1倍,2倍,3倍,...)でなければならない。整数倍でない場合には、元に戻れないので、「波」の干渉が起こり周期性が保てない。 原子内の電子が「ボーア軌道」を運動するなど、それをニュートンやガリレオの物理学で説明することは困難である。素粒子の現象を理解するためには、かつての物理学とは観点が異なる物理法則、それは過激な新理論であるが、その量子力学を発展させるしか説明がつかないのである。 物質を構成する原子・電子・光子・クウォーク・ニュートリノなどの粒子を研究する量子力学は、1910年頃にスウェーデンのコペンハーゲン大学のシュレディンガー、ニールス・ボーア、ハイゼンベルグなどの若き3人の天才学者によって提唱され、その微粒子は波動性と粒子性をもつため量子と呼ばれた。その振る舞いや法則の内容があまりに奇抜で、当時のアインシュタインを頂点とした物理学では全く理解できないため、その真実性について大論争を引き起こした。 この量子力学を打ち破るために世界中の著名な物理学者が数多くの実験を行なったが皮肉なことにすべての実験は、結果的に新しい量子物理学の正しさを証明することになった。20世紀の最初の数十年間に行われた実験によりはっきりとその振る舞いが示された。1,986年に、国際物理学会でその内容の正しさを認め、現在、様々な研究機関で量子力学を応用した新しい技術の開発や研究が進められている。 ラザフォードによって原子には正に帯電した原子核が存在していることが明らかになり、その後原子のモデルとして、原子核の周りを電子が円運動している状態が提唱された。しかし、電子は大きな速度で円運動するため、外部に電磁波を放出するため、そのエネルギーを瞬時に失い、一秒の十億分の一の百万分の一の十分の一と言う瞬間で、電子は螺旋を描きながら原子核に墜落するはずだ。これは原子がつぶれることを意味するが、現実ではそれはありえない。 そこで、ボーアは電子を粒子ではなく波としてとらえる原子モデルを考えた。つまり、原子の周りで定常波をつくるような波を電子としたのだ。このようなモデルで考えた、電子を1個のみ含む水素原子の半径のことを「ボーア半径」と呼ぶ。全体としての原子の大きさは「ボーア半径」によって定められる。水素原子の電子の基底状態(主量子数n=1)における軌道半径であり、この状態における水素原子の半径に相当する。 5.2917720859×10-11mとなる。 原子核はそれよりはるかに小さく、「ボーア半径」の僅か十万分に一しかない。この微細な領域を探るには、はるかにエネルギーの大きい粒子が必要になる。素粒子を加速すれば、その量子の量子的波長を短くすることができる。しかし高エネルギー粒子加速器が登場するのは1,950年代になってからである。 目次へ |
|||||||||
| 3)量子とは ニュートンが運動の法則と万有引力の法則を発見したのは17世紀で、江戸時代の初めに当たる。ニュートンの能力は卓抜している。この時代に、天空も地上も同じ物理法則に従っているのに気付いたことであった。リンゴの落果が、ビックバンまでに及び、宇宙も地球同様に、ニュートンが提唱した物理法則に従っている。 しかしながら量子化学が研究対象とする粒子の世界では、別次元の法則が働いている。 ニュートリノは、他の物質と殆ど反応しない。ニュートリノは、物質と相互作用(反応)する力が弱いからである。ニュートリノが、物質と相互作用する時に働く力を「弱い力」と呼ぶ。このミクロの世界で働く力には、他に3つある。先ずは「重力」で、それから「電磁力」、そして原子核の中で陽子と中性子を結びつけている「強い力」である。 「弱い力」は、文字通り弱い力で、陽子の大きさの1,000分の1ほどの距離にしか、その力は及ばない。基本的に「弱い力」は、電磁力と比べようもないほど、力の及ぶ範囲が非常に短い。そのため、ニュートリノの「弱い力」が発揮されるのには、「弱い力」が及ぶ距離まで接近しなければならない。つまり相互作用をするほどに、他の粒子に近づくことがごく稀であるため、物質中を極めて長い距離を走らないと相互作用は生じない。ニュートリノが、地球を容易く突き抜けることができるのも、そのためである。 「強い力」の意味合いは、電磁力と比べても強いからで、つまり原子核の中で正の電荷を持つ陽子同士は電磁的な反発力が働くので、その電磁力に勝る「強い力」が働かなければ、原子核を維持できない。また電荷を持たない中性子が、原子核内に留まれるのも、電磁力とは別の力が働いているからである。ただその「強い力」が及ぶ範囲は、原子核の内部くらいで極めて限定されている。そのため「強い力」とはいえ、「電磁力」のように日常生活では実感されない。 1934年(昭和9年)、湯川秀樹は、原子核の陽子と中性子を結びつける粒子、つまり「強い力」を伝える役割の素粒子が存在すると考え、「中間子」と名付けた。その「中間子」が、1947年に、イギリスの物理学者セシル・フランク・パウエルCecil Frank Powellの実験で、「写真乾板上」に、殆ど直角に曲がった粒子の軌跡が写し出された。これにより1949年(昭和24年)に湯川博士のノーベル物理学賞の受賞が決定した。翌1950年、セシル・パウエもノーベル物理学賞を受賞した。その理由は「写真による原子核崩壊過程の研究方法の開発および諸中間子の発見」である。パウエルの業績は、未だ中間子を生成できるほど高エネルギーの粒子加速器が存在していなかった時代に、湯川博士が予言した中間子を、「写真乾板」を使って発見したことにある。 1948年、戦時中に建設中止になっていた、粒子加速装置(シンクロトロンsynchrotron)がカリフォルニアで運転をはじめた。人為的に高エネルギー粒子を作り出す粒子加速装置は、宇宙線から粒子を見つけ出すより非常に効率がよい。このシンクロトロンにより、湯川の予言した「π(パイ)中間子」が、核子を結びつける粒子であることが証明された。 湯川秀樹が予言した「π中間子」は、素粒子として、また宇宙線の実験では非常に関わりが深い。特に「π中間子」の内で、プラスやマイナスの電荷を帯びるものは、飛行中に壊れて「ミューオン」や「ニュートリノ」になる。 一方、電気的な力は距離が離れていても、その力は感じられる。高速の電子を物質に入射すると、だいたい10cmも走れば、物質中の原子核や電子と電磁的な相互作用を起こす。特に、電子は負の電荷を帯びているため、距離が少し位離れていても電磁力の影響を受ける。 例えば、真空中で飛んできた電子が陽子 によって散乱される場合、 直接衝突しない場合でも、負電荷の電子は正電荷の陽子に電気的に引き付けられ、 軌道が曲がる。 その際、電子は真空中でどうやって陽子の存在を知るかと言えば、電子は陽子から飛んできた光の素粒子 「光子」を吸収することで陽子に気付き、電磁力を受ける。 つまり、荷電粒子は光子の交換を通じて電磁相互作用する。 宇宙では、超新星爆発や太陽表面の爆発などで発生した高エネルギーの電荷を持つ粒子がいつも飛び交っている。これは一次宇宙線と呼ばれていて、約90%が陽子1個でできた水素原子核、約9%が陽子と中性子が2個ずつでできたヘリウムの原子核、僅か1%が粒子やヘリウム原子核よりも重たい原子核になる。これらの粒子が地球の大気圏に突入すると、高度数10kmで空気中の窒素や酸素などの原子核と衝突し、核反応を起こして放射性同位元素を生成させたり中性子や陽子をはじき飛ばしたり、π中間子などの粒子を発生させたりする。 それらが崩壊して電子やγ(ガンマ)線、μ(ミュー)粒子、ニュートリノなどの粒子が作られ、この発生の様子は「空気シャワー」と呼ばれ、一次宇宙線の衝突で発生した粒子を二次宇宙線と呼ぶ。 高エネルギー粒子が、物質中で原子核と相互作用すると、多数の2次粒子が発生する。高エネルギーの2次粒子群は、物質中を進行しながらさらに相互作用を起こし、その総粒子数をネズミ算的に増加させていく。この現象をカスケードcascadeという。やがて、元のエネルギーが、平均エネルギーの小さい2次粒子に分割されると、相互作用を起こさなくなって総粒子数は減少していく。 大気の上層部でシャワーとなった二次宇宙線のうち、地表まで降ってくるのは大部分がミュー粒子だが、他にニュートリノや電子なども含まれている。ミュー粒子(ミュオン)や電子のように電気を帯びた粒子が、物質の中を通ると、周りの分子や原子に含まれる電子をはじき飛ばしてイオン化という現象を起こす。 例えば、ヘリウムガスの中に電気を帯びた粒子が突入してくると、粒子の軌跡の周りにあるヘリウム原子の電子が弾き飛ばされる。弾き飛ばされた電子は、プラスの電圧がかかった電極に引き寄せられて加速されていき、この加速された電子がさらに他のヘリウム原子の電子をはじき飛ばしてねずみ算式にたくさんの電子を作り出す「電子のなだれ現象」が起きて放電(スパーク)を発生させる。 電子・γ線・μ(ミュー)粒子の多くは、大気や地上でエネルギーを失って止まる。ニュートリノは、物質と相互作用する時に働く力が弱く、物質と反応する機会が稀ので、地球深く入り通り抜けていく。これを観測するのが「スーパーカミオカデ」で、地中深くに設置されるのは、観測の妨げになるミュー粒子が少ないからである。 地上に存在するいろいろな物質の中で、水素原子はもっとも単純な構造になっている。水素原子は正の電荷を持った陽子1個の周りを電子1個が回っている。この陽子を電子の仲間であるミュー粒子(ミュオン)で置き換えるミュー粒子ビームを使って、ミュー粒子の周りを電子が回るミューオニウムという状態の性質を調べたり、物質の表面の様々な性質を調べられている。 ミューオニウムをさらに大量に発生させ、この測定の精度をさらに高めていき、より効率的に熱エネルギーミューオニウムを発生させることのできる物質の探索や、効率的な超低エネルギーミュー粒子ビーム発生法の研究を経て新しい世代のミュー粒子ビーム源へと発展していく。 電気は今では人の日常生活には欠かせない。磁石は鉄を近づければ引き寄せられる。かつては、電気と磁気は相互関係しない現象と見られていた。しかし、1820年、ハンス・クリスチャン・エルステッドは、電流を流すと、導線の近くに置いてある方位磁石のN極が、以外な方向を指すことに気付いた。エルステッドの研究は更に進み、電流を流すと導線の周りに円形の磁場が作られ、その影響により方位磁石の指す向きが変わることが分かった。この段階で、電気と磁石の相互作用に気付いた。 それから間もなく、アンドレ=マリ・アンペールが「アンペールの右ネジの法則」を発見した。電流を流すと、その方向に対して磁場が右ネジに回る向きに発生する、つまり電気と磁場の関係が極めて密接することが明確になった。アンペールの名は、電流の単位「アンペア」として使われている。 1831年、マイケル・ファラデーが「電磁誘導の法則」を発見した。ファラデーは、電流から磁場が作られるなら、逆に磁気から電流が作られると考えた。ファラデーはまず、鉄のリングの2ヵ所にコイルを巻きつけて片方に電流をながすと、もう片方のコイルにも電流が流れることに気付いた。電流によって起こった磁気の変化によって電流が作られたのである。 更にコイルの中に磁石を出し入れすると電流が流れることも観察された。つまり磁場が変化すると電流が流れることを示していた。アルペールやエルステッドの発見は、電気が磁場を生むものであったが、ファラデーの発見は、磁気の変化が電気を生むことの発見であった。電気と磁場は、互いに密接な相互関係があって、どちらも原因となり、どちらも結果となることが明らかになった。 電磁誘導は、現在のIHヒーターの動作原理となる法則である。IHとは、Induction Heatingの略で、電磁誘導加熱により鍋そのものを発熱させる。つまり、磁場が変化すると鍋などの導体(無数の自由電子を含んだ物質金属など)内に電流が発生するので、IHヒーターの中にあるコイルに交流電流を流すと磁場が発生し、この上に鍋などの金属を置くと電流が発生し、その電気抵抗により発熱する。 1864年、ジェームズ・クラーク・マクスウェルは、これまでに解明された電気と磁場の関係を整理し「マクスウェルの4つ方程式」を著した。この理論により電気と磁場の現象が統一的に理論的に構成され「古典電磁学」が完成した。 マクスウェルの理論は、単にこれまでの実験結果を説明するだけでなく、新たに「光の速度で伝わる電磁波」の存在を予言した。「マクスウェルの4つ方程式」から、電気と磁場が一体となって伝わる波が存在し、理論から導かれるその速さは、既に実験で証明されている「真空中に伝わる光の速度」と同じであることを示した。 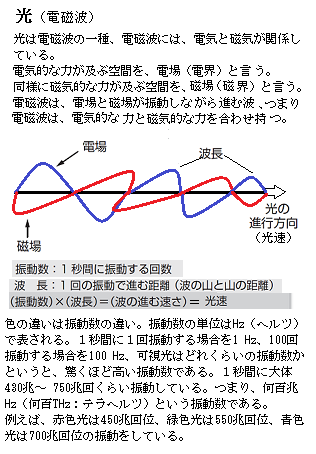 つまりマクスウェルは、光も「電磁波」と呼ばれる波の一種であることを証明した。1888年、電磁波を実験で検出したのは、周波数の単位に名前を残すドイツの物理学者ハインリヒ・ヘルツHeinrich
Rudolf Hertzであった。ハインリヒ・ヘルツは、様々な実験器具を自ら開発し、多くの実験を重ねて電気が起こす波を観察記録し、次々と電磁波の反射・屈折・干渉の動きを解き明かしながら、マックスウェルの理論を完全に検証した。 つまりマクスウェルは、光も「電磁波」と呼ばれる波の一種であることを証明した。1888年、電磁波を実験で検出したのは、周波数の単位に名前を残すドイツの物理学者ハインリヒ・ヘルツHeinrich
Rudolf Hertzであった。ハインリヒ・ヘルツは、様々な実験器具を自ら開発し、多くの実験を重ねて電気が起こす波を観察記録し、次々と電磁波の反射・屈折・干渉の動きを解き明かしながら、マックスウェルの理論を完全に検証した。電磁波は、波長の長い方から電波・赤外線・可視光線・紫外線・X線・γ線などに分類できる。意外にも、その波長によって、他の物質との反応が極端に異なっている。電磁波を人の目で確認できるのは、可視光線だけであるが、目で確認はされないが、スマホやカーナビに伝わる電波は、日常生活に欠かせない。 太陽光線の内、可視光線より波長の長い赤外線は熱さの原因、可視光線で一番長い波長は赤い光である。波長が短くなるにつれ、オレンジ・黄色・緑・青と変わり、一番短い波長が紫の色であり、もっと波長の短い紫外線が日焼けと肌の染みの原因となる。 光の代表的な性質として「光の三法則」があり、「光の直進」「光の反射」「光の屈折」に関する法則、このうち1番目の「光の直進」は、人は日常的に直感している。 厚い雲の隙間から漏れる太陽光は幻想的で神々しい。「薄明光線」「天使のはしご」「レンブラント光線」など、この光景に触発され表現する。宮沢賢治は「告別」という詩の中で「光でできたパイプオルガン」と詠んだ。この時見えるものは、光が直進することで、その径路にある空気中のチリや水蒸気が真っすぐな光の帯となる。光は障害物がなければ真っすぐに進む。これが「光の直進(性)の法則」である。 光に速度があることを最初に実証したのは、デンマークの天文学者レーマーで、1676年の事であった。当時、木星の衛星の1つであるイオが木星の影に隠れる「食」の時間が観測ごとに変化することが知られていた。当時の天文学者は、イオが木星の周りを周回する速度が一定しないからだ、と考えた。 しかしレーマーは、地球も木星も太陽の周囲を回る惑星であるが公転速度に差があり、2つの惑星の間の距離や、地球とイオの間の距離が刻々と変化する、そのため「食」の間の地球とイオンの距離も、近づく場合と遠ざかる場合がある。そのため光の速度が一定していれば、イオから光が地球に到着するまでの間の時間は、距離によって変化する。イオが地球に近づけば、遠い場合より「食の時間」が見かけ上短くなる。 レーマーは、計算を重ね、光の速度を秒速21万kmと見積もった。実際に光の速度は秒速29万9792.458kmであるが、数値の桁は見事にあっている。 ガリレオは、数km離れた2人の男の間の明りで「光の速度」を測ろうとしたが、何度繰り返しても光は一瞬で数kmの間を行き来した。 光の正確な測定は、1849年、フランスの物理学者フィゾーによって行われた。フィゾーは高速で回転する歯車を備えた実験装置で、片道約8km先に反射鏡を置き、歯車を回転させ、光をその隙間を通して往復させた。次に歯車を回転させ、次第に回転速度を速めると、行きに歯車の隙間を通った光が、次にくる歯車に当たって通り抜けなくなる。この時の歯車の回転速度から、光が片道約8km往復するに要する時間が測定でき、光の速度を計算した。 フィゾーは光の速度を、秒速31万5000kmと算出し正解に近づいた。 1862年には、地球の自転を証明する「フーコーの振り子(高い天井から吊るした鉄球が時間の経過とともに回転しながら振動する。地球が自転しているので見かけ上振り子の振動方向が少しずつ回転してずれていく)」で有名なフランスの物理学者フーコーが、フィゾーの実験を改良し精度を高め、秒速29万8600kmと測定した。その後も改良実験が重ねられたが、1973年、レーザーを使った精密な測定により秒速29万9792.458kmと値が導きられた。 しかし現在では、光の速度は実験により求めるのではなく、「定義された値」とされている。速度は移動距離を移動時間で割った値であるため、長さや時間の尺度が本来正確に測定されていなければならない。秒速29万9792.458kmと言う9桁の精度のある値を出すためには、1秒の定義(セシウム原子の出す電磁波の波1回分の時間の91億9263万1770倍)は10桁以上の精度があるが、長さの定義はそこまでには至っていなかった。1983年に「真空中の光の速さは定数c=秒速29万9792.458kmである」と定義された。これを「1m」の長さの基準とし、「光が2億9979万2458分の1秒間に進む距離」を「1m」とした。  透明な大気の中には、窒素分子や酸素分子など様々な分子が存在している。これらの分子は、太陽光を僅かに散乱させる。紫色光や青色光のような波長の短い光の方が、波長が長い赤色光より多く散乱する。光を水面の波にたとえれば、波長の長い波にとって、小さな分子は水面に浮かぶ木の葉のようなもの、波は木の葉に当たっても殆ど影響されずに通り過ぎる。波長の短い波にとっては、分子は大きな船体のようなもの、波は船体に当たって大いに散乱する。一部は宇宙空間に戻っていく。 透明な大気の中には、窒素分子や酸素分子など様々な分子が存在している。これらの分子は、太陽光を僅かに散乱させる。紫色光や青色光のような波長の短い光の方が、波長が長い赤色光より多く散乱する。光を水面の波にたとえれば、波長の長い波にとって、小さな分子は水面に浮かぶ木の葉のようなもの、波は木の葉に当たっても殆ど影響されずに通り過ぎる。波長の短い波にとっては、分子は大きな船体のようなもの、波は船体に当たって大いに散乱する。一部は宇宙空間に戻っていく。「ものが見える」と言うことは、ものに当たって散乱された光が目に飛び込んでくるからである。人が日中、明るい空を見上げると、太陽の紫色光や青色光が、大空に強く散乱されて四方八方から人の目に飛び込んでくる。赤色光は、散乱されにくいので人の目に直接入射してくるだけであるため認識できない。また人の目には、紫色光よりも青色光に対する感度の方が高い。そのため日中の青天を、空の色と思う。 夕陽は赤い、夕焼けの空は赤っぽく見える。散乱されにくい赤色光は長い距離を飛んでも、ある程度は残っている。その残った赤色光だけが空気中の分子や塵、水蒸気などにより散乱されため夕焼けの空は赤く見える。 空気中の分子の大きさは、光の波長の1,000分1程度、光が分子のような非常に小さな物質に当たる時の散乱を「レイリー散乱」と呼ぶ。「レイリー散乱」での散乱光の強さは波長の4乗に反比例する。赤色光の波長は、青色光の波長より約2倍なので、散乱は約1/16と少ない。 虹を作る水滴は、光の波長よりずっと大きい粒子であるため、散乱光の強さは、どの光の波長でもほぼ変わらない。こうした散乱を「非選択的散乱」と呼ぶ。 また海が青く見えるのは、青天の空を映しているからではなく、光の散乱の効果よりも、水が赤色の光を吸収する方がかなり大きいからである。 無色透明な水の中に、太陽の光を10m位通すと、赤色の光は殆ど吸収され、そのため全体的に青っぽい色になる。その残った青色光が水中で散乱するため「海の色は青い」と見られる。 水分子H2Oは酸素原子1個と水素原子2個からできている。その3つの原子の間で絶えず振動が起こり、その振動数は約1秒間に100兆回の振動である。この振動数に一致した光がやってくると、水分子は光を吸収する。 赤外線は、一般に0.75~200µmの波長範囲を持つ電磁波の一種で、可視光より長い波長を持つ。人は、目の中の網膜で光を検出して脳に伝える。その際、この高い振動数を、そのまま直接振動として感じているわけではなく、振動数に応じた刺激を脳が学習して、振動数の違いを色の違いとして認識している。例えば、赤色光は450兆回位、緑色光は550兆回位、青色光は700兆回位の振動をしている。 可視光の色を、振動数の低い順に並べると、赤・橙・黄・緑・青・藍・紫となる。 約1秒間に100兆回振動する光は、波長で言うと約3㎛(マイクロメートル;30-6m)の赤外線になる。そのため水は3㎛付近の赤外線は全く通さない。また振動による吸収は、その振動数の整数倍の振動数を持つ光も吸収する。波長で言うと「整数分の1」の波長の光を吸収する。水分子の場合、2分の1の1.5㎛付近や、1分3付近の1㎛などで吸収が起きる。これを「2次の吸収」「3次の吸収」と呼ぶ。 可視光では、赤色光が「4次や5次の吸収」に引っかかる。緑色や青色の光も、もっと高次の吸収を受けるが、次数が高くなるにつれ吸収力は急激に弱くなる。青色光は赤色光と比べて1,000分1ほどしか吸収されない。そのため赤色の吸収がより大きくなるため、青色の海に見える。 海の色は青色だけではない、海水に含まれ塩分やその他の成分、海水中のプランクトンの量や海底の地質の違いなど、様々な影響を受ける。 沖縄の海だと1mlの海水に10個位しか植物プランクトンは含まれていない。沖縄の海は栄養分や植物プランクトンの少ない場所なので、青だけがどんどん濃くなり藍色に見える。一方、沖縄の海の浅瀬では、砕けた珊瑚や有孔虫の死骸の堆積などによる白砂の反射でエメナルドグリーンになる。 東京湾だと1mlの海水に1,000~1万個くらいの植物プランクトンが含まれている。富栄養化eutrophicationや植物プランクトンの多い場所では、青い色に黄色や緑色が混ざって黒っぽく見える。 光より波長の短いのがレントゲン撮影に使われるX線、そのX線より更に波長の短いのがγ線である。これらすべてが電磁波で、信じ難いことに同じ仲間である。今では、あらゆ る波長域の電磁波が、様々な技術に活用され日常生活には欠かせない存在となっている。 19世紀の終わり頃までは、ニュートンの運動の法則と万有引力の法則、重ねてマクスウェルの「電磁気の法則」で、自然界のあらゆる現象が説明できると考えられていた。 量子とは、主に原子より小さい世界で、粒子性(物質の性質)と波動性(状態の性質)を併せ持つ、とても小さな物質やエネルギーの単位であるため、 普通の物質と区別するため、「量子」(quantum) と呼ぶ。物質を形作っている原子や原子核、電子や陽子と中間子、光子や陽電子、ニュートリノやクォーク、レプトンleptonに分類される電子などといった素粒子も量子に含まれる。電子は「量子」の代表格であるが、量子は、特定の粒子の名前ではない。「万物の根源」と言うほどの意味であり、原子の内側にあるものは、「部品」ではなくて、「量子」である。 20世紀の初めになると、原子は今でも量子であるが、素粒子と言わなくなる。さらに小さな、 もっと基本的ものから構成されていることが明らかになったためである。 量子とは、単に「小さい」だけではなくて、「光量子」や「エネルギー量子」といった単語が量子力学を学ぶ際に使われるが、それはそれぞれ「光の最小単位」、「エネルギーの最小単位」を意味する。つまり、量子とは「一定量を持った物理量の最小基準」であり、原子より大きい世界に存在する「物質」とは振る舞いが異なる。電子は「量子」なので、電子1個だと水素、2個ならヘリウムという、物質の世界では起こらないような現象が生じる。その「量子」を研究するのが「量子力学」である。 量子の世界は、原子といったナノサイズ(1メートルの10億分の1)、あるいはそれよりも極めて小さな世界で、通常、日常的に観察されるニュートン力学や電磁気学などの物理法則が通用せず、「量子力学」というとても不思議な法則に従っている。実際の原子半径は、約10-10m=1Å(オングストローム)= 0.1ナノメートル(nm)、即ち100億分の1mである。 素粒子や原子と原子以下の粒子に関連するエネルギーには、電子ボルトelectron Voltと言う非常に小さなエネルギーの単位「eV」を使う。1電子ボルトとは「1ボルトの電池で1個の電子を回路で加速した時に、電子が獲得するエネルギー」である。生物学で扱うデリケートで微弱な化学結合では、0.1 eV程度のより小さなエネルギーで起こっている。 アセチレン(分子式は C2H2)は、酸素と混合し、完全燃焼させた場合の炎の温度は3,330 ℃にも及ぶため、その燃焼熱を目的として金属加工工場などで多く使われる。構造式は HC≡CHの炭素間で三重結合によるもので、その時の爆発で解放されるエネルギーは、アセチレン分子1個あたり10 eVほどであり、非常に大きな爆発音が起こる。この爆発音は、化学エネルギーが運動エネルギーとして開放されたと時に生じる衝撃波である。 アインシュタインの有名な式E=mc2により、静止している粒子はすべて、慣性質量mに等価なエネルギーEを持つことになる。そのため素粒子の質量も、エネルギーの単位を使って定量的に表せられる。 例えば陽子の質量1.67262158× 10-27kgは、変換式1GeV/c2=1.783×10-27kgを使えば電子ボルトで表すことができる。結果、陽子の質量は0.938GeV/c2(1 GeVギガ電子ボトル=10億eV)となる。 なお、重力質量と慣性質量は「はたして同等なのか?」という議論が古くからあったが、今日では両者は一致すると考えられている。アインシュタインも両者は区別できないとして、一般相対性理論を展開している。 20世紀の科学に起こった2つの偉大な革新的な成果が、量子論とアインシュタインの相対性理論であった。 量子論が教えてくれるのが、「自然界のあらゆるものを形成する量子は、粒子でありながら波でもある」と言う。それまでの物理学では全く合い入れない「衝撃的で不可解な量子論」に依らなければ、粒子の世界を垣間見ることもできないのである。粒子は量子力学的な波と理解されている。その波は、ある時間とある場所で、点状の粒子として検出される。それは、アインシュタインの一見単純でありながら、その式を形成する要素の中身が膨大でありすぎるため、E=mc2 の理解は、その後の実験データーが積み重なることにより実証されて、漸く受け入れられた。その式により生物学上のクエン酸回路の本質も理解されている。 その粒子の波の速度が光の速度に近づくと、アインシュタインの相対性理論が働いてくる。 光速c(ラテン語で速さを意味する celeritas にも由来するものである)=波長λ(ラムダ)×振動数ν(ニユー) (完全な真空中では、「光子」は、秒速29万9792km。特殊相対性理論の「光速度不変の原理」では「光の速度 c は、光源の運動の状態に関わらず常に一定値である」) E=hν=h×c/λ (c=λ×ν) (光子のエネルギー E (energy) は振動数νに比例し、波長λに反比例する。その比例定数をプランク定数 h といい、プランク定数 h = 6.63×10-34 J/s) どんな粒子でも、エネルギーを与えれば与えるほど、振動数が増え、その量子的な波長が短くなる。光の速度に近づくほどの運動するエネルギーを倍増させれば、その素粒子の量子的な波長は半分になる。つまり、素粒子に大量のエネルギーを与えれば与えるほど、量子的な波長は短くなるため、素粒子をどんどん加速させ高エネルギー状態にすれば、どんどん微細な道具に仕立てることができるようになる。これが現代の大掛かりな顕微鏡や粒子加速器の原理的な基礎になる。そのため素粒子を探索の道具にするために、素粒子に大きなエネルギーを与える必要があるため、その装置は一段と巨大化する。 可視光の波長は、大きなエネルギーを持つ青い光は、0.00004cm(4×10-5cm)、光子1個につき約3eV、小さなエネルギーの赤い光では、0.00007cm(7×10-5cm)、光子1個につき約2eVほど、従って、可視光を構成する光子の量子波長は、この範囲内で、そのエネルギーは約2~3eVとなる。そのため精密な光学顕微鏡であっても、可視光の量子的波長より大きいもの、0.0001cm(10-4cm)よりも大きな物体しか調べられない。例えば、ウイルスや生体細胞内の小器官 やDNAなどは観察できない。 目次へ |
|||||||||
| 4)電子顕微鏡 考古学でいうガラスの起源は、5,000年前頃のメソポタミアに始まる。完全なガラス製品の出土は、4,500年前頃のメソポタミアとその周辺地域からで、丸玉・管玉・トンボ玉(アンティークのモザイク模様)のような小さな装飾品が鋳造されている。最古のガラス遺跡は、北メソポタミアからアナトリア半島(トルコ)、シリア、パレスチナにかけてのBC1,600~1500年代の地層ら発見されている。この頃には、装飾や手芸などに用いられる穴の開いたビーズが、交易品としても用いられ始め、インダス川流域で作られたエッヂッドカーネリアンビーズ(カーネリアンと言う赤い天然石に草木の汁で模様を描く)のネックレスは、インダス文明の最大の工芸品として、エジプトやメソポタミアにも海運(草船)を利用して輸出されていた。エジプトやメソポタミヤの王家の墓など、各地で発見されている。 BC1,000年頃になるとアレキサンドリアやフェニキュアなどでガラス玉作りは盛んになる。古代エジプト史上最大となる版図を築いたエジプトのトトメス3世(BC1490年頃~1436年頃)が、ガラス職人を捕虜として連れ帰り、エジプトで美しいガラス容器が作られるようになった。古代エジプトにはガラスの原料になる天然の炭酸ナトリウム(ソーダ)が豊富にあった。 「ローマガラス」とは、BC27年からローマ帝国が東西分裂するAD395年までの、約400年の間に作られた、とされている。帝政が始まる頃、シリアやエジプトといった主要な炭酸ナトリウムの産地が、ローマ帝国の領土になった,が関係しているようだ。 11世紀以降、アラビア化学が発展し、拡大鏡としての利用が始まった。中世最大の物理学者イブン・アル・ハイサム(ラテン名;アルハーゼン)は、バスラ(現;イラク南部の油田地帯)で生まれカイロで活躍し、その地で没した。その主著『光学の書』(全7巻)の中で、眼球の仕組みは、物が放つ光を受けて眼の中に像が結ばれると考え、物が見える現象を解明した最初の科学者と言える。鏡やレンズについても実験装置を作って、光の屈折や反射の原理をいくつも測定し解説した。 『光学の書』は、13世紀にヨーロッパに伝わり、その本がラテン語に翻訳され、『光学宝典』と呼ばれ、多くの修道士に読まれるようになり、ヨーロッパ各地で修道士によるレンズの製作が盛んになった。当時は、書物の上に直接置くルーペloupe(リーディングストーン)として使用されていた。 14世紀中頃の、両眼の眼鏡を掛けた修道士の絵が残されている。16世紀に入るとヨーロッパ各地に眼鏡職人が現れて、そうした人々の中から望遠鏡や顕微鏡が発明されてくる。 現代の各種観察手段の「肉眼」「光学顕微鏡」「電子顕微鏡」などの分解能とは、物と物を分離して観察できる最短の距離を指す。ヒトの目の分解能はおおよそ0.1 mm、それ以上小さい物の観察には、「光学顕微鏡」や「電子顕微鏡」が使用される。光学顕微鏡では、観察したい試料に光を当てて、像を拡大して観察するのに対して、電子顕微鏡では光の代りに電子線を試料に当てて、像を拡大して観察する。電子顕微鏡は物理や化学、生物から医学部門と幅広い分野で活用されている。 レンズを複数くみあわせた現在のような顕微鏡が発達するのは、19世紀になってからである。光学顕微鏡は、試料に可視光線や近傍の波長域の光を当てて、像を拡大して観察する。そのため色がついて見える。19世紀末には、光学顕微鏡のほぼ限界まで性能が向上し、飛躍的な発展を遂げた。一方、光学顕微鏡の解像度、分解能は、光を使う以上、原理上の限界があった。野口英世は黄熱病の原因を細菌と考えていたが、実際にはウイルスで、可視光の光子では、対象が0.00001cm(10-5cm)より小さいと、鮮明な画像は得られやない。ウイルスばかりか、DNAの観察もできない。 光学顕微鏡では見られない素粒子の世界を見るには、可視光の代わりにエネルギーの高い粒子をぶつける必要がある。電子顕微鏡は電子線を用いて測定対象物の拡大像を得ることがでる。電子線は電磁波として見た場合、非常に波長の短い波なので、光学顕微鏡などよりはるかに高い倍率での形態観察が可能となる。ただ電子を当てるため白黒に見える。 走査電子顕微鏡Scanning Electron Microscope (SEM)においては、電子線を用いるため、焦点深度が非常に深い位置まで達するため立体的な形態観察が可能となる。原子よりも小さな粒子でも、数十倍~数万倍以上の広い倍率で観察が可能となる。電子顕微鏡の光学顕微鏡に対するメリットは、倍率はもとより分解能にある。 電子も他のどんな粒子と同様、量子的な波長がある。その電子を加速するために、電子顕微鏡には、小型加速器が組み込まれている。電子を加速して、可視光の光子の1万倍の20,000eV程度の運動エネルギーを与えることができる。旧式テレビのブラウン管でも、この程度のエネルギーが電子に与えられていた。この電子のエネルギーでも、加速された電子の量子的波長は、約0.000000001cm(10-9cm)となり、可視光の波長よりかなり短くなっている。 走査電子顕微鏡は、真空中で細く絞った電子線で試料表面を走査し、その時試料表面から出てくる二次電子を検出することにより、画像化させたものを、モニタ-上に試料表面の拡大像を表示する電子顕微鏡である。 真空中で電子線を試料に照射すると、二次電子などが試料から放出される。二次電子は、一次電子の試料内での非弾性散乱(入射電子が試料を構成する原子に衝突するとき、電子や結晶格子と相互作用をしてそのエネルギーの一部失って速度が遅くなり散乱される電子)によって、試料を構成する原子から励起された電子で、入射電子による二次電子の励起は、試料の深さとは無関係に起こっているが、二次電子のエネルギーは小さく試料内で散乱されるため、試料の表面に到達できるのは、試料の浅い部分で励起されたものだけである。それを検出して得られた二次電子像は、試料の微細な凹凸を反映している。 そのため、二次電子は、試料表面の形状により発生量が違うため、結果的に試料表面の凹凸情報を反映した像による3D解析ができる。また、二次電子は材料によっても発生効率が異なる。ただ、通常は試料形状の方がコントラストには大きく寄与する。二次電子以外に、試料からは反射電子や特性X線なども放出される。 そのため、走査電子顕微鏡には、X線検出器を装着して元素分析を行う事も可能で、走査電子顕微鏡は試料形状の観察だけでなく、その試料にどんな元素がどの程度含まれているかを調べるX線分析装置としても活用されている。 電子顕微鏡なら原子より小さな粒子でも、電子線を使って調べることができる。電子線を発生させる電子銃の性質から、数キロボルトから数百キロボルト、時にはそれ以上の高電圧が必要である。電子顕微鏡では安定した電子線を作るために高性能な電源や、顕微鏡内を真空に保つ機構が必要で、光学顕微鏡と比較すれば大掛かりな構造となる。したがって高電圧の発生装置や真空ポンプ、顕微鏡自体は耐圧構造でなければならないなど、装置が大がかりになりがちで専用の部屋が必要となる。 走査型電子顕微鏡に限っては、卓上に置けるタイプなど小型製品も増えてきている。卓上走査型電子顕微鏡は、高画質のSEM画像観察と高度な画像解析に優れ、光学顕微鏡で撮影した試料全体の画像を見ながら、SEMでの観察位置を確認することができる。 透過型電子顕微鏡Transmission Electron Microscope(TEM )は、試料に電子線を当てて、それを透過してきた電子を拡大して観察する電子顕微鏡で、試料の構造や構成成分の違いにより、透過する電子の密度が変わる。数百倍~数百万倍の広い倍率をカバーする試料の投影拡大像を得ることのできる装置である。この試料を透かして観察するため、「透過電子顕微鏡」と呼ばれいる。 対象物を出来るだけ薄く切ったり、電子を透過する薄膜に対象物を塗ったりして観測する。透過電子顕微鏡の電子線を加速させる電圧を「加速電圧」と言う。その加速電圧が300kV の時の電子線の波長は0.00197nm(0.000000000197=1.97×10-10cm)になる。 光学顕微鏡で使用される可視光線の波長は400~800nm(0.00004cm~0.00008cm=8.0×10-5cm)であるから、電子線の波長の方が格段に短い。透過電子顕微鏡の分解能は、加速電圧を高め電子線の波長を短くすればするほど、透過する電子が増えるため、そのデータ解析の精度はより向上する。 目次へ |
|||||||||
| 5)光の波長とエネルギー 量子という考え方は光の研究から生まれた。量子と言う考え方を最初に物理学にも持ち込んだのは、1858年、ドイツのキールに生まれたマックス・プランクMax Planckである。1918年には、ノーベル賞を受賞し、1947年没した。翌1948年に設立されたマックス・プランク研究所は、これまでに17人のノーベル賞受賞者を輩出している。自然科学や人文・社会科学など、幅広い分野の研究に取り組むドイツ随一の学術研究機関であり、各分野の世界トップレベルの研究者たちが集まっている。 プランクの「エネルギー量子仮説」は、光のエネルギーは、ある決まった「とびとびの不連続の値」しか取らないと言う。現在では、ある一定の波長を持つ光のエネルギーは、連続ではなく、「とびとびの値」をとる「かたまりのようなもの」であることが分かっている。プランクはさらに追求した結果、一つの仮説(量子仮説)に達する。やがて、光子だけでなく、物理量がとびとびの不連続の値を取るものを総称して「量子」と呼ぶようになる。 当時、プランクは、「熱した物質の温度とその物質が出す光の色」の関係を説明するのに「光のエネルギーは小さな固まり」と考えると分かりやすいことに気付いた。 黒体black bodyという言葉を聞いたことがあるだろうか。物体が例えば赤く見えるのは、それを光で照らした時に赤以外の波長の光が吸収され、赤の光だけが反射されるからである。黒い物体は、あらゆる波長の光を吸収する物体である。この様な物体を黒体という。一方、この黒体を高い温度に熱すると、黒体からは色々な波長の光が放出される。 例えば、溶鉱炉の中の鉄が赤く見えたり、裸電球の色が黄色く見えたり、また、太陽からの光が白く輝いて見える。そのことから、溶鉱炉の鉄やタングステン電球のフィラメント は黒体に近い存在と考えられ、その色の違いは黒体の温度の違いを表している、とも言える。 黒体を熱すると、温度が上がるにつれ、最初は赤かったのが黄色くなり、さらに白ぽくなる。これは温度が上がるにつれ、ヒトの目に見える光の色、言わば、その物体が放出している「一番強い光の色」が赤から黄色にかわる、つまり波長が次第に短くなるためである。 太陽の表面の温度は、約6,000度、太陽表面で一番温度が低いのは、約4,400度の黒点、中心部は約1,500万度と見られている。太陽が放出する様々な波長の光を含んだ光を白色光と言う。それは、単に人の目に白く映るからである。この様々な波長を含んだ白色光を、ガラスでできた三角形のプリズムに通すと屈折によって様々な色に分離され、波長の比較的長い赤はあまり曲げられず、波長の比較的短い青は大きく曲げられる。これを光の分散と呼ぶ。つまり、ヒトは、太陽光から放出される波長の異なる色のスペクタルspectrumをすべて同時に見ると、純粋な白色と認識する。 光は、波としての性質(電磁波)を持つ一方で、つぶつぶの粒子のような性質も示す。そのため、波としての性質を表して電磁波 electromagnetic waveと呼ぶ一方、 粒子として振舞う光を光子 photonと呼ぶ。 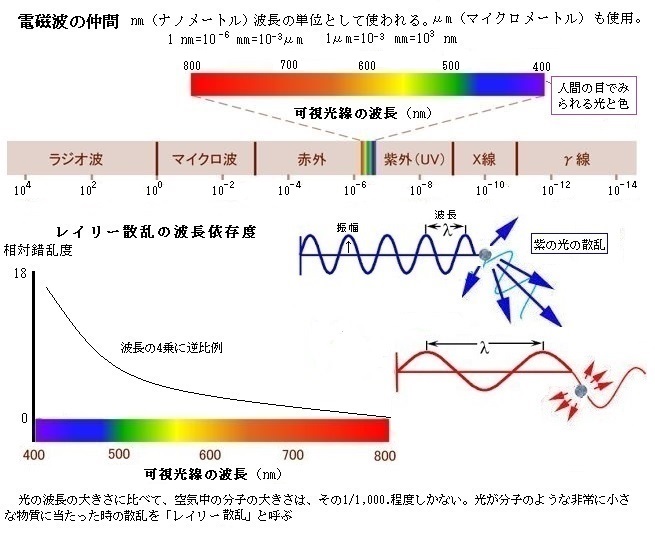 光とその仲間を総称して「電磁波」と言う。光とその仲間の正体は、空間を伝わる電気的な波である。電気的な波が起こると、必ず磁気的な波も同時に起こるので、電磁波と呼ばれている。光とその仲間たちとの違いは、波長の違いである。波長とは、波の一番高い場所から次の山までの長さである。電磁波の中で、波長が最も長いのが電波である。それから赤外線・光(可視光)・紫外線・X線・ガンマ線の順に波長が短くなる。 光とその仲間を総称して「電磁波」と言う。光とその仲間の正体は、空間を伝わる電気的な波である。電気的な波が起こると、必ず磁気的な波も同時に起こるので、電磁波と呼ばれている。光とその仲間たちとの違いは、波長の違いである。波長とは、波の一番高い場所から次の山までの長さである。電磁波の中で、波長が最も長いのが電波である。それから赤外線・光(可視光)・紫外線・X線・ガンマ線の順に波長が短くなる。太陽の光は、様々な波長の光の混合物で、赤い光が最も長く(約700nm)、最も波長が短いのが紫の光(約400nm)である。光の波長の大きさに比べて、空気中の分子の大きさは、その1/1,000.程度しかない。光が分子のような非常に小さな物質に当たった時の散乱を「レイリー散乱Rayleigh scattering」と呼ぶ。 光が持つ様々な性質や、光が関わる様々な現象は、「光には波としての性質がある」ことによる。しかしながら、光は、同時に粒子としての性質を持つ。その光を粒子の集まりとしてとらえた時、その粒子を「光子photon」と呼ぶ。 真空中を伝わる光(電磁波)の速さは常に一定で、 その速さを光速 c と呼ぶ。 つまり光(電磁波)の波長と振動数の積は常に一定なので、波長と振動数はお互いに反比例する。 光速c(celeritas;秒速)=波長λ(ラムダ)×振動数ν(ニユー) 光子のエネルギーはその振動数によって決まる。波長が長いほど、振動数は低くなりエネルギーも低くなる。光子のエネルギー E (energy) は振動数νに比例し、波長λに反比例する。その比例定数をプランク定数 h といい、プランク定数 h = 6.63×10-34 J/s E=hν=h×c/λ (c=λ×ν) 光を「波」と捉えるだけでは、そのエネルギーは遠ざかるほどに弱まってしまう。光を光子と言う粒と考えれば、光子1個のエネルギーは、光の振動数に比例し波長と反比例して決まるため、振動数が多きくなるほど、光子1個のエネルギーも大きくなる。 光は電磁波の一種であり、波としての性質を持つことは分かっていたが、20世紀になると、波としての性質だけでは説明がつかない現象が発見された。光は波と粒子と言う二重の性質を持っているとしか言いようのない「光の二重性」があり、それが普通の物質と区別するため「量子」と言う新たな概念を生み出した。つまり「量子化学」は、「光の二重性」の研究を端緒にする。 従来の物理の概念では、波と粒子が1つのものの中で両立することはありえないのである。1つのものが波であれば、それが粒子となりえない。その逆も然りである。 ところが、金属に紫外線のような光を当てると、金属の表面から電子が飛び出す。これは「光電効果photoelectric effect)」と呼ばれる現象で19世紀の終わりごろから知られていた。 金属の中の電子は原子核の引力で束縛されてて、普通は外へ出てこられない。それが外部から光を当てると、金属の表面から電子が飛び出す。様々な実験をしてみると、金属から電子が飛び出すのは、紫外線のような波長の短い光だけで、赤色のようなの波長の長い光をいくら流しても電子は飛び出さない。逆に波長の短い光なら弱い光でも電子は飛び出す。 この現象を説明するために、アインシュタインは光を粒子と考えた。1905年、光を波として考えるだけでは説明できなかった「光電効果」について、「光は波長に応じたエネルギーを持つ粒である」と考えることで、これを説明する。光はエネルギーの固まりとして考えを進めるのだが、そのエネルギーを持った最小単位としての粒子である光子の存在を考えた。1個の光の粒子を光子photonと呼ぶ。青色光の光子は電子を飛び出させることのできる高いエネルギーを持った光の粒子、赤色光の光はこれができない低いエネルギーの光の粒子であると考えた。アインシュタインは、光子は1秒あたりの振動数vに比例したエネルギーを持つと仮定した。波長λとは、反比例をする。 E=hν=h×c/λ (c=λ×ν) 青色光(λ=400 nm)の光子1 モルmolは約300 kJ のエネルギーを持ち、赤色光の光子1 モルのエネルギーは175 kJ に相当する。つまり、振動数が高い光子ほど、電子にあたると電子を素速く動かすことができる大きなエネルギーを持っている(基準に用いられている「質量数12の炭素12C」が12gあるとき、そこに含まれる炭素原子の個数を数えると6.02×1023個となります。この個数を、1molと定義し「物質量」の定義とする)。 金属から電子が飛び出すに必要なエネルギーは、その金属によって異なるが、それに必要な最小エネルギーが決まっている。それも光の粒子性によって理論的な説明が成り立つ。 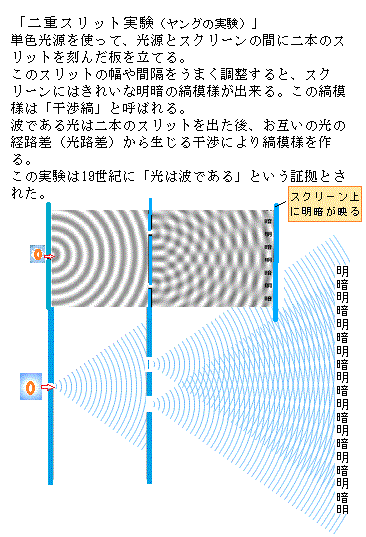 「光は、波でもあり粒でもある」このための実験が行われた。1805年ころイギリスの物理学者トーマス・ヤングThomas Youngの干渉実験(ダブルスリットの干渉実験)において、光を極端に弱くして「光が一粒しかない状態」でも、干渉縞が現れるかどうかを調べるもので、光の一粒一粒を検出する技術を使って行われた。 「光は、波でもあり粒でもある」このための実験が行われた。1805年ころイギリスの物理学者トーマス・ヤングThomas Youngの干渉実験(ダブルスリットの干渉実験)において、光を極端に弱くして「光が一粒しかない状態」でも、干渉縞が現れるかどうかを調べるもので、光の一粒一粒を検出する技術を使って行われた。第一段階目の単スリット(光や電子の流れを絞る細いすき間;細隙)で波を1つに絞り、その単スリットから等距離の位置にある2つのスリットに波を通す。すると実質的に、この第二段階目の複スリットからは位相(周期的な運動をするものが、1周期分の中のどの位置にあるかを示す)の揃った2つの波が発射されることになる。このように工夫されたスリットを用いて、光の干渉現象を観察する実験のことを「ヤングの干渉実験Young's interference experiment」と言う。 光波と光波がぶつかって、強め合ったか弱めあったかは、スクリーンで確認できる。隣同士の光波の山が重なり合えば、その箇所は明るくなり、光波の山と谷が打ち消し合う箇所は暗くなる。スクリーン上にはそれらが交互に現れ、縞模様ができ、これを干渉縞(かんしょうじま)と言う。この実験により、光が干渉することが示され、光の波動説が示される。 アインシュタインは、1,921年にノーベル物理学賞を受賞した。その理由は、「光量子仮説に基づく光電効果の理論的解明」であった。その当時でも、相対性理論は難しすぎて、審査委員会が理解できなかったようだ。 こうして、アインシュタインの光量子説をもとに、その後の量子力学的な考察や実験によって光子の二重性は確認されている。そして現在では光子は、光の吸収や放出といった光と物質の相互作用が関連する分野では粒子として、光の伝播に関わる領域では波として扱われている。光子は「宇宙を構成する4つの力」のうち「電磁気力」を伝える働きをしていることがわかっている。その他の3つは「重力」「強い力」「弱い力」である。 目次へ |
|||||||||
| 6)光速度不変の原理 光の速度は、真空中では秒速30万km(正確には、29万9792.458km)である。現在の物理学では、この光の速度は一定で、これより速く進むものは存在しないとされている。しかも、アメリカの物理学者マイケルソンとモリーの1,887年の実験により、光については「速度の加法定理」は成り立たず、つまり「真空中において、光の速度は光源の速度に依らず一定である」ことが分かった。 ロケットが光速度(c)に近い速度0.99cで飛んでいるときに、ロケットから飛び出した光があったとしたら、その光の速度は c + 0.99c = 1.99c ではない。 「真空中において、光の速度は光源の速度に依らず一定である」 特殊相対論の仮定では、答えは c である。 この難しい問題に答えを出したのが、アインシュタインで、マイケルソンとモリーの実験結果から、「どのような速度で動いている観測者から見ても、光の速度は一定である」とする「光速度不変の原理」を打ち立てた。この原理を発展させ、1,905年に「相対性理論」として発表された。この理論は、その後の様々な実験により、正しいことが確認され、20世紀の物理学の礎となった。 w =( u + v )/( 1 + u v/ c2) この式には、重要な意味が秘められている。 光は秒速30万km(c)で進む、地球の公転速度が秒速30km(v)である時に、人が公転方向に普通に歩く速さは秒速1.25m(u)、人の単純な速度の加算では、w (加算速度)= u + v となる。vとuの値が、光速度 c に対して余りにも小さいため、この式からu v/ c2 は、1億分の1となるため、光の進む速度は、地球の公転速度の影響を受けることはない。つまり、光については、速度の加法定理は成り立たない。光速度cの二乗と比べて、現実に余りにも小さな速度u、vをいろいろ代入して計算して試して欲しい。 また、「真空中において、光の速度は光源の速度に依らず一定である」ならば、永久に減速しないため、光子の射程距離は無限大となる。そのため、視物質の分子中の電子に、働きかけるに十分なエネルギーを持った光子が目に入れば、その星からの光が見える。光が関わる現象の多くは、光が「波であり、粒でもある」二面性に起因する。 約432光年離れた北極星を見た時、その1,587年の日本では、豊臣秀吉は、惣無事令に従わなかったことを理由に九州の戦国大名を討伐している。 青天の空や、早朝や夕方の空が赤く見えるのは、太陽光のスペクトルspectrumが空気層を通る距離と関係する。太陽が昇る時と沈む時、太陽の位置は、ヒトの真上から離れて遠く横に移動する。そのため、太陽光の空気層を通る距離は、真上に比べて横の方が、はるかに距離が長くなる。いままで細かいチリの間をすり抜けてきた波長の長く振動数の低い赤い光も、細かい酸素や窒素の分子にぶつかり散らばる頻度が格段に高くなる。 つまり、光の波長が短く高エネルギーほど、空気分子が多くの光を散乱させる。そのため波長の短い青い光は、空気中を通る際にどんどん散乱してヒトの目に入ってくる。 一方、波長の長い赤い光は、あまり散乱しないで、小さな大気の粒子の脇を通過して行く。夕方、太陽の光が地平線近くから地面を照らす時は空気を通過する距離が長いので、青い光は殆どなくなり赤い光だけが残っているので、夕日が赤く見える。長い波長の赤い光は、散乱されにくく、厚い空気の層を通って遠くまで伝わり、赤い光だけが散らばった空が目に映るので、人には夕焼けの空となって見えるようになる。 真空中での光速はその値が決まっている。しかし、均質な媒質中では基本的に直進する性質を持つが、媒質が均一でない場合は進行方向が変化することがある。一般に、光の行く手に存在する微粒子などによって、光の進行方向が不規則に変化する現象を「光の散乱」と呼ぶ。 物質に侵入した光は波長によって光速の値が違ってくる。可視光線が物質に侵入すると、通常、波長が短い(振動数が大きい)光の方が、光速が遅くなる。その理由は、ガラスなどを構成する原子では、赤色波より紫色波の固有振動数方が、ガラス構成原子の固有振動数に近く、波を吸収してから再放出するまでに時間が掛かるからである。光速が遅いということは、絶対屈折率が大きいということであり、波長によって速さが違うということは、波長によって絶対屈 折率が違う、ということになる。 目次へ |
|||||||||
| 7)光の散乱と励起 青天の空が青いのも、光のスペクトルが、波長によって色が異なるからで、太陽光は、地球の大気圏に入ると、空気中の大気を構成する細かい酸素や窒素の分子にぶつかり、光の向きが変わるからである。可視光線の波長は400~800nm(1 nm = 1×10-9m;10億分の1m)、波長によって異なる色感覚を与え、紫(380-430 nm)、青(430-490 nm)、緑(490-550 nm)、黄(550-590 nm)、橙(590-640 nm)、赤(640-770 nm)として認識される。空気分子の大きさは、酸素0.364nm、窒素が0.378nm程度。波長の短いもの、つまり赤よりも青のスペクトルの方が、波長が短いため振動数が大きい。 光や電波のような電磁波が、その波長と同程度以下の大きさの粒子に当たったとき、粒子から2次的な電磁波が発生して周囲に広がる現象を散乱という。特に、光が空気分子に当たった時のように、電磁波の波長に比べて粒子 が十分小さい場合の散乱のことを、空の青さを説明する理論を研究したレイリー卿の名前をつけてレイリー散乱と呼ぶ。このレイリー散乱が赤い夕日や青空を作り出している。  しかし、青い光が赤い光よりもなぜ散乱するのかは、波長ではなく、その振動数の問題である。酸素や窒素分子の共鳴振動数は、200nm付近の紫外線部にある。太陽光が空気分子に当たると、共鳴振動数付近の光が共振(基底状態→励起状態)し、すぐに開放(励起状態→基底状態)される。開放される際には四方八方に分散される。これが散乱光である。そのため進行方向の光が弱くなる。 しかし、青い光が赤い光よりもなぜ散乱するのかは、波長ではなく、その振動数の問題である。酸素や窒素分子の共鳴振動数は、200nm付近の紫外線部にある。太陽光が空気分子に当たると、共鳴振動数付近の光が共振(基底状態→励起状態)し、すぐに開放(励起状態→基底状態)される。開放される際には四方八方に分散される。これが散乱光である。そのため進行方向の光が弱くなる。 固有振動数とは、物体や構造物が持つ固有の共振周波数のことであるが、それぞれ振動しやすい固有の振動数があり、この周波数では、一旦外力が生じると、外部から力を加えなくても自分自身だけで振動し続ける。この固有振動としtれ。形状・拘束位置・材料のヤング率(縦弾性係数、建造物に使われている材料は、力を加えると変形し取り除くと元の形に戻る弾性体である。そのため、外力が加われば変形する。その外力と変形量の関係を表す係数である)や密度によって異なる。固有振動に合えば、弱い力であっても、最終的には大きな振動が。 では共鳴振動数以外の光はどうかというと、吸収・放出過程の時間が非常に短いため、振動数に幅がでてくる。そのため、青色の光の方が、赤色の光より10倍近くも強い強度で散乱している。したがって、青天の散乱光の中には、青色の光は、赤色の光の10倍近くも含まれ、このため、空は青く見えるのである。 もう1つの空が青く見える要因の一つに、空気分子が乱雑に配置されているからである。もし結晶のように原子が規則正しく配置されているならば、入射した光はそれぞれの原子からの散乱光が干渉して、透過光と反射光になって屈折の法則と反射の法則に従う特定の方向のみに進み、それ以外の方向には現れないことになる。 光の錯乱は障害物の大きさにより、障害物が光の波長の10分の1以下の場合がいわゆるレイリー散乱と呼ばれるもので、光の色による依存性が出てくる。空が青いのは、空気分子による太陽光のレイリー散乱による。 光と微粒子との相互作用によって起こる散乱の程度は、光の波長 λ と、微粒子つまりその分子や原子による電場・磁場の領域Dとの相対関係で決まる。微粒子の電場・磁場の領域 D が光の波長 λ よりも遥かに小さい場合( D << λ )は、光の波長が短いほど散乱され易く、具体的には波長 λ の 4 乗に逆比例して散乱され易くなる。赤色の光の波長は、青色の光の波長より約2倍ある。青色の光は約16倍も散乱していることになる。 この領域の散乱が「レイリー散乱」と呼ばれる。 この光のスペクトルを、温度の違いごとに調べても、光の強さはある波長で頂点に達し、その後急速に弱まってしまう。熱した物体が出す光のスペクトルの「一番強い光の色」は、その物体の温度がどうであれ、ある波長で頂点に達し、それ以上波長が短くなっても、その光のスペクトルは急速に弱まる。その観察結果を、当時では理論的に説明できなかった。プランクが唱える量子と言う学説では、ある一定の波長を持つ光のエネルギーは、連続しない「とびとびの値」が、それぞれ「固まりのようになり」解離している、と見ている。量子と言う画期的な理論展開ではあったが、その当時、プランクは、「光は粒子である」と明確に主張したわけではない。 原子に結合している電子にしても、量子力学的な性質によって、あるとびとびの状態しかとれない。その状態をエネルギー準位energy levelと言う。 エネルギー準位の中で、 最もエネルギーの低い状態を基底状態ground state、それ以外の状態を励起状態excited stateと呼ぶ。これらのエネルギー準位は、量子数と呼ばれる自然数(n =1, 2, …)で番号づけられている。 分子もすべてエネルギーを持っており、分子が持っているエネルギーの量も連続的なものではなく、量子化されている。これはあるエネルギー準位に対応する振動数でのみ、分子は振動することができることを意味する。 電磁波は「空間の電場と磁場の変化によって形成された波」であり、「物質がエネルギーを外部へ放射するときに生じるもの」であり、「光は特定の範囲にある電磁波」であり、「光こそが物質から放出されるエネルギー」である。 太陽や夜空の星は、そのエネルギーによって異なった色の発光する。450nm付近の波長であれば青色の光、青天の輝きとなる。人は、この光を見ることで、波長の違いを色として認識する。 それでは、発光しない物質の色は何によって変わってくるのか。物質はある一定のエネルギー(ここでは一定の光の波長)を吸収する。例えばリンゴであれば、400~600nm付近の光を吸収するが、600~700nmの赤色の光は吸収されず、散乱、反射する。この600~700nmの散乱・反射した光が、人の目に入りリンゴが赤く見える。 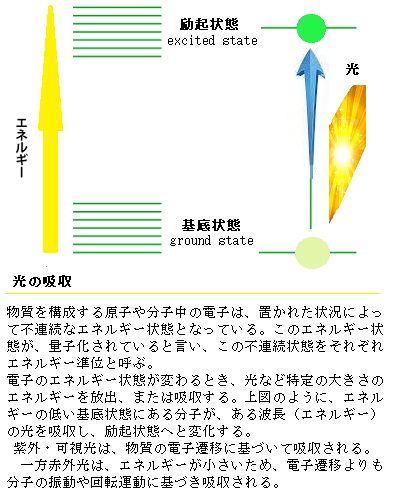 紫外線や可視光は、物質の電子遷移に基づいて吸収されるが、赤外光(2.5~25μm)は、紫外線や可視光(0.2~0.78μm)よりもエネルギーが小さく、電子を遷移させることができないが、分子に赤外領域のエネルギーを与えると、化学結合の振動が生じる。このとき、吸収された赤外線エネルギー量を測定することで、化学結合の種類を知ることができる。そのため、むしろ分子振動のエネルギーの解析に当る。「赤外分光法」は、物質に赤外光を照射し、透過または反射した光を測定することで、試料の構造解析や、質量・質量比・物理量などの定量分析などに利用される。 紫外線や可視光は、物質の電子遷移に基づいて吸収されるが、赤外光(2.5~25μm)は、紫外線や可視光(0.2~0.78μm)よりもエネルギーが小さく、電子を遷移させることができないが、分子に赤外領域のエネルギーを与えると、化学結合の振動が生じる。このとき、吸収された赤外線エネルギー量を測定することで、化学結合の種類を知ることができる。そのため、むしろ分子振動のエネルギーの解析に当る。「赤外分光法」は、物質に赤外光を照射し、透過または反射した光を測定することで、試料の構造解析や、質量・質量比・物理量などの定量分析などに利用される。化学結合する力は、粒子間の電子の授受による。通常、物質は、いくつかの原子が結びついて分子や結晶を作ったり、イオン同士が働いて結晶を作る。この物質中での原子と原子の結びつきを化学結合という。原子の種類ごとに、電子を引き寄せて束縛しようとする力は異なり、これを相対的に数値で表示したものを電気陰性度electronegativity(原子が共有電子対を自分の方に引っ張る強さ)と呼ぶ。電気陰性度の大きい原子と小さい原子が結合するのが一般的であるが、電気陰性度の大きい物ほど、電子を吸引する力と電子を束縛する力が大きい。 およそ、すべての有機化合物は、赤外領域に固有の吸収スペクトルを持っている。原子同士の結合は硬く固定されているわけではなく、バネで繋げられるように、ある程度の柔軟性をもっている。分子の振動や回転の状態を変化させるのに必要なエネルギー(赤外光の波長)は、物質の化学構造によって異なる。結合振動は、伸縮振動(結合の長さが変化する振動)と変角振動(結合距離はそのままで結合角が変化する振動)の二つに大別される。この伸縮振動と変角振動のエネルギーはそれぞれ異なっている。つまり、一つの化学結合に対して、二種類のスペクトルが現れることになる。 赤外光により原子間を繋いでいる化学結合が、赤外線の照射により以前よりも激しく伸び縮みをする。その試料分子に赤外線を照射し、振動している化学結合の振動数が照射光の振動数と一致すれば、赤外線のエネルギーが吸収される。エネルギーが吸収されると、その振動している化学結合の振幅が増大する。この領域の電磁波のエネルギー吸収を検出し、波長に対して透過した光のパーセント(透過率、%T)を図表化すると、あらゆる物質は分子中に特定の結合を含んでいるので必ず固有の赤外吸収パターンを示す。これが赤外(IR)吸収スペクトルinfrared absorption spectrometry である。試料の構造解析や定量観測を行う分析手法の蓄積により、物質に赤外光を照射し、透過または反射した光を測定することで、化学構造や状態に関する情報が容易に得られるようになる。 アインシュタインは、1905年に発表した「特殊相対性理論」に先立つ3カ月前に、「光量子仮説(こうりょうしかせつ)」と呼ばれる、「光はエネルギーを持った粒子である」と最初に論評した。現在では、「光のエネルギーを持った粒子」を、「光子」と呼ぶ。電磁気力の力の粒子は光子、電磁気力は光子をやり取りすることで伝わる、と説明する。 アインシュタインは、光電効果を説明するため、以下のような仮説を立てた。 1) 光は、エネルギーを持った粒子(光子)の流れである。 2) 光子1個と電子1個が衝突すると、光子の持っていたエネルギーはすべて電子に渡り、光子はなくなる。 3) 光子1個が持つエネルギー E は、E=hν で表される( h : プランク定数, ν: 光の振動数)。 原子の内部では原子核の周りを、電子が雲のように広がって覆っているが、金属原子の場合では、負電荷の電子が正電荷の原子核の影響から離れて自由に移動している。放出された電子は、伝導電子として、金属の陽イオンが配列した空間を移動して電気伝導に寄与する。それにより、電流は-極から+極の方へ向かう電子の流れに従う。チタンなどの金属元素では、一部の電子が原子核の周りの狭い領域に局在しており、それが高温超電導などの特性に寄与する。 原子核により束縛された電子の振舞いは、飛び飛びのエネルギーをもった定在波として表される。 各エネルギーに対応した特徴ある電子の分布を 軌道orbitalと言う。金属の中でも特に電気伝導率が高い銅では、4s電子(s軌道s orbitalとは、原子を構成している電子の軌道の1つ)が、銀では5s電子が伝導電子として結晶中を運動している。結晶や分子、原子の中で起こる電子運動やエネルギー状態を電子構造ectronic structureと呼ぶ。 金属板に光を当てると、そこに溜まっている電子が飛び出してくる。電子は金属の中で、自由電子気体 と呼ばれるエネルギー状態を保っている。電子が持つエネルギーはそれぞれ異なり、 個々の電子によって違う値を持つが、伝導電子を一定の空間内を互いに相互作用することなく自由に運動する量子であると考え、 このようにとらえ た電子の状態を、気体分子の運動になぞらえて自由電子気体free electron gasと呼ぶ。 電子自体エネルギーを持つが、これだけでは金属の外に飛び出すことはできない。金属中に閉じ込められた状態にあるままで、どれだけのエネルギーを誰から受け取れば、金属の外へ 飛び出すことができるのか? 金属中に存在している電子が、本体の金属の外へ出て行くということは、自然に起こることはない。電子にエネルギーを与えれば、電子は金属の外へ 飛び出すことができる。 光が波であるとすると、電子は光が当たるたびにエネルギーを吸収すると考えられる。吸収したエネルギーが大きくなれば、金属から飛び出すことができるはず、もしそうだとすると、光の振動数に無関係に、エネルギーの大きい強い光を当てるか、 エネルギーが小さい弱い光でも長時間当て続ければ、電子は飛び出せるはず。しかし、実験結果はそうならない。光は波としての性質以外に別の性質を持つことが分かる。 現在、「エネルギーを持った光の粒子」は「光子」と呼ばれ、光は「波の性質と粒子の性質を兼ね備えている」ことが定説である。 実は、光に粒子のような性質があることは、ニュートンの時代から言われてきた。光に照らされてできる、遮られた影と陰は、光が粒子である明らかな証明である。また、光が波であることは、流れの中の障害物の後ろに回り込む波のように伝わっていく様子から実感される。この性質を回折diffraction(かいせつ)と呼ぶ。波長が大きいほど回折角、即ち障害物の背後に回り込む角度が大きくなる。 その一方、光が波であることは、2つの波が重なる時に生じる「干渉」と言う現象から明らかである。2つの波が重なる合成波により大きくなったり、小さくなったりする。2つの光が重なる時、光の山と山が重なればより明るくなる。光の山と谷が重なると波を打ち消し合い暗くなる。また、波長の違いによって色付きが生じている。 量子quantumと言う考え方は、光の研究から生まれた。それが原子の構造を理解するためには不可欠な論拠となり、それ以来、量子力学は、従来の物理学のニュートンやマックスウェルなどが説く基礎的理論とは別の物理学における原理原則を組み立てってきた。それを実証する実験成果も同等と評価され、ノーベル物理学賞の栄誉に浴する。 「波」は物質ではなくて「状態」である。海水という「物質」があり、その「状態」が波である。原子より大きければ、「物質」と「状態」をはっきりと区別できるが、原子より小さい素粒子の世界では、その区分は困難を極めた。 電子は「物質」だけでなくて「状態」でもあるも、しかし「海水」にあたる物質が見当たらない。粒子性(物質の性質)と波動性(状態の性質)を併せ持つ、このような特殊な存在を、 普通の物質と区別するため、「量子」(quantum) と呼びようになった。 1897年、イギリスの物理学者J.J.トムソンは、実験によって「陰極線」が様々な元素に共通して存在する粒子と分かり「物質片corpuscles」と名付けた。この粒子が「電子」と呼ばれた。 1905年、アインシュタインは、それまで波動であると考えられていた「光」が、粒子性も合わせ持つとして「光量子説」を発表した。 1927年のノーベル物理学賞の受賞者であるスコットランド物理学者ウィルソンCharles Thomson Rees Wilsonは、大 学卒業後、気象学に興味を持ち雲に関する研究 を始めた。1894年、イギリス最高峰のベン・ネヴィ ス山の山頂にあった気象観測所に臨時スタッフ として数週間駐在する機会があり、雲や霧が光 と織りなす現象の不可思議な美しさに感動し、実験室でこの雲や霧を再現しようとした研究過程で、霧箱を創作した。 霧箱は、密閉容器 の中に水分を含んだ空気を入れて、急激に減圧し過飽和状態にし、更に過冷却すると、気体分子のイオン化が起こり、そのイオンが凝結核condensation nucleus(大気中に含まれる水蒸気が凝縮して水滴を生じるときの核となる微粒子)となって霧を発生させる。1895年、X線が発見されると、ウィルソンはさっそくエックス線をガラス瓶に照射した。 霧箱中には、空気の元素(窒素、酸素)や水分が含まれている。その中を放射線が通ると、その道筋に沿って電離が起こり陽イオンが発生する。この陽イ オンが凝結核となって周囲にある水分が集まり、その気体の中に霧の飛跡を作る。これにより「光子の飛跡」が観測された。 アインシュタインの「光量子仮説」の光の粒子性を、さらに確実に証明したのが、1923年、アメリカの物理学者コンプトンの実験であった。 X 線が「粒子」となって 黒鉛 (炭素の結晶) 中の電子という 「粒子」に衝突して散乱されることによって 、光はエネルギー hν を持った「粒子」 となって 空間に存在することが 確実になった。 コンプトンは波長が一定のX 線を黒鉛 照射した時、 散乱角が大きくなると 散乱された X 線の波長が長くなることに気付いた。入射したX 線が 「粒子」として電子に衝突し 散乱された際に、反跳電子にエネルギーEを奪われた分だけ振動数が減少したと考えた。入射した X 線の「粒子」の エネルギーEを hν、運動量pを hν/ c とし、 散乱角θの方向に 散乱された X 線の「粒子」の エネルギーE'はhν'、 運動量p'は hν'/ c とし、衝突された反跳電子のエネルギーE'を E'= hν-hν'とした。 コンプトン散乱は、 X 線の粒子性を見事に説明したが、コンプトンの実験では、弾き飛ばされた反跳電子の観測はできない。これは少し後にウィルソンの霧箱 を使って写真に撮ることができた。1927年のノーベル物理学賞は、 「コンプトン効果」と「ウイルソンの霧箱」の同時受賞であった。 1924年、フランスの理論物理学者ルイ・ド・ブロイは、光に二重性があるように、電子や陽子といった、それまで粒子と考えられてきた物質粒子一般にも拡大適用できりる、と発表した。これが後に「物質波」とか「ド・ブローイ波」と呼ばれる。その実正研究により、1928年、「物質波」の存在が、後に結晶の回析実験により、証明されることになる。ド・ブロイ氏の提案から数年後、それまで粒子だと信じて疑わなかった電子が、波としての性質を持つことを認めざるを得ない実験結果が発表された。 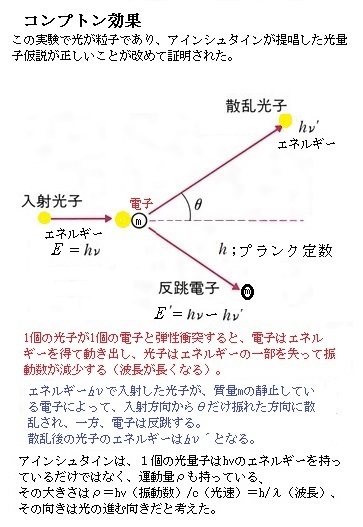 デビソンとジャーマーの実験が有名である。ニッケルの単結晶に照射した電子が、ある方向に強められて散乱されるのだ。これは波が回折・干渉してある角度に強く跳ね返る様子に非常に似ている。これはド・ブロイが「もし、物質粒子がそれらに伴う波の波長と同程度の幅をもつスリットを通過すると、光子が単一のスリットの実験で回折refractionするのと同様に、物質粒子も回折を引き起こす」とした提案の正しさが証明された。 デビソンとジャーマーの実験が有名である。ニッケルの単結晶に照射した電子が、ある方向に強められて散乱されるのだ。これは波が回折・干渉してある角度に強く跳ね返る様子に非常に似ている。これはド・ブロイが「もし、物質粒子がそれらに伴う波の波長と同程度の幅をもつスリットを通過すると、光子が単一のスリットの実験で回折refractionするのと同様に、物質粒子も回折を引き起こす」とした提案の正しさが証明された。
20世紀初頭、量子論によって、電子は粒子と波の両方の性質を持つことが認められた。「quantum(kwάnṭəm)」とは、本来、「(特に)少量」を意味するが、原子より大きい世界で観察される「物質」とは異なる振る舞いをする(make a quantum of effort もう少し努力をすれば)。量子論の成果により、電磁波である光が真空中であっても伝わることが、その「粒子性」により説明できようになった。 電子も波のような「波動性」を持っている。その波の形を調べようとして、電子の波動を数学の関数の形で記述したものを 「波動関数」と呼ぶ。 量子力学的な実験結果で証明されるか、その理論が基礎方程式に組み立てられる直前までを量子論と呼び、実験により証明されるか、基礎方程式が確立すれば量子力学と呼び分けている。 量子力学では電子の運動の基礎方程式を、波動方程式とする「波動力学」(シュレーディンガー流)が確立されている。その「量子」を研究するのが「量子力学」で、電子は「量子」の代表格である。単に、原子を構成する「部品」ではなく、あえて「量子」と呼ばれる重要性がある。 電子の波動性を理解する上で最も分かりやすい実験結果の1つに、スリットを通る電子についての測定が挙げられる。電子も光と同様に、スクリーン上に干渉縞が現れる。 電子が単なる粒子であればスリットを通った電子は単に直進するのみである。 もう一方のスリットが開いていようが閉じていようが 1つのスリットを通った電子がスクリーン上に到達する位置は変わらないはずだ。それにもかかわらず干渉縞が現れることは、確かに電子が波の性質を持っていることを示している。 しかも電子にも粒子としての性質がある。 高感度のスクリーンを用いることで、 1つ1つの電子がスクリーン上に到達した位置を記録することができる。干渉縞が現れる場合にも、1つの電子は1つの点に到達する。明らかに、電子も粒子なのである。 目次へ |
|||||||||
| 8)光子の運動量 そもそも高温の物体は振動する。それにより電子が振動すると、光が生じ周囲に広がる。電子の固有振動数は、物質中における電子の状態により様々に変わるが、その固有振動数と一致する光を受け取ると、電子はその固有振動数で振動を始める(共振、または共鳴と言う)。 光を含む電磁波の種類は多く、物質に与える影響は様々であるが、すべてが電子や極性分子を振動させることができる。ただし物質の固有振動数も様々なため、その振動数に一致した電磁波が来た時だけ振動する。 例えば、電磁波の中でも振動数が大きい(波長が短い)紫外線やX線、ガンマ線は、大きなエネルギーを持っているので、分子中の電子を弾き飛ばして化学結合を壊したり、電気的に中性な原子の電子を弾き飛ばして、電荷を持ったイオンにしたりする。振動数が大きい電磁波が細胞の中のDNAにぶつかると、DNA分子中の電子を弾き飛ばし切断するなど傷を負わせ、それが蓄積されると細胞の癌化を招く。 分子中の電子は、通常、特に固く結合しているため固有振動数が大きく、非常に速く振動している。そのため振動数の大きな電磁波でないと電子を弾き飛ばせない。 電子の固有振動数も、電子が物質中で、どのくらいの強さで結合しているかで決まる。例えば、金属中の自由電子free electron(物質内で特定の原子間の結合に束縛されず自由に動き回れる電子)は結びつきが弱く金属内を自由に行き来する。自由電子が金属結晶などには豊富に含まれるため電気をよく通す導体となり、ゴムなどには含まれないため絶縁体(不導体)となる。そのため金属は、電磁波のどんな振動数でも電子は共振する。ただし余り振動数が大きい紫外線くらいになると電子は自由に動けなくなる。 「温度」とは、物質中の原子や分子の運動の激しさを表す指標になる。すべての原子や分子の運動がとまる温度を「絶対零度」と言う。摂氏マイナス273.15度である。それから温度が高くなるほどに、原子や分子が激しく振動したり、勢いよく回転したりする。 分子の中で電子の偏りがあると、分子全体で中性であっても、電気的に片側がプラス極に、反対側がマイナス極に分かれる極性分子となる。この極性分子も振動・回転をするから、プラス極とマイナス極が振動することになり、光(電磁波)が生じる。このように電子の振動や極性分子の振動・回転で発生する光(電磁波)を「熱放射」と呼ぶ。温度の高い物体ほど、原子や分子が激しく振動するので、電子も激しく振動し、その結果、振動数の大きく、波長の短い光がより多く放出される。 赤外線は熱を持ったあらゆる物体から発生する。赤外線は日常生活的な温度でも熱放射により発生する電磁波である。そのため人の体からも放出されている。物体の温度が、およそ摂氏2,000度以上になると、赤外線より振動数が大きい可視光が多く放出される。 熱放射では、原子や分子がランダムに振動するので、電子もランダムな速さで振動するため、様々な振動数の電磁波が電子から放出される。白熱電球も、電流を流すとフィラメントが熱くなり、温度が急激に上がるにつれ強い光を放ち、2,000度以上の高温になると白く光る。ただ、可視光だけでなく、赤外線も多く放出している。そのため白熱電球は非常に熱くなり、エネルギー効率の観点から、本来、可視光だけでよいので、赤外線が多く放出される分は無駄なエネルギーになる。 効率的に光を生み出す蛍光灯やネオンサインは、放電などによって原子にエネルギーを与え、原子の中で電子を「軌道ジャンプ」させることで光を生み出している。 原子の構造は、中心部に質量を占める原子核があり、その外側の「存在してもよい軌道」を電子が回っている。原子核に一番近い内側の軌道を「基底状態」と言い、その外側の軌道を「励起状態」と呼ぶように、中心から遠い軌道ほど円周距離が長い分、勢いが強くなり、原子核から遠い軌道にある電子ほどエネルギーが高い。 通常の安定した原子の中では、電子はできるだけ内側の軌道を回ろうとする。そこに、原子外から来た 高いエネルギーを持った高速の電子が原子に衝突し光を放つと、元々原子内にあった電子は、その光を受け取って「励起」して、その外側の軌道へ「ジャンプ(遷移)」する。 原子は興奮し続ける「励起状態」を長く保てず、やがて電子は元の内側の軌道に「遷移」しようとする。この戻る時に、より低いエネルギーなるため、その差のエネルギーを「光」として放出する。ここでも「電子が動けば光が生まれる」、その原則が働く。その過程において、核心となるのは、余分なエネルギーは光として放出され、外側の軌道へジャンプする時には光は発生せず、内側にジャンプする時だけ光が放出される。 このようにして生まれた光は、電子が外側の軌道にいる時のエネルギーと、内側の軌道にいる時のエネルギーとの差を、エネルギーとして持っていることになる。光などの電磁波のエネルギーは振動数で決まるが、どんな振動数の電磁波になるかは、原子の種類で変わる。その特定されている振動数の光だけが放出される。つまり、その光は、軌道のエネルギー差に相当する「特定の振動数」を持つことになる。 LEDはフィラメントを利用する白熱灯や蛍光灯と異なり、電気を直接光に変化させるという発光原理である。そのため、電気が効率的に光へ変わり、消費電力が節約できる。LEDチップへ電気を流すと、N電極(マイナス電子が多い半導体)からP電極(プラス正孔が多い半導体)へ電子が流れ、衝突が起きた部分で発光が起こる。これは、P型半導体の正孔とN電極の電子が結合し、エネルギーが放出されるためで、この状態を再結合と呼ぶ。その再結合時に、電子と正孔が元々もっているエネルギーの和よりも小さくなるため、余分となったエネルギーが光として利用される。 LEDからは、白・赤・青・緑といった様々な色彩を放出されるが、それはLEDチップに含まれる化合物による。化合物にはアルミニウム・ガリウム・インジウム・ゲルマニウム・窒素・リンなど様々なだが、それぞれ波長が異なり、この波長の長さがLEDの色を決定する。 光は波であるだけでなく、同時に粒子としても振る舞う。粒子としての波を光量子と言う。これはプランクが考え出した量子論の考え方を適用したもので「光量子仮説」と呼んだ。 光にはエネルギーの最小単位があり、その最小単位が光子である。そのため光子のことを「光量子」と呼ぶこともある。 振動数ν(ユニー)の光であれば、hνのエネルギーを持つ光子なのだ。そのエネルギーの最小単位は光の波長によって異なり、波長の短い光ほど最小単位のエネルギーは大きく、波長の長い光ほどエネルギーの最小単位は小さくなる。つまり、光は波としての性質と同時に、粒子としての性質も持っている。これが「波と粒子の二重性」の概念であり、量子力学誕生のきっかけとなった。その後、電子や陽子などの粒子も波動的性質を持つことが分かった。 アインシュタインは、1個の光量子は、hνのエネルギーを持っているだけでなく、光量子は粒子として考えられるので、エネルギーも持つが運動量Pも持つ。 その大きさは、 P= hν/c= h/λ で、その向きは、光の進む向きだと考えた。光子の運動量Pは、振動数νに比例して、波長λに反比例する。 光子の運動量はプランク定数hに光の波長λの逆数をかければよいのである。 光子のエネルギーは次式で、 E= hν これにアインシュタインの相対性理論の式E=mc2を代入すると次式になる。 mc2= hν この考え方は、アメリカの物理学者アーサー・コンプトンArthur Holly Comptonによって実験的に確認された。静止している電子にX線を当てると電子は、エネルギーを得て飛び出し、衝突後に散乱したX線は、エネルギーを奪われ波長が長くなることが見出された。このX線を光子と考え、1 個の光子が1個の電子と弾性衝突(衝突の前後で2物体の力学的エネルギーの和が変化しない衝突)した結果、電子はエネルギーを得て跳ね飛びだし、光子はエネルギーの一部を失って振動数が減少し、波長が長くなる「コンプトン効果」と呼ばれ現象が生じ、光が粒子であることを示す有力な証明となった。 現在の量子力学は、観測しない時に電子はどの位置にあるのか、といった問いには答えない。「実験事実により検証できない内容については議論しない」という研究スタイルである。それが「観測により検証された内容」であれば、量子力学は方程式から完璧な軌跡を予想して見せる。観測された物理現象が説明でき、しかも論理的に矛盾のない基礎方程式を作り上げるからである。時には、正しそうな方程式が先に組み立てられ、後からその意味を考え、.その後の測定結果と矛盾が無ければ、それが正しい理論とされる。予想と異なる測定結果が現れたら、理論を修正する手順を踏むこともいとわない。その方程式から予測される事があれば、新たな実験と観測により検証もする。 直感的に理解できる方程式が基礎となっていた古典物理学と比べると、 量子力学の真価が発揮される粒子の世界では、直感が正しく働かないか、 直感とはかけ離れた不可解な論理構成になっている。 19世紀末から20世紀初頭に始まった量子論ないし量子力学は、1926年にエルヴィン・シュレーディンガーがそれまでの物理学と発想が異なる、シュレーディンガー方程式(波動関数)によって量子の状態を確率的に定めることができる数式を発見したことが大きく貢献した。これは重要な発見であったが、シュレーディンガー自身、量子の状態は決定論的に予想することが可能、しかし、まだ途上であると考えていた。これは当時の多くの物理学達の共通の考えでもあった。 すなわち波動関数は、それ自体で既に完成しているのであるが、量子の状態を決定論的に表すことはできないというものであった。これを確率解釈という。 1905年、アインシュタインによって理論が発表され、それまで波動と考えられていた光が粒子性を有しており、1 つの粒子としての光子が E= hν のエネルギーを持つことが示された。 第7代フランスのブロイ公爵・理論物理学者ルイ・ヴィクトル・ド・ブロイLouis Victor de Broglie(1892~1987)が、1924年、「光が二重性を持つならば、物質もまた二重性を持つはずだ」と言う「ド・ブロイ波(ド・ブロイの物質波)の理論」を発表した。 ド・ブロイが光以外の物質にも波動性であると着想したのは、1922 年初頭に光量子に関する論文を書いてから1923年9月に至るまでの長い熟考の時期があった。その理論の特徴は特殊相対性理論を指導原理とし、光量子に付与すべき質量を精確に測定することを目指した。  その思考の過程で、ド・ブロイは質量を持つ任意の物質粒子にも、波動性が存在するのではないかと着想した。ド・ブロイのこの考えが、特殊相対性理論は質量を
もつ任意の物質粒子にも拡張できる可能性があり、そこから質量と振動数を結びつけるという飛躍的な着想をする。 微視的粒子も光の波動性を共有し、 その思考の過程で、ド・ブロイは質量を持つ任意の物質粒子にも、波動性が存在するのではないかと着想した。ド・ブロイのこの考えが、特殊相対性理論は質量を
もつ任意の物質粒子にも拡張できる可能性があり、そこから質量と振動数を結びつけるという飛躍的な着想をする。 微視的粒子も光の波動性を共有し、プランクの式の E = hν アインシュタインの特殊相対論の式 E = mc2 とを関連付けて、振動数をもとに質量を定義しようとした。 ド・ブロイによる提案は、次の2式から定式化される。 E=hν 光の振動数νとエネルギーEを結びつけるこの式は、光に対して適用される式だけでなく、あらゆる物質が共有する波動性を示す非常に重要な一般式と考えた。 一方、ジェームズ・クラーク・マクスウェルJames Clerk Maxwellの電磁気学において、光の運動量pと光の速度cとの積から、 E=cp というエネルギー Eの関係式が見出されていた。 光の波長λは λ = c /ν = h / p が導かれていた。 ド・ブロイは、微視的粒子の運動量pを p = mv ①式 質量mと速さvとの積で示した。 波動性の運動量pを p = h / λ ②式 量子力学における基本となるプランク定数、h=6.62607015×10-34J・s(ジュール秒)を波長で除算する値で示された。 ①式と②式から ド・ブロイは、この考えが質量を もつ任意の物質粒子にまで拡張できる可能性があると認識、そこから質量と速度vを結びつけるという飛躍的 な着想を得た。 h / λ = mv= p ③式 ド・ブロイの波長は、 λ = h / p = h / mv となる。 このド・ブロイの関係式は、すべてのミクロの物質が、h/pで表される波長をもっていることを示す。この波を「ド・ブロイ波」、または「ド・ブロイの物質波」と呼ぶ。 つまりアインシュタインが考案した「光の二重性」は、、他の微視的粒子にも共有されている、と仮説が立てられ、ド・ブロイの関係式λ=h/pから「粒子は全て波でもある」と公子ルイ・ド・ブロイが一本の博士論文を書き上げた。 これは、光の二重性は、ミクロの世界に存在する物質全てが、光のような波動性と粒子性を持つことを示し、量子全てに共通する重要な性質であることを明らかにした。 ボーアの量子条件とは、「電子軌道が存在する条件は円軌道の長さがド・ブロイ波の波長の整数倍である事」である。ド・ブロイ波とも呼ばれるこの波は、半径γ(ガンマ)の円軌道を電子e-が振動ν(ニュー)しながら、質量mでまわっている式である。 ド・ブロイの論文は斬新過ぎて、提出された教授陣の理解を超えたため、アインシュタインに意見を求めた。アインシュタインは「この青年は博士号よりノーベル賞を受けるに値する」と予言した有名な逸話が残っている。 このド・ブロイ波を説明するための微分方程式が、シュレディンガー方程式と呼ばれる方程式だ。実際、「ド・ブロイ波」の存在が実験で確かめられる以前に、シュレーディンガーの方程式が発表されている。シュレディンガーが波動力学を構築するようになった動機も、アインシュタインがド・ブロイの物質波に関連して論文を発表し、それを詳しく大学のセミナーで紹介するようにシュレディンガーに依頼したからであった。当時、シュレディンガーは1921年からて6年間、スイスのチューリッヒ大学で数理物理学教授を務めていた。 ルイ・ド・ブロイは、アインシュタインの予言どおり、この博士論文発表後の僅か5年後の1929年、ノーベル物理学賞を37歳で受賞した。 ノーベル物理学賞は、その理論が実証されて初めて授与される。1927 年にデヴィッスンC.J.DavissonとジャーマーL.H.Germerの共同実験で、電子ビームを金属結晶に照射すると、その散乱角と強度の間にはX 線の場合と似たような電子回析が起きたことを示した。1927年、G.P. トムソンの実験でも電子線の回折を確認した。1937年、「結晶による電子線回折現象の発見」によりC.J. デヴィッスンとともにノーベル物理学賞受賞。陽子や電子のような物質を構成する基本粒子は、古典力学では、粒子として取扱われる。しかし、量子力学によると、これらの物質粒子は粒子性とともに波動性を持っている、と解析する。 ド・ブロイの関係式にボーアNiels Bohrの量子条件を当てはめれば、電子が円軌道を描くと言うボーアモデルが説明できる。電子が波とすると、その軌道に整数倍と言う条件が付くことも、ド・ブロイの関係式をボーアの量子条件に代入すれば導ける。 半径 γ の円軌道の円周の長さは 2πγ 、電子が波であるなら、円周の長さは波の波長の整数倍でなければならない。電子が円軌道で周期性を保つためには一周して戻ってきた時に元に戻らなければならない。一周して元に戻るには円周の長さが波長の整数倍(1倍・2倍・3倍...)である必要がある。整数倍でないと、元に戻れないため、「波の干渉」により周期性が保てられない。 ボーアの量子条件は γp = η(h/2π) なので、ド・ブロイの関係式を代入すると 2πγ(h/λ)= ηh (η=1,2,3…) (h /λ= p = mv) となり、これにド・ブロイ波長の公式に代入すれば、次の条件が成り立つ場合のみ波が存続できる。 2πγ mv= ηh ド・ブロイの物質波の仮説は、シュレーディンガー の波動方程式として示された。シュレーディンガー方程式 を解くことによって、ボーアの量子論の結果も全て完璧に導くことができる。そして ミクロの世界の謎が次々に解決されてきた。 シュレーディンガー方程式が、様々な系、例えば水素原子の解析など、方程式の結果と実験データとが見事に一致するため、シュレーディンガー方程式が 「量子力学」の基本方程式であり、ミクロの世界を支配する基本原理であることが理解されてきた。より精密化されて「量子力学」が基礎物理学の柱の一つになり、量子力学は金属や半導体のような物質の性質を説明するのに不可欠となり、電気電子工学にとっても重要な分野でとなっている。 シュレーディンガー方程式は、現在でも、ミクロの世界を支配する 革命的な新力学 「量子力学」 の 基本方程式 となっている。ニュートンの運動方程式が マクロの世界を支配する基本方程式であるのと対比される意義は大きい。 目次へ |