| Top 車山高原 車山高原お知らせ 車山ブログ 歴史散歩
|
DNA DNAが遺伝物質 生物進化と光合成 葉緑素とATP 植物の葉の機能 植物の色素 葉緑体と光合成 花粉の形成と受精 ブドウ糖とデンプン 植物の運動力 光合成と光阻害 チラコイド反応 植物のエネルギー生産 ストロマ反応 植物の窒素化合物 屈性と傾性(偏差成長) タンパク質 遺伝子が作るタンパク質 遺伝子の発現(1) 遺伝子の発現(2) 遺伝子発現の仕組み リボソーム コルチゾール 生物個体の発生 染色体と遺伝 減数分裂と受精 対立遺伝子と点変異 疾患とSNP 癌変異の集積 癌細胞の転移 大腸癌 細胞の生命化学 イオン結合 酸と塩基 細胞内の炭素化合物 細胞の中の単量体 糖(sugar) 糖の機能 脂肪酸 生物エネルギー 細胞内の巨大分子 化学結合エネルギー 植物の生活環 シグナル伝達 キク科植物 陸上植物の誕生 植物の進化史 植物の水収支 拡散と浸透 細胞壁と膜の特性 種子植物 馴化と適応 根による水吸収 稲・生命体 胞子体の発生 花粉の形成 雌ずい群 花粉管の先端成長 自殖と他殖 フキノトウ アポミクシス 生物間相互作用 バラ科 ナシ属 蜜蜂 ブドウ科 イネ科植物 細胞化学 ファンデルワールス引力 タンパク質の機能 呼吸鎖 生命の起源 量子化学 同化:生物が無機物質を取り込み、生体で利用できる物質にする反応を指す。 固定:ガス状の物質を取り込む意味合いが強く、非生物にも使われる。 1m = 103mm ; = 106µm ;= 109nm |
| 目次 |
| 1)「生物の誕生」は素粒子から |
| 2)宇宙誕生 |
| 3)地球の誕生 |
| 4)ジャイアントチューブワーム |
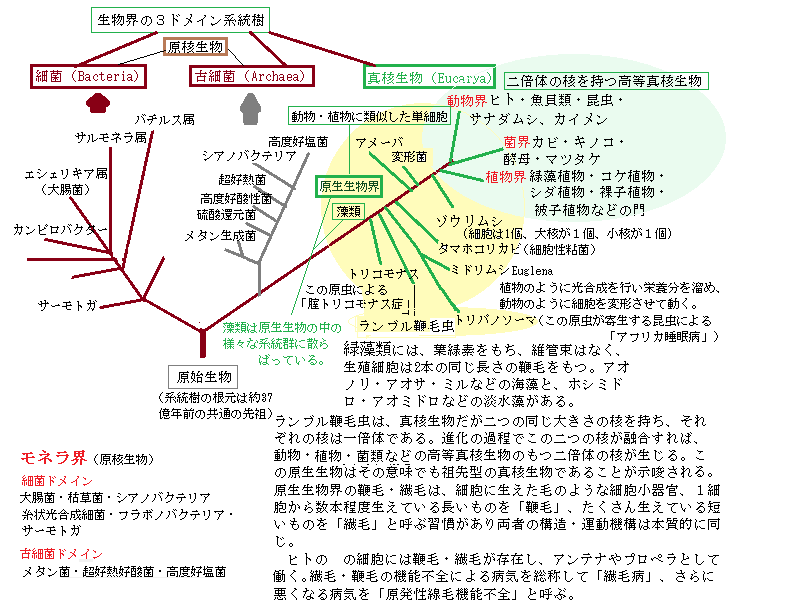
| 5)生物の単一性と多様性 |
| 6)真核生物 |
| 7)脂質二重層の薄い膜 |
| 8)原核生物 |
| 9)プラスミド |
| 10)古細菌(アーキア) |
| 11)シアノバクテリアcyanobacteria(藍色細菌) |
| 12)葉緑体とミトコンドリア |
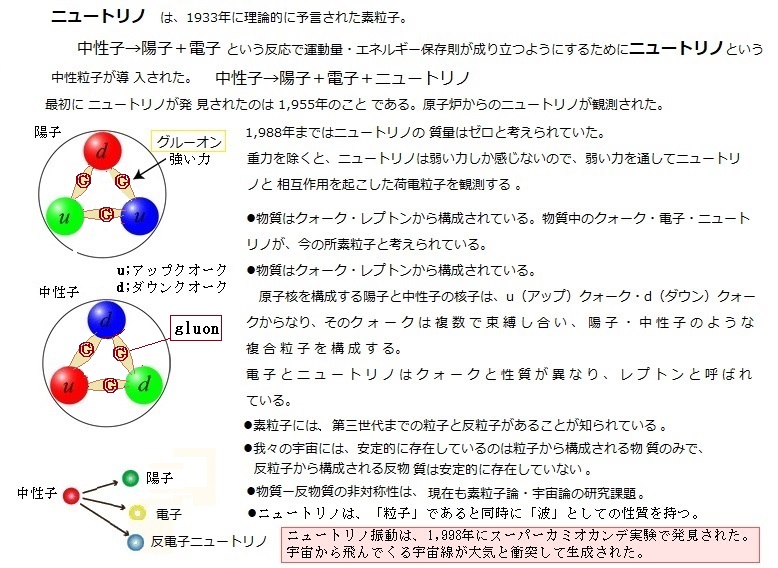
素粒子は一種の自転をしていて角運動量(回転運動の勢い)により物理量を持ち、素粒子は物質を構成する素粒子と力を媒介する素粒子に大別される。物質を構成する素粒子には、クォークquark(陽子の中に存在する点状粒)族とレプトンlepton族の2つに分類されている。ニュートリノneutrinoは、電子の仲間のレプトンの一種で、電気的には中性なので、 中性微子(ちゅうせいびし)とも呼ばれる。例えばクォーク3つからできる陽子1つと、レプトンの仲間である電子1つを組み合わせて水素原子が作られる。
物質は、少数のクォークとレプトンからできている。その素粒子間を支配しているのがたった4種類の自然界の力である。それらは、素粒子の間に働く4つの力、「電磁気力」・「弱い力」・「強い力」・「重力」、これらの力はそれぞれ、光子photon(こうし;「電磁気力」を伝える働きをしている。光は波長に応じたエネルギーを持つ粒である)、ウィークボソンweak boson(陽子の約80〜90倍の質量を持つ粒子で、弱い相互作用を媒介する粒子であり)、グルーオンgluon(クォークを結びつけ、陽子や中性子などの核子を作り、またそれら核子から原子核を作る力)、グラビトンgraviton(未発見の重力を媒介する伝達粒子、未発見の理由は重力が他の素粒子の間に働く3つの力に比べて極めて小さいため)によって伝達されている、と言う。
即ち、陽子や中性子などを構成するクォーク族に働き掛け、原子核を構成する核子を作る「強い力」、電気や磁気を持つ粒子間に働く「電磁力」、β崩壊などに関与し、クォーク族にもレプトン族にも働く「弱い力」、そして質量を持つ粒子間に働く「重力」である。遠い距離まで作用する電磁力や重力と異なり、強い力と弱い力は非常に短い距離にしか作用しないため、日常生活では、その力の存在は感知できないが、粒子間の衝突や崩壊を通して、重要な役割を果たしている。
1932年に、中性子 neutronが発見されていた。さらに「電気を帯びていなくて、知らないうちにどこかへ飛び出してしまう、幽霊のような粒子がある、と考えるとつじつまが合う」と理論物理学の観点から、この粒子を、オーストリアの物理学者パウリは「ニュートロン」と呼んでいた。これが今日のニュートリノだった。
突然現れて明るく輝き、やがて消えていく「超新星爆発」は、「新」と言う呼び名とは真逆で、広大な宇宙で度重なる太陽の何倍もある重い星の終末期の姿である。この爆発のエネルギーの99%は、ニュートリノとして放出され、大量の物質が超高温・超高密度になった時の情報を、そのまま地球に届けている。
それは太陽の中心部の核融合反応で作られたニュートリノが、ほとんど何物にも遮られず、真っすぐ約8分後に地球に到達して、その中心部の情報を伝達していることでもある。 同じく核融合反応で作られる波長の短い光のγ線(ガンマ線;原子核の壊変によって原子核から放出される電磁波)は、数十万年費やして、ようやく太陽の表面にたどり着くまでに、電子などに何度も衝突して反応を繰り返すため、エネルギーを失って波長の長い可視光に変わっている。
ニュートリノが最も多く作られたのは、宇宙の始まり「ビックバン」と言われている。つまり宇宙空間は、その誕生以来、ニュートリノで満たされている。つまりニュートリノは、宇宙で一番多い、ありふれた粒子なのである。
宇宙マイクロ波cosmic microwaveは、宇宙の「最後の恒星の散乱面」から発せられている。ビッグバンが起こってから約40万年後、宇宙は低温になり、陽子が電子と結びついて中性の水素原子ができた。それまで散乱する電子に進路を阻まれていた光子が、ようやくまっすぐに進めるようになり、宇宙の「晴れ上がり」となった。宇宙マイクロ波は、この後に発せられた光と言われている。宇宙が誕生した瞬間を観測できないのは、宇宙の「晴れ上がり」前の光をとらえることができないからである。
もし宇宙を満たすニュートリノが観測できるようになれば、宇宙マイクロ波の観測より、さらにビックバン直後に遡る情報が得られることになると期待されるからである。
それまで理論的に解析された素粒子は、
中性子 → 陽子+電子
と見られていたが、1933年に、運動量・エネルギー保存則が成り立つ ようにするために、ニュートリノという中性粒子の理論が導 入された。
中性子 → 陽子+電子+ニュートリノ
中性子 ⇒ 陽子 + 電子 + 反電子ニュートリノ
最初に ニュートリノが発 見されたのは 1955年のこと である。原子炉からのニュートリノの観測による。
1998年までは、ニュートリノの 質量はゼロと考えられていた。
ニュートリノは、「粒子」であると同時に「波」としての性質を持つ。そのため、それぞれ異なる質量の固有状態を持つニュートリノ1、ニュートリノ2, ニュートリノ3は、それぞれ異なる振動数を持つ波として空間を伝搬する。このニュートリノの3種類は、「3種類のフレーバー(香り)を持つ」と表現された。
フレーバーは、それぞれの質量固有の波の重ね合わせとなり、ニュートリノが空間を飛ぶ間に波の位相が変化し、フレーバーの種類が移り変わる、と言う。 この現象を「ニュートリノ振動」と呼ぶ。「ニュートリノ振動」はニュートリノが質量を持つ証であり、かつ、ニュートリノ同士の混合があるときに起こる現象でもある。
「弱い力」、つまり弱い相互作用を媒介する素粒子であるウィーク・ボソンweak bosonは、陽子の約80~90倍の大きな質量を持っている。中性子の崩壊を起こす力を伝える粒子で、1つはWボソンという電子と同じ電荷を持つ粒子、もう1つはZボソンという電荷を持たない粒子の2種類がある。
Wボソンは陽子の約80倍、Zボソンは約90倍と他の素粒子に比べて大きな質量をもち、ごく短時間のうちに別の粒子に崩壊してしまうという特徴を持つ。 弱い相互作用 とは、素粒子の間で作用する4つの基本相互作用の内の一つである。弱い核力、あるいは単に弱い力とも呼ばれ、基本的に電磁力に比べて力の及ぶ範囲が非常に短い。この相互作用による効果は、放射性核種(放射性同位体)を崩壊させる力として発現し、代表的なものにベータ崩壊がある。
原子核のなかには、粒子や電磁波などの放射線を放出して、自然に他の原子核に変わったり、状態を変えたりする。これを放射性崩壊と呼ぶ。このような原子核を放射性核種という。自然に放射線を放出して崩壊し、他の原子核に変わる原子核、ウラン系列・アクチニウム系列などに属し自然界に存在する天然放射性核種と、原子炉や加速器で作られる人工放射性核種とがある。 「弱い力」は、電磁相互作用と比較して、その力学的相互作用の本質的な強さを表すの物理量は、電磁気力と同程度でありながら、力が届く距離が非常に短いため、その力は弱く見えるので、日常世界では感じ取ることができない。
実際には、 「弱い力」どころか、すべてのクォークやレプトンに働き、原子核のベータ崩壊、中性子などの素粒子の崩壊の原因となり、また素粒子 の種類を変えることもできる。例えば、ベータ崩壊で中性子がニュートリノと電子を放出して、陽子に変わる時などに微弱な力として原子核内で働く。
(この場合の「β崩壊」では、中性子が陽子へと変わるときに、電子とニュートリノが1つずつ放出される現象として現れる。)
素粒子とは、それ以上分割することができない最小の粒子であるため、内部構造を持たないと考えられている粒子のことである。原子核物理学では、理論的・実験的研究が盛んに行われている。当初の原子論が暗黙裡に納得していた素朴な図式が、根本的に崩壊した。物理学の理論全体としては、原子は当初となえられていたものとは極めて異質なものになっている。現実の原子は、原子の大きさに比べて原子核が極めて小さく、また電子は確率的に分布しているため、原子の構造を写実的に描くことは困難となっている。
現在ではクォークは6種類あることが分かっている。素粒子物理学の標準理論では、陽子はアップクォーク2個とダウンクォーク1個から構成され、中性子はアップクォーク1個とダウンクォーク2個からなる陽子に電子とニュートリノが含まれている。素粒子レベルで見ると、アップクォークとダウンクォークの 2 種類だけでできているということになる。他の4種類のクォークは、存在が不安定なので、より安定なアップとダウンに変身して消えてしまい、実験室で作り出しても直ぐ消えると言う。
 原子核を構成する陽子は、大きいエネルギーを担う2個のアップクォークup quark(u)と1個のダウンクォークdown quark(d)、さらに小さいエネルギーを担うクォークと反クォーク、そしてこれらのクォークを強い相互作用で結びつけるグルーオンgluonという素粒子で構成されている。つまり、グルーオンはクォークを結びつけることで原子核を構成する重要な役目を果たしている。
原子核を構成する陽子は、大きいエネルギーを担う2個のアップクォークup quark(u)と1個のダウンクォークdown quark(d)、さらに小さいエネルギーを担うクォークと反クォーク、そしてこれらのクォークを強い相互作用で結びつけるグルーオンgluonという素粒子で構成されている。つまり、グルーオンはクォークを結びつけることで原子核を構成する重要な役目を果たしている。クォークの識別記号としての「アップ」と「ダウン」には、「上」や「下」といった位置や方向に関わる意味合いは まったく含まれていない。それは、対となる性質と機能をもった素粒子の 片方に「アップ」、もう片方に「ダウン」という 単なる識別記号を与えたに過ぎない。陽子と中性子を構成する最も基本的な3つのクォークが 、2種類一組であることを表現したに過ぎない。
陽子や中性子が3つのクオークからなるのは、「アップクォーク」が+2/3の電荷を持ち、「ダウンクォーク」が-1/3の電荷を持つからである。つまり陽子の電荷をクオークの電荷で計算すると、2×(2/3)+(-1/3)=+1となり、中性子の場合では、(2/3)+2×(-1/3)=0となり辻褄が合う。
全ての粒子は、地球の自転に似た「スピンspin」と呼ばれる粒子の「向き」を表す固有の性質を持っている。このスピン(向き)が、素粒子間の反応や素粒子の崩壊を支配している。しかも、陽子の向きは、陽子内部のクォークの向きの合計で決まる、とかつては考えられていた。しかし、陽子の向きに対してクォークの向きを合計すると全体の20~30%に過ぎないことが判明した。
スピンspinとは、素粒子が自転する向きを言うのだが、素粒子におけるスピンとは、 個々の素粒子に存在する固有の運動量であり、確かに、素粒子の種類によって、スピンの変化のあり方がパターン化されているようだが、同じ種類の素粒子でも、あるいは、全く同一の素粒子ですら、 条件が異なれば、まったく異なるスピンのあり様が観測されている。
「強い力」は、電磁気力の 100 倍程の大きさを持つ最も強い力なので、この名前が付けられた。「強い力」を媒介する力の粒子グルーオンは、電荷はゼロであり、質量も理論的にはゼロである。ただ、原子核内の陽子同士は正の電荷を持つため電磁的な反発力が働き、しかも電荷を持たない中性子が原子核内に留まるためには、電磁力とは別の力が働かなければならない。しかし、「強い力」の及ぶ範囲も、原子核の内部くらいの範囲に限られるから、電磁力より強いからと言って、日常生活では感じられない。
1978年、電子と陽電子の衝突実験により、グルーオンが存在しなければ観測される事がない3つの粒子ジェットを伴う崩壊が観測されたことにより、グルーオンの存在が実証された。この実験では3つのジェットそれぞれが1個ずつのグルーオンに対応する。翌年の1979年には、2つのジェットはクォーク、1つのジェットはグルーオンという、グルーオン単独の事象も観測されている。 しかし、グルーオン自体が「強い力」を持ち、クォークを結びつけて、陽子や中性子 を作り、また原子核内における陽子同士の間で生じる電気的な斥力にまさり、中性子とともに原子核を保持し続ける。
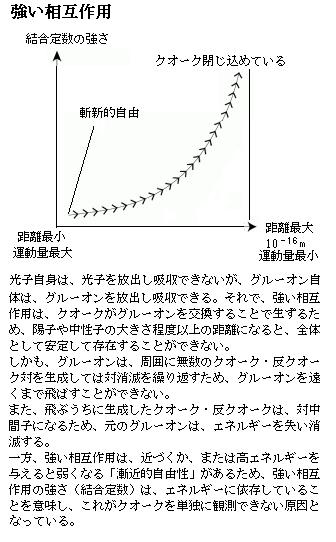
グルーオン自体の「強い力」は、距離が離れるほど強くなるが、それも核子(陽子・中性子)の大きさを超えると「強い力」は、閉じこめられる 。言わば、「強い相互作用」は、クオーク間の距離が小さくなると、グルーオンを交換する運動量が高くなることで、逆に弱くなる「漸近的自由性」と呼ばれる特性があり、一方、距離が大きく離れると相互作用が強まり、クオークを単体で取り出すことを困難にする特有の反応を示す。「強い力」の到達距離は、グルーオンが質量を持たないにもかかわらず短いため、日常では感じることができない。
例えば、電子は、その電荷を通じて電磁気力を感じるが、クオーク間では、「グルーオン」と言う質量ゼロの粒子の交換を通じて「強い相互作用」を生じさせると考えられている。「強い相互作用」の到達距離は10-16mと非常に狭いが、その力は非常に大きい。弱い力の3桁以上大きな力で、クオークを閉じ込めている。この力は紐のようなもので、ある距離に達すると切れるが、切れると双方の切り口にクオークが現れるようだ。
原子核ではクォークやグルーオンといった素粒子が、ある法則のもとで結合していると理解されている。顕微鏡でさえ見ることができない、そんな途方もなくミクロな世界の事が、なぜ「分かる」か言えば、物理の研究者は、目には見えなくとも、あらゆる実験データの積み重ねから、素粒子のふるまいを統一的に説明できる理論体系を作り、素粒子の世界を解明しようとしている。その理論体系を「模型」と呼ぶこともある。クォークとグルーオン、電子とニュートリノなどの相互作用を解き明かした集積を「素粒子標準模型elemental particle standard model」あるいは「素粒子標準理論」などと言う。
β崩壊とは、原子核からベータ線(電子)が放射される現象で、弱い力によって起きる原子核の放射性崩壊であり、原子核中の中性子が、電子と反電子ニュートリノを放出して陽子に変わるβ-崩壊と、陽子が陽電子と電子ニュートリノを捕獲して中性子になるβ+崩壊とがある。さらに、β崩壊の例として参考になるのが、水素の同位体である。1個の陽子と2個の中性子を核子とする三重水素が、中性子が多すぎて不安定であるために、このうちの1つの中性子がβ-崩壊を起こして陽子となり、陽子2つに中性子1つのヘリウム3となる。この現象では、中性子が陽子に変わっただけだから、核子の総数は変化しない。質量数が、反応前後で同じ3であることにかわりはないが、原子番号は、陽子が1つ増えるために、ひとつ上がって水素の1からヘリウムの2へ原子番号が変わる。
また、中性子には電荷がなく、陽子の電荷がプラス、電子の電荷がマイナスであるから、反応の前後では電荷の総量レベルでは変化していない。この放出された電子、あるいは、放出された電子が飛んでいる状態を、「β(ベータ)線」と呼び、この現象を「β崩壊」と呼ぶ。
これまですべての物質の元であると考えられてきた原子は、実は宇宙のたった4%に過ぎない。宇宙の大部分は「暗黒物質」や「暗黒エネルギー」など、まだ正体のわかっていないものからできている。
地球に引っ張っている重力は、すべての素粒子の引力、即ち万有引力として働く。その重力子は質量を持たないので、遮られることなく無限遠まで作用し、地球・太陽・銀河系などの天体の運行をつかさどり、巨大な宇宙の構造を作り出している。
アインシュタインは、光の電場や磁場の振動が、波のようにして伝わっていくように、重力も波のように伝わっていると予言し、これは重力波と呼んだ。重力をチャージするのが質量、よって重力は質量に比例する。重力波で観測できるようになると、宇宙を「見る」新しい窓が開けることになる。宇宙には光で見えないものも数多くある。それが重力波なら見えるようになる可能性がある。それにより宇宙が生まれたときの風景が見えてくるかもしれない。重力波観測に大きな期待が寄せられている。
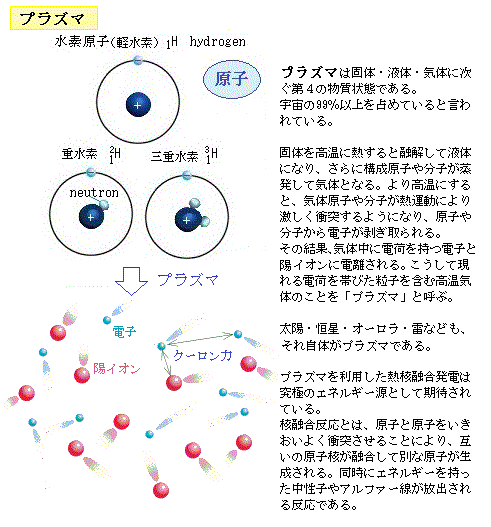 プラズマとは
プラズマとは 温度が上昇すると、物質は固体から液体に、液体から気体にと状態が変化する。さらに、気体の温度が上昇すると気体の分子は解離して原子になり、さらに温度が上昇すると原子核のまわりを回っていた電子が原子から離れて、正イオンと電子に分かれる。この現象を電離と呼ぶ。電離によって生じ た荷電粒子を含む気体をプラズマと呼ぶ。
原子の中心が原子核、原子核の周りをまわっているのが電子と言う。原子核はプラスの電荷を、電子はマイナスの電荷を帯びている。本来、イオンionとは、1個以上の電子を失った原子(正イオン・陽イオン・カチオン・正電荷)や、1個以上の電子を新たに獲得し原子(陰イオン・負電荷)を言う。化学の用語としては「プラスイオン」や「マイナスイオン」のような用語は曖昧な部分があるので使われない。「陽イオンpositive ion」または「陰イオンnegative ion」と言う 。
頻発する太陽の表面で起きる大爆発を「太陽フレアsolar flare」と呼ぶ。大きな黒点のまわりでも、時々、起きる現象である。太陽フレアは黒点の活動と大きな関係があり、黒点周期の極大期には、大黒点や黒点群の近くで毎日のようにフレアが起きる。太陽の表面には、コロナcorona(太陽の光環)と呼ばれる100万℃以上の温度の、密度の低い薄い大気がある。このような超高温では、気体が電子と正イオンに電離したプラズマ状態になっており、太陽の重力でも、このコロナガスを繋ぎ止めることができない。
フレアは黒点の磁場が変化するとき、そのエネルギーが周りのガスに伝わって起きる。太陽フレアによるガスからは、電波やX線のほかに、電子や陽子などの電荷をおびた素粒子(プラズマ)が飛び出す。X線やイオンや電子などの素粒子は地球に10分から1〜2日後に到着して、電離層や地磁気を乱して、電波通信が妨害されるデリンジャー現象dellinger effect(アメリカの物理学者 J.デリンジャーDellingerが 1935年に発見した) や磁気嵐magnetic stormを引き起こす。太陽風solar Winds(たいようふう;プラズマの流れ・コロナガスの噴出)と呼ぶ。また、オーロラの活動も活発になる。
自然界には、地球のエネルギーの源である太陽、水素原子の陽イオンと電子を主成分とする太陽風、地球を取り巻く電離層、極地の空を彩るオーロラ、真夏の積乱雲から走る稲妻など、様々な形のプラズマが存在している。太陽風に含まれるコロナのガスは、温度が100万度以上にもなるため、水素原子は陽イオンと電子に分解している。その陽イオンと電子を主成分とするコロナガスは、太陽から放出され、通常、惑星間空間を毎秒300-800kmの速さで吹いている。太陽から吹き出されたエネルギーの高い荷電粒子の中には、プラズマの他に、ヘリウムや酸素ばかりか、シリコンや鉄など重い原子のイオンが数パーセントほど混じっている。
また夜空に無数に散りばめられた数々の恒星の内部や、加えて星々の間の空間にも希薄なプラズマが広がっている。宇宙を構成する物質の99%以上がプラズマであるといわれている。太陽風の届かない惑星間のプラズマは、密度も温度も低いが、相対的にその量が非常に多いため、その宇宙空間にある物質の99.9 % 以上がプラズマであると言われている。 地球上では粒子密度が高いため電離しにくいが、高度が増すにつれて電離する割合が増加する。それは太陽からの紫外線やX線により電離されることが多い一方、粒子密度の減少により再結合によって中性原子neutral atom(イオン化していない原子)に戻る機会が減ることによる。そのため高度 100 km あたりでプラズマの密度が極大になり、電離層を形成する。高度約 300 km 以上の領域は磁気圏と呼ばれ、さらに電離しやすくなる。宇宙空間となり粒子密度が減少するため電子密度はゆるやかに減少し、磁気圏の外側の境界は、太陽風と地球磁場との釣り合いで保たれている。
プラズマには磁力線を閉じこめる性質がある。太陽風は、太陽の磁力線をも惑星間空間に放出している。つまり、太陽風は磁気と電気を帯びたガスの流れなのである。
 電気の正体は、現代の物理学では金属元素の電子(自由電子)であると言う。この特定の原子間の結合に束縛されず自由に動き回れる自由電子free electronが移動することにより、電気エネルギーが発生する。電流は、マイナスの電荷を持つ電子が原子の中から飛び出して移動することで発生する。マイナスの性質を有する電子は、プラス極に引き寄せられる。この電子の移動を電流という。電流はプラスからマイナスに流れていると思われているが、実はマイナスからプラスに向かって流れている。このような誤りは、避雷針を1,753年に発明したアメリカ合衆国の創立者の一人のベンジャミン・フランクリンの勘違いから始まった、と言われる。
電気の正体は、現代の物理学では金属元素の電子(自由電子)であると言う。この特定の原子間の結合に束縛されず自由に動き回れる自由電子free electronが移動することにより、電気エネルギーが発生する。電流は、マイナスの電荷を持つ電子が原子の中から飛び出して移動することで発生する。マイナスの性質を有する電子は、プラス極に引き寄せられる。この電子の移動を電流という。電流はプラスからマイナスに流れていると思われているが、実はマイナスからプラスに向かって流れている。このような誤りは、避雷針を1,753年に発明したアメリカ合衆国の創立者の一人のベンジャミン・フランクリンの勘違いから始まった、と言われる。
1897年、イギリスのトムソンによって電子の正体が明らかになった時には、誤った説がすでに世界中に広く浸透していた。この矛盾によって電気の説明や計算に支障が生じることはないため、今日では「電子はプラスの方向に流れ、その反対の流れを電流とする」という約束事に繋がった。
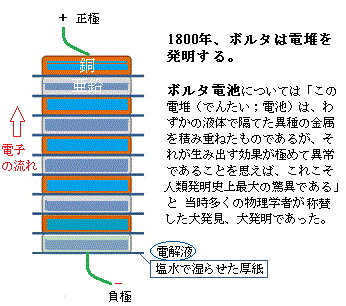
二種類の金属単体を電解質水溶液に入れると電池ができる。これはイオン化傾向(単体の金属の原子が、水または水溶液中で電子を放出して陽イオンになる性質)が大きい金属が電子を放出して陽イオンとなって溶け、イオン化傾向の小さい金属へ析出する。
1,800年頃にイタリアの物理学者であるボルタによって発明されたものが「ボルタの電池」である。ボルタの電池の構造は、電極に銅板と亜鉛板を使い電解液に塩水や希硫酸を使った。つまり、銅と亜鉛の板に塩水で湿らせた厚紙をはさみ、これを直列に接続すると数に比例して効果が高まり、またライデン瓶のように一回の放電で消耗しないことも確認された。ボルタの電池は電気が発生すると電極に変化が起こり、銅板は色が黒くなってくる。そして、亜鉛板の方は電解液に溶けていってだんだんと小さくなっていく。そのため銅板の方をプラス(正極)、溶け出して小さくなって行く方をマイナス(負極)、と考えた。その際、電気の流れる方向(電流)が、プラス(正極)からマイナス(負極)に流れると思い込んだ。
19世紀の終わり頃に電子(自由電子)が発見された。その電子がマイナスの電荷(負電荷)を持っていた。その時点で初めて、電子がマイナスからプラスに流れる事が分かった。イオン化傾向の大きい方の金属を負極(ふきょく)という。イオン化傾向の小さい方の金属を正極(せいきょく)という。
電子が流れ出す電極を負極(-極)、電子が流れ込む電極を正極(+極)と言う。つまり、負極から正極に電子が流れる。
亜鉛は銅よりもイオン化傾向が大きい、つまり、酸化されやすい性質があり、物質が酸化されると、電子を失う。亜鉛は酸化されて、亜鉛イオン・Zn2+になり、そのときに、電子e-を放出する。亜鉛から出た電子は、導線を通って銅板に移動する。その時、溶液中の銅イオンCu2+が、その銅板の表面で電子を受け取ることで、Cu2+が還元されて、銅Cuになる。負極・正極のそれぞれで、酸化還元反応が起こり、電子の流れが生じる。それが電気エネルギーになってモーターなどを動かす。
ある物質が帯電しているとき、その帯電の大小の程度を電荷electric chargeという。様々な物質をいろいろな方法で帯電させた結果、電荷には、帯電した2個のもの同士を近づけた時に引っ張り合う「引力」が働く場合と、反発しあう斥力が働く場合の2種類がある。このような、帯電している物体に働く力を静電気力という。ここで観察される静電気力を、クーロン力と呼ぶことがある。2個の電荷同士がおよぼす力は同じであり、従って作用・反作用の法則に従っている。
イオン相互作用は、「クーロンの法則Coulomb's law」と呼ばれる。この法則はシャルルド・クーロン(Charles Augustin de Coulomb)というフランスの物理学者が発見した。
1つの分子上にある電荷を帯びた基は、別の分子が持つ逆の電荷を帯びた基を引き付ける。このイオン相互作用ionic interactionや静電気的相互作用electrostatic interactionのエネルギーは、クーロンポテンシャルエネルギーCoulomb potential energyで表される。
E = k q_1 q_2 / D r
という2つの電荷の積に比例し、その距離rに反比例する力が働く。この力をクーロン力(静電気力)と言う。静電気による電荷同士に働く力である。帯電していない状態を電気的に中性と言う。
電荷の単位はクーロンである。クーロンの記号はCである。クーロン法則によると q_1 , q_2 という2個の原子に電荷があるとき、その2つの点電荷の距離がr(Å単位)である。
Dは比誘電率relative permittivity(pə`ːrmitívəti;誘電率)で、介在する溶媒となる物質(誘電体)の誘電率と真空の誘電率の比、その誘電体により様々な値をとる。誘電率は物質内で電荷と、それによって与えられる力との関係を示す係数である。各物質は、サイズや体積に依存しない固有の誘電率を持ち、この値は、外部電場からの静電気力を受けて誘電体を構成する原子、あるいは分子がどのように応答するかによって定まる。実験によってその値は決定されている。比誘電率は、クーロン力を低下させる。
Kは比定定数である。「真空中での」と断っている通り、電荷を取り囲む物質の種類ごとにkの値は異なる。kは物質に固有の値なのだ。慣例により引力が働く場合にEは負の値を持つとする。
プラズマと通常の中性気体との大きな違いは、荷電粒子の間にクーロン力が働くことでる。中性気体では2つの粒子が極めて接近したときだけ、粒子間に力 が働くのに対して、クーロン力ははるかに遠方まで力が及ぶ。そのため、1つの粒子の運動は多くの粒子に影響を及ぼし、中性気体には見られない様々な現象が現れる。プラズマ中の荷電粒子は、原子に束縛されていた電子がエネルギーを得て電離することによって生じる。そのため、粒子のもつ運動エネルギーは粒子間に働くクーロン力のポテンシャルエネルギーよりも大きいのが普通である。また、粒子損失がなければ、プラズマ中の電子のもつ電荷の総和と正イオンのもつ電荷の総和は、符号が逆でも大きさは等しいので、全体としてほぼ電気的中性である。電子ビームやイオンビームのように電気的中性条件を満たしていない荷電粒子系は、通常プラズマとは呼ばない。
われわれの生活空間にも、正の電荷を持つ原子と負の電荷を持つ電子がバランスよく手を取り合って存在している。しかし、空気中には負の電荷の電子が不足した状態であるため、他のものからその不足した電子を奪い取ろうとする物質がある。そのような物質を酸化物質といい、活性酸素などがこれにあたる。人でいえば、細胞を酸化し老化させる物質でもある。
アインシュタインの公式
E=mc2 (エネルギー E = 質量 m × 光速度 c の2乗)
「質量の運動はエネルギーに変わる(質量とエネルギーの等価性)」、さらに「質量には膨大なエネルギーが閉じ込められている」ことを世界一有名な、しかも簡単な方程式で示した。従って重力は全ての粒子で働く。しかし、地球全体が紙を引っ張る重力よりも帯電した下敷きが紙を引っ張り上げる静電気力の方が強い。しかも、素粒子の質量は非常に小さい。 それがアインシュタインの公式に従えば、超新星爆発までも起こし得る。
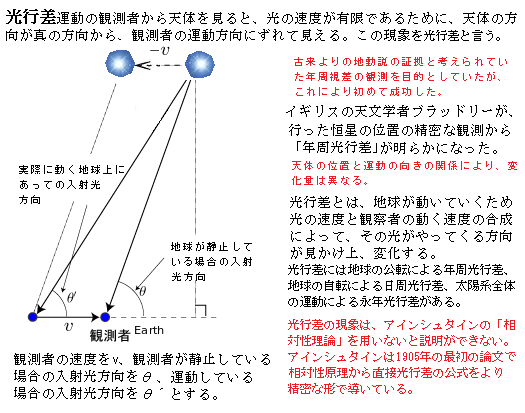 E=mc2、このアインシュタインの式は、自然科学の様々な基本方程式の中で最も有名な方程式であるが、アインシュタインは、全く新しい物理法則を創案したのではなく、質量保存の法則や運動量保存の法則、そして光行差aberration
of light(運動している観測者から天体を見ると、光の速度が有限であるために、天体の方向が真の方向から観測者の運動方向にずれて見える。この現象を光行差と言う)でさえ取り込み、相対論を提案する前からの古典的な法則を複合し、かつて誰もなしえなかった大きな転換的発想を提唱した。
E=mc2、このアインシュタインの式は、自然科学の様々な基本方程式の中で最も有名な方程式であるが、アインシュタインは、全く新しい物理法則を創案したのではなく、質量保存の法則や運動量保存の法則、そして光行差aberration
of light(運動している観測者から天体を見ると、光の速度が有限であるために、天体の方向が真の方向から観測者の運動方向にずれて見える。この現象を光行差と言う)でさえ取り込み、相対論を提案する前からの古典的な法則を複合し、かつて誰もなしえなかった大きな転換的発想を提唱した。例えば、太陽の中心は約2,400億気圧・約1,400万度の超高圧・超高温状態で、それは他の星の中心でも同様の反応が起こっているいるのだが、そこでは4個の水素が1個のヘリウムに変換する核融合反応が生じている。
ヘリウム原子1個の質量は、4個の水素原子の質量を合わせたものよりも、僅かに小さい。言い換えれば、4個の水素原子の質量全体の約2.9%、水素原子1個当たりに換算すると、0.7%だけ少ない。つまり水素がヘリウムに変換する核融合により0.7%の質量が、アインシュタインの式通りに、エネルギーに転化されるのである。
つまり太陽の中心では、毎秒6億トンの水素がヘリウムに変わる。それは
6億トン×0.7% = 420万トン
という物量が、とてつもないエネルギーになり転換されている。
当然、とうに大爆発をしているはずだ。それなのに、太陽や星の中心で起こっている核融合は、極めて安定している。
水は0℃より低い温度では氷(個体)、0℃から100℃の間は水(液体)、そして100℃より高い温度では水蒸気(気体)になる。その温度の違いがあっても、どんな物でもこのように3種類の状態になる。さらに「第4の状態」がある。温度をさらに上げて、だいたい1万℃以上にすると、原子の中の原子核と電子がはなれて勝手に動くようになる。この状態を「プラズマ」と言う。原子力発電の核融合反応では、燃料には重水素や三重水素といったガスを使う。高温状態にして、分子や原子の状態からプラズマの状態にまずする。
外界から熱の供給が無い状態で、気体が膨張することを、断熱膨張と呼ぶ。 反対に外界から熱の供給が無い状態で、気体が圧縮されることを、断熱圧縮と呼ぶ。気体を断熱膨張させると気体の温度は下がり、反対に気体を断熱圧縮すると、気体の温度は上がる。
核融合反応は、軽い原子核同士が融合し、より重い原子核に変わることを言う。融合した時に、とてつもない大きなエネルギーが出る。太陽も核融合で燃えている。太陽は3/4が水素(H)からできている。太陽の中心では、約2,400億気圧・約1,400万度の超高圧・超高温状態にあり、さらに高い密度(鉄の20倍と粒子の数が多い)の中で、水素が核融合反応を起こしてヘリウム(He)となり、その際の膨大なエネルギー(熱や光)を出している。太陽は、地球の約33万倍もの質量を持つ巨大なガスのかたまりである。巨大であるため、核融合反応で水素が消失されるまで50億年もかかると言う。地球は、太陽と比べれば格段に小さく、太陽のような高い密度を作ることができないので、水素で核融合反応を起こすことはない。
それでも、太陽や巨大な星々の中心で起きている核融合反応は、極めて安定し持続をしている。つまり中心の核融合が暴発しかけて、温度が急上昇すると、外界から熱の供給が無い状態での気体の膨張となり、つまり断熱膨張による温度の低下が生じ反応は落ち着く。その結果、逆に温度が下がり過ぎると、外界から熱の供給が無い状態で、気体が圧縮される断熱圧縮で温度が上がる。この断熱膨張と断熱圧縮の繰り返しで核融合が持続される。
ビッグバンによる宇宙創成期には、その重力がその巨大な超々高エネルギーとして働く。その高温・高密度の激しい高エネルギー重イオン衝突の過程から鉄よりもさらに重い重元素が一気に生成され、それらの重力エネルギーが一挙に解放される超新星爆発により宇宙へ吹き飛ばされていく(電子の過剰あるいは欠損により電荷を帯びた原子が「イオン」で、特にヘリウムより重い元素のイオンは「重イオン」と呼ぶ)。地球を形成している元素すべてが、太古に幾つもの超新星爆発による生成物である。
超新星爆発によって周りが吹き飛んだ後の中心には、中性子の塊が残る。中性子星の誕生である。中性子星の密度は、(2-7) × 1014 g / cm3は、通常の原子核の密度は、~2.5 × 1014 g / cm3、中性子星の平均密度は、原子核の1~3倍、想像を超えた領域で、温度や磁場によって固体または液体状態となっている。
中性子星の質量が大きくなっても、その密度の硬さで重力による収縮圧に対抗できるが、やがて圧倒的な圧力により縮むとブラックホールとなって崩壊する。重力は自然界にある4種類の力の中では一番弱いが、膨大な質量となれば無限に強まっていく凄さがある。アインシュタインの公式、E=mc2のエネルギーは、無限大に近い数字になる。
ストロマトライト
細胞の多様性が生物の多様性に繋がるが、2016年8月31日付けの学術雑誌NATUREに「世界最古」とされる生物化石の発見が発表された。その化石は、グリーンランド南西部のイスア地域の37億年前と推定される地層から見つかった。今回、発見されたのは、単なるバクテリアの個体化石ではなく「ストロマトライトStromatolite」と分析されている。
ストロマトライトとは、主にシアノバクテリアcyanobacteriaが作る構造体である。この生物グループは基本的に緑色をした光合成を行う多数の細菌類であるが、この藍色細菌cyanobacteriaには、細胞から菌糸を伸ばして固体表面を滑走運動する種があり、細胞から分泌粘液を出し、それによりコロニーを形成する。また、一部のシアノバクテリアは、多くの個体が密集し土砂などを利用して大きな構造物を作る。
英名ストロマトライトStromatoliteとは、ギリシャ語のstroma+lithosから派生し、ギリシャ語のstromaは層の意味し、lithos はrock「岩」を意味する。直訳すると「層状の岩」である。イスア地域で発見されたストロマトライトは、小さな構造物で、雪解けによって露出した地層から発見された。このイスア地域には、一ヵ所だけで、タービダイトturbidite(混濁流によって運ばれた海底堆積物、砂岩・泥岩の互層を特徴とする)の露頭が存在する。タービダイトは明確な深海底の堆積物である。38億年前の海溝から混濁流(乱泥流)が、大きなエネルギーを持ったとなってここにタービダイトを堆積させた。
インド洋に発達するベンガル海底扇状地では、約2,800km にわたって混濁流の痕跡がある。これは、北海道から沖縄までの日本列島の全長にほぼ匹敵する。混濁流は、驚くほど長距離を流れ下っている。 ベンガルとインダスの巨大な海底扇状地には、ヒマラヤ山脈の上昇に伴った膨大な量の堆積物が中新世以降供給され続けている。
混濁流が、これほどの長距離を力を増しながら流れを持続できるのは、流れの侵食・自己加速作用によるものである。流れる混濁流の流速が十分に速いと、流れの中にある渦が海底面の堆積物を巻き上げて、懸濁する浮遊堆積物の濃度を増加させる。濃度の増加が、流れの密度の増加になり、その流れは加速され、さらに底面の堆積物を侵食する能力が増す。
混濁流が十分な流速・濃度で発生すれば地形だけを見れば陸上のV 字谷とよく似ている。日本近海では,天竜川の沖合に発達する天竜海底谷や、釧路川の沖合に発達する釧路海底谷などの海底谷は、直線的な形状が、やがて蛇行していくこともある。
混濁流とは、重力によって駆動される密度流の一種である。水中では浮力と水の粘性が働くため、ひとたび海中に砂や泥が充満した懸濁が生じると、堆積物はなかなか沈降しない。そ して、いったん生じた懸濁液(粘土を含んだ濁水のように、液体中に顕微鏡で見える程度の粒子が分散しているもの)は、周囲の流体よりも浮遊している堆積物の分だけ密度が高く、その分増した重力に引かれて斜面下方向へと流れ始める。これが混濁流である。
侵食と加速を繰り返して、巨大な混濁流に成長する。この過程を混濁流の自己加速と呼ぶ。これが、わずかな懸濁物から始まった流れが巨大な海底谷・海底扇状地を形成する原因となる。混濁流にとって、海底面の堆積物はいわば途中で補充される燃料となる。底面の堆積物から位置エネルギーを補充して、混濁流は極めて長い距離を流れ下る激流にもなり得る。
流れが底面を侵食しながらしだいに加速する。また下流地点ほど混濁流の流速が速くなる。
生物の進化を探究するためには、宇宙や地球の物理的な大変動を契機に生命体が誕生し、主としてタンパク質やその他の化学分子、生化学的な反応径路が、時の経過とともに器官・機能を構成していく一方、それを変えていくあり様を解明していく必要がある。
その関係で最も基本となるものが相同homology(性;ホモロジー)関係であり、2つの分子が共通祖先に由来していれば「相同」と言う。相同な分子をホモログhomolog(相同遺伝子)と言うが、これは2つに分類される。
同種間にあるホモログはパラログparalogと呼び、それらの多くは精緻な生化学的機能が異なっている。異種間で見られるホモログがオルソログorthologであり、それらの機能は意外にも、極めて似ているか同一である。
となれば、分子間の相同性を解析すれば、それらの機能に関わる情報だけでなく、進化の過程にまで及ぶことになる。もし、新たにDNAに配列決定されたタンパク質が、既に特性が解明されているタンパク質と相同であれば、そのタンパク質の生化学的な機能の解明に極めて参考になる。相同性は、多くの場合、塩基配列やアミノ酸配列に統計化された類似性により見出され、その立体構造を比較することで通常証明される。
目次へ
1929年、アメリカの天文学者ハッブルが、観測により遠くの銀河ほど地球から速く遠ざかっていることを発見した。これが「ハッブル法則」で、宇宙の膨張を意味する。
宇宙のはじまりは138億年前、超高温・超高密度の火の玉の急膨張により誕生したとされている(ビッグバン)。観測の結果、銀河が遠ざかっていることが明らかになり、宇宙の膨張が解明された。
宇宙誕生以前は、現在の宇宙の全エネルギーが圧縮され、光さえ脱出することができない状態であり、それを「宇宙のブラックホールblack hole」と表現する。
アインシュタインは、ブラックホールでは、重力は無限の密度を持つと説く。その初期の宇宙は全てのエネルギーが一点に集中していることに なり、誕生直後の宇宙は、想像を絶するほどの約1,000億度の超高温で、しかも高密度に凝縮されていたことになる。この状態からの爆発を、「インフレーション期」と呼ぶ。
ビッグバン直前の「宇宙のはじまりの瞬間」をとらえたのが「インフレーション理論inflationary cosmology」である。1981年に、東京大学の佐藤勝彦名誉教授が発表したインフレーション理論は、宇宙誕生の初期、10-36秒後から10-34秒後という超短時間に、極小だった宇宙が急膨張し、その際に放出された熱エネルギーがビッグバンの火の玉になった、とする理論である。米国のアラン・グース(A.H. Guth)が、ほぼ同時期に同じような理論を提唱している。
インフレーションほどの急膨張であれば、巨大な星の爆発など、質量を持った物体が運動するときに生じる「時空の歪み」を光速で伝える「重力波」が生じる。つまり、物質密度の揺らぎが、時空の揺らぎとなって重力波が生成されるからである。地球に届く重力波は極めて微弱で、直接の観測は困難だと言う。
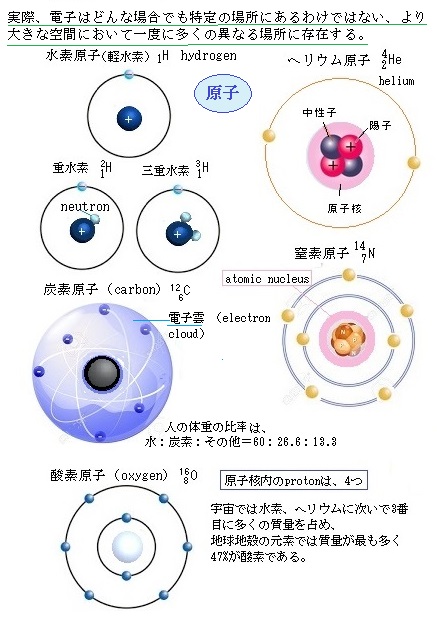 その膨張は光の速さを超えたと言う。その後も宇宙は膨張し続ける。膨張にともなって徐々に冷えていき、「インフレーション期」から約38万年が経過すると、約3,000K(2,727℃)まで冷えた宇宙では、最初に電子やニュートリノなどが生成され、次に陽子が生成された。電子が陽子に捕らえられ最初の原子・水素H(原子番号1,中性子を含まない)ができた。水素は宇宙で最も豊富に存在する元素であり、宇宙の質量の3⁄4を占める。水素は互いの重力で引き合い、そのため至る所に集合し、その水素を集めて恒星となり、水素原子は、自身の重力で密度の高い所へ収縮していき、密度が高くなればなる程加速的に密集し、内部の圧力と温度が際限なく上昇する。
その膨張は光の速さを超えたと言う。その後も宇宙は膨張し続ける。膨張にともなって徐々に冷えていき、「インフレーション期」から約38万年が経過すると、約3,000K(2,727℃)まで冷えた宇宙では、最初に電子やニュートリノなどが生成され、次に陽子が生成された。電子が陽子に捕らえられ最初の原子・水素H(原子番号1,中性子を含まない)ができた。水素は宇宙で最も豊富に存在する元素であり、宇宙の質量の3⁄4を占める。水素は互いの重力で引き合い、そのため至る所に集合し、その水素を集めて恒星となり、水素原子は、自身の重力で密度の高い所へ収縮していき、密度が高くなればなる程加速的に密集し、内部の圧力と温度が際限なく上昇する。この星の中心核では、全質量の圧力による高圧と、その重力エネルギーにより熱を発し高圧・高温になり、水素の原子核同士が融け合う核融合が点火され、新たなヘリウム原子が生まれてくる。例えば、軽くて燃えやすい水素の同位体である重水素と三重水素の原子核を融合させると、ヘリウムと中性子ができる。同時に、反応前の重水素と三重水素の重さの合計より、反応後にできたヘリウムと中性子の重さの合計の方が軽くなり、この軽くなった分のエネルギーが放出される。また、その重力によって自由に飛び回っていた素粒子のクォークquarkとグルーオンgluonが合体し、中性子や、陽子と中性子からなる原子核など様々な複合粒子を形成する。
クォークや電子が、物質を構成する一番小さい単位である素粒子と呼ばれるもので、クォークは全部で6種類ある。レプトン lepton(軽粒子)も全部で6種類あり、電子やニュートリノ neutrino がこれに含まれる。
なお、現在運転されている原子炉では、核分裂反応を利用している。核分裂では、ウランやプルトニウムなどの重い原子核に中性子を投入して軽い原子核に分裂させる。その際、軽くなった分だけ発生するエネルギーを原子炉で取り出して発電する。
ヘリウムの核融合が始まると、それによる膨大な発熱と重力による圧縮が平衡状態になり、しばらくは縮まなくなる。この際の大きなエネルギーが、恒星の輝きのエネルギー源であり、これが現在の太陽の状態である。
やがて水素が全部ヘリウムになると発熱しなくなる。再び重力による収縮が優勢になり、重力により縮む中心部では、圧力と温度が急上昇し、今度はヘリウムの核融合が点火される。核融合による膨大な熱エネルギーが収縮を抑えてヘリウムがなくなるまでこの原子核同士の核融合が続く。太陽より大きな恒星では、このようなプロセスが繰り返されて炭素・窒素・酸素などのより重い元素が次々と作られていく。この段階では、未だ重い元素は宇宙に飛び散ってはいない。
この反応は、いくら大きな恒星であっても鉄が形成されて核融合は終わる。原子番号が大きくなると、原子核同士の陽子は同じプラスの電荷を持つため、陽子を構成する素粒子の数が増えれば、互いの反発する力が大きくなるため、核融合が起こりにくくなってしまう。核融合を起こせる元素は、鉄(原子番号26)までが限界で、それより重い元素は核融合ではできない。
鉄はまた、最も結合エネルギーの大きい原子核なので核融合反応を起 こさない。元素の中で一番安定している。そのため融合や逆の分裂をするにしても、化学変化には常に熱エネルギーを必要とする吸熱反応endoergic reactionする。その反応は自発的に起こりえない。どの場合でも発熱どころか、周囲から熱エネルギーを奪うことになる。さらにニュートリノが、エネルギーを持ち去って逃げていく。やがて、核融合による発熱がなければ、巨大な恒星の圧倒的な重力による収縮力に対抗できない。
この状況下の巨大な恒星は、その重力による圧力で鉄の原子がどんどん縮む。間もなく、膨大な圧力で中心部にある鉄原子が潰され、遊離していた電子が原子核と一体になるほどに縮む。結果、原子の中の電子と陽子が合体して、中性子とニュートリノになる。
原子核の直径は、原子全体の直径の1万分の1以下しかない。星は一挙に内部に向かって凝縮する。それにより激しく落下する粒子の重力エネルギーが一気に解放されるため、膨大なエネルギーの瞬間的な集積となり、それが大爆発を誘発する。これが「超新星爆発」である。
この瞬間、地球上の人々には新しい星の誕生と見える。
恒星の進化は、基本的にはその質量 によって決まる。重い恒星ほど明るく輝くが、そのため短い一生となる。太陽の8~10倍より重い星は、最期に超新星爆発という大爆発を起こし、星の内容物を宇宙空間にばらまくとともに、中性子星やブラックホールといった高密度の天体を残す。ここ2,000年の間に肉眼で見えたことが記録されている超新星は8例ある。
巨大恒星の最終末期に起こる壮大な「超新星爆発」による、この巨大恒星の生滅は、地球上から見れば星が誕生したと錯覚される。
「明月記」は、藤原定家が記す1,180年から1,235年までの日記で、天文現象に関する記録を遺す貴重な史料と評価されている。望遠鏡が無い時代に観測された超新星爆発の記録は世界に7件しかない。その内の3件が「明月記」に書かれている。
1,230年、旧暦11月4日に、定家が「この星鵬々(ほうほう;大いなる瑞兆の意を含む)として光薄し、その勢い小にあらず」と記 している。1,054年、平安の陰陽師、安倍一族が実際に観測したものを、安倍泰俊が調べて藤原定家に報告したことによる。定家は、建仁元(1,201)年、『新古今和歌集』の撰者の一人に任命されている。
それが、客星である「かに星雲(M1)」の965年前の姿である。おうし座の超新星の残骸で、中心には高速で回転する中性子星neutron star (パルサー)がある。パルサーの正体は、超新星爆発によって生まれた中性子星から発せられる放射状のビームで、光・電波・X線・ガンマ線などを周期的に規則正しく放射している。1.6m秒(1m秒は1/1,000秒)から8.51m秒と非常に短い周期で明滅する。超新星爆発は、大質量の恒星が最期に起こす大爆発で、明るい星のように見える。かに星雲(M1)でも、違った年に撮影した写真を見比べると今でも膨張しているのが分かると言う。かに星雲の超新星爆発でも、中心に中性子星が誕生している。
炭素より重い元素の起源は、恒星内部での核融合と超新星爆発が切っ掛けとなる。鉄より重い元素も、巨星の段階で一部は合成されるが、ウランより重い元素が合成されるのは超新星爆発のときのみである。膨大な質量を持つ中性子星の密度であっても、やがて「質量の運動はエネルギーに変わる」、さらに「質量には膨大なエネルギーが閉じ込められている」。
この物質と重力の関係を簡単に示すアインシュタインの公式
E=mc2 (エネルギー E = 質量 m × 光速度 c の2乗)
がその物理作用により、中性子星の驚異的な密度に起因する質量が重力となって働くため、膨大な質量を持つ巨星に作用する重力による圧縮に抗するすべもなく、やがてブラックホールとなり崩壊過程をたどる。超新星爆発の後の爆発噴出物は、星間空間に散乱する。
超新星爆発による爆発のエネルギーは、膨大な数のニュート リノを宇宙空間に飛散させる。地球から16万光年離れた大マゼラン星雲でおきた超新星爆発(SN1987A)にともなうニュートリノが地球に到来している。1,987年2月23日に、大マゼラン星雲中で発見された超新星SN1987Aによる爆発時に放出されたニュートリノが、世界最大の地下ニュートリノ観測装置の「カミオカンデ」で検出され、これが世界初の太陽系外天体からのニュートリノ観測となった。その時代ごとに観測不能の領域に果敢に立ち向かう理論物理学の研究成果を、確実に実証してみせたのである。
ニュートリノは、原子核を構成する極めて重要な素粒子でもある。1,998年、東大教授の梶田隆章博士らは、大気中に飛び交うニュートリノの観測から、長い距離を飛んできて地球の裏側に飛び込むニュートリノの数が、カミオカンデの検出器 の真上から降り注ぐニュートリノの数に比べて、約半分 しかないことを検証した。 これは、ニュートリノが飛んでいる間に別の種類のニュートリ ノに変身してしまう「ニュートリノ振動」という現象による事が明らかになった。地球の裏側に入ったミューニュートリノが地球内部を通過する間に、タウニュートリノ(ニュートリノには電子ニュートリノ、ミューニュートリノ、タウニュートリノの3種類がある。さらに、それぞれの粒子に対する反粒子も存在する)に変身するため、ニュートリノが減る現象として観測された。そのニュートリノ振動は、ニュートリノに質量があるときだけ起こ る現象である。いわゆる、ニュートリノ振動の発見は、ニュー トリノが質量を持つという決定的な証明となった。 2,015年、梶田隆章博士らによる実証実験の成果が、今後の理論物理学の研究に確かな論証基盤となり、その後の物理学研究に大きく貢献すると評価され、ノーベル物理学賞を受賞した。
原子核を構成する陽子には、大きいエネルギーを担う2個のアップクォークquark(u)と1個のダウンクォーク(d)、さらに小さいエネルギーを担うクォークと反クォーク、およびこれらのクォークを強い相互作用で結びつけるグルーオンgluonという素粒子で構成されている。
グルーオンは、「糊づける」という英語 glueに由来し、クォークを結びつける「のり」の役割をしている。陽子内部では、クォークと反クォークが共存し、対消滅と対生成の反応が生じている、と言う。
陽子と中性子の質量はほぼ等しく、電子の質量の約 1,800 倍であるため、原子の質量は原子核の質量にほぼ等しくなる。電子は原子の広がりを決めっている。電子は、単なる粒子ではなく、波の性質を持つ粒子として振舞う。そのため、原子核のまわりに存在する電子の位置と運動は特定することができない。その電子軌道は雲のように描かれることになる。
グルーオンはクォークを結びつける「のり」の役割をする素粒子であるため、陽子や中性子などの核子を作るばかりか、それらの核子を原子核として一体化する核力にもなっている。例えば、陽子が持つ電磁力は、すべてが同じプラスの電荷なので、その反発する力が、原子核を結合させるグルーオンの強い「糊づけ」の核力に勝れば、原子核は分裂してしまう。同じ電荷を持つ陽子同士の反発力の大きさは、クーロンの法則により距離の二乗に反比例する。原子核の領域は、原子や分子の半径が 10-10 m(100 億分の1m)位の、非常に小さな粒子であり、極論すれば距離が全く無いとまで言える素粒子の世界でもある。そのため陽子同士の反発力は絶対的に働く。中性子はその陽子間に挟まり、その電磁的な強力な反発力をゆるめ、核力でくっつきやすくする手助けをする。
中性子は原子核内では安定するが、原子核外に取り出されると15分程度で「陽子+電子+反電子ニュートリノ(素粒子)」の3つの粒子に崩壊(β崩壊)する。原子核の構成要素は陽子と中性子だが、中性子は電荷を持たないため容易に原子核に入れる。しかも、中性子は、陽子と電子が水素原子を形成する場合よりも更に密接に結合する。そのため重い水素の同位体が生まれ、質量数が2(原子核が陽子1つと中性子1つ)の重水素2H、質量数が3(原子核が陽子1つと中性子2つ)の三重水素3Hができ、その反応の物理化学の延長(星の燃焼)でヘリウム4He(原子番号2, 原子核が陽子2つと中性子2つ)ができる。そのためヘリウムの存在量は、水素に次いで宇宙で2番目に多いことになる。
例えば、三重水素3Hは、陽子が1つに中性子が2つ、中性子が多すぎて不安定である。このうちの1つの中性子がβ崩壊を起こして陽子となれば、陽子2つに中性子1つのヘリウム3(3He)となる(ヘリウム同位体)。この現象では、中性子が陽子に変わっただけで、核子の総数は変化しない。質量数は、反応前後と同じ3のままである。原子番号は、陽子が1つ増えるために、ひとつ上がって、水素の原子番号1からヘリウムの原子番号2になる。
このヘリウムがさらに核融合して、炭素・窒素・酸素、やがてカリウム、次にもっと重い鉄原子までが核融合で作られた。それまで散らばる電子により散乱させられていた光が、電子が陽子に捕らえられるため直進できるようになり宇宙を照らす。これを「宇宙の晴れ上がりclear up of the Universe」と呼ぶ。この時の光は「宇宙背景放射cosmic background radiation」として、現在でも観測されている。その観測結果から、宇宙のの晴れ上がりの時の物質の分布は、殆ど一様だったことが解明されている。
「β崩壊」により不安定な原子核を安定化させる。安定した原子核の領域は、陽子の数と中性子の数が同じであることが望ましい。それから外れるほど不安定さが増す。余りに大きく外れると、つまり陽子数と中性子数が余りに違いすぎると原子自体が崩壊する。言い換えれば、陽子が持つ電磁力と原子核を結合させる核力が均衡しなければ、原子核は分裂する。それが核分裂で、原子力発電や核兵器に用いられて厄介なことになる。不安定な原子核を安定化するために、中性子を陽子に変えて中性子の数を減らし、陽子の数を増やして、陽子と中性子の数を同数にし、アンバランスを解消させる。この現象を「β崩壊」と呼ぶ。中性子が陽子へと変わるときに、電子と反電子ニュートリノが1つずつ放出される。この放出された電子、あるいは、放出された電子が飛んでいる状態を「β線」と呼ぶ。
中性子 ⇒ 陽子 + 電子 + 反電子ニュートリノ
(中性子が多過ぎる場合は、電子を放出すれば陽子に変わる)
ニュートリノは、「ニュートラル=電気を帯びていない」「イノ=(イタリア語で)小さい」 という意味で、宇宙の中で光の次に多い素粒子でありながら、未だ謎の多い粒子である。ニュートリノは電子の仲間のレプトンという素粒子の一種であるが、電気的には中性である。レプトンは、原子核の中で働くグルーオンの強い核力の影響を受けない。太陽や星の中心では核反応にともなってニュートリノが発生している。やがて、このニュートリノの優れた透過力を利用して、太陽を含めて星の内部などを見ることができるのではないかと期待されている。
あらゆる物質は、その熱に応じた電磁波を出す(熱放射)。電磁波は熱い物質ほど波長が短い。宇宙の晴れ上がり時の光(約3000Kの物質が発する光)が、宇宙の膨張で波長が伸び約3K(-270℃)のマイクロ波になった。これを宇宙マイクロ波背景放射cosmic microwave background (CMB)という。この時期に放出され、約137億年かけて到達した光を、現在観測している。3,000K(2,727℃)あった温度は、約3K(-270℃)のマイクロ波になるまで下がったと計算になる。
セルシウス温度とは、「1気圧のもとで氷がとける温度を0℃、水が沸騰する温度を100℃」と定めた温度、絶対温度とは、「原子・分子の熱運動が殆どなくなる温度を“0”K」とする温度を言う。
セルシウス温度Celsius temperature と絶対温度の温度目盛りの幅は同じで、セルシウス温度t〔℃〕と絶対温度T〔K〕の関係は、
T=t+273 となる。
宇宙空間は、まったくの真空ではなく、非常に薄い水素やヘリウムのガスや塵のような物質が漂っている。これが原始星の原料になる。1cm³あたり約1,000個以上のガス分子が存在しているところを分子雲と呼び、この中でも特に星間物質が多く集まっているところで星が生まれる。
太陽の3/4が水素でありながら、地球の約33万倍もの質量を持つ巨大なガスの固まりである。中心部の水素の質量をヘリウムに変える核融合反応nuclear fusion reaction(軽い核種同士が融合してより重い核種になる核反応)で得られるエネルギーによって、重力から自身を支え続けている。中心部分の水素がなくなれば、核融合反応によるエネルギーが失われ、重力により中心部が潰れていくが、ある程度潰れたところで、ヘリウムを炭素や酸素に変える核融合が起こることで、引き続き核反応から得られるエネルギーで太陽は支え続けられていく。太陽の約10倍以上の質量を持つ大質量星も、中心部のヘリウムが尽きた後に潰れ始めるが、ある程度潰れたところで、炭素の核反応が起こるのに十分な密度と温度に達するため、再び核融合によるエネルギーで大質量星は支えられる。大質量星は、以降も重力により潰される前に、中心部が鉄で満たされるまで、次々とより重い元素を合成する核融合を起こし、そのエネルギーで星を支え続ける。
大きな恒星は、重力により、その中心に向かって質量に応じる大きな力が働く。その圧力が中心部における核融合反応を誘発し、その爆発力が外側に向かい、双方の力のバランスが保たれた状態で存続している。ところが、核融合反応が終わってしまうとこのバランスが崩れ、一気に内側へ収縮する。これを「重力崩壊」と言う。重力崩壊が起こると、中心に押し寄せてくるガスの圧縮の反動で、外側へ向かって、周りのガスを吹き飛ばす超新星爆発が発生する。
太陽の40倍以上の質量を持つ恒星の最期の爆発により、原子核からアルファ線やベータ線が飛び出した後、原子核に残された最も波長の短い、つまりエネルギーの大きい光、ガンマ線と呼ばれる放射線が凄まじい勢いで放出される。 銀河では絶えず超新星爆発が起こり、塵やガスの粒子となって銀河に漂っている。太陽系は今から約46億年前、銀河系の片隅で超新星の大爆発によって誕生した。途方もなく激しい衝撃波で飛び散った星間ガスや塵が、次第に集まり星間分子雲が形成され、この星間分子雲が凝縮を繰返して密度の高い塊となる。
星と星の間の空間に遊離する大量のガスやチリの殆どは水素とヘリウムで、他に炭素や窒素、酸素などの重い元素がチリとして混在する。この場所を「分子雲」と呼び、ここから無窮に近い星の一生がスタートする。この塊は重力の作用で収縮し、温度が上昇して、塊のあちこちに小さいガスの塊(原始恒星の卵)が誕生する。やがて、ガスの塊の周囲に水素1H、ヘリウム2He、炭素6C、窒素7N、酸素8Oなどを含んだ原始太陽系星雲が集合して前惑星系円盤が形成される。中心のガスの塊は、周囲の星間物質を取り込みながら、質量と密度を増しやがて核融合を起こし輝きを始め高温の天体になる。これが原始恒星の誕生である。太陽は、こうした原始恒星から進化した原始太陽の一つである。
原始太陽は、さらに星間物質を取り込み、質量と密度を増して高温高圧の天体へとますます進化していき、やがて 原始太陽の重力で、太陽系星雲は原始太陽を中心とする「原始惑星系円盤」と呼ばれるガス円盤を形成する。太陽の材料の残りである塵やガスからなる円盤中の塵は、互いの重力によって集まり、直径数kmほどの微惑星となる。微惑星はさらに互いの重力で衝突と合体を繰返して大きくなり、数百万年かけて数十個の原始惑星に成長し、しばらくは原始太陽から受ける重力に支配されて回転しながら外側へ展開していき、太陽系が誕生する。やがて原始惑星の軌道が、他の原始惑星の重力により、しばしば大きく乱され、原始惑星の軌道が交差したところで巨大衝突が起こる。原始惑星同士の重力により衝突と合体の繰り返しにより、約一億年で現在の太陽系の9個の地球型惑星に成長した。原始惑星同士の衝突は「巨大衝突」と呼ばれている。
目次へ
地球の誕生は、およそ46億年前、宇宙の始まりから既に100億年近く経っていた。地球は大きくなりその重力を増すとともに、ますます微惑星を引き付け、巨大な隕石になって地表に激突した。隕石は、毎日何千個と降り注ぎ、その度に地球は大きくなり、隕石には鉄はじめとする金属や岩石、また、水や二酸化炭素など様々な物質が含まれていた。地表に激突した瞬間、発生した熱のために鉄や岩石は溶け、水は水蒸気となって二酸化炭素などとともに原始大気を形成した。落下する微惑星はその衝突エネギーにより一瞬にして溶け、地表をマグマで覆っていく。
軽い原子核同士が融合して、より重い原子核に変わる時に、膨大なエネルギーを放出する核融合反応では、少量の燃料から膨大なエネルギーを発生させる。例えば、1gの重水素2H(原子番号1,質量数2)、三重水素3H(原子番号1,質量数3)燃料からタンクローリー1台分の石油(約8t)に相当するエネルギーが得られる。
重い鉄は下に沈み軽い岩石分は表面に集まる。繰り返し落下する微惑星の衝突によりやがて地表は煮えたぎるマグマオーシャンへと変化し、その深さは500㎞、温度は千数百度に達した。その衝突熱により微惑星中に含まれていた水分は一瞬にして蒸発し分厚い大気の層を作っていく。その厚さは500㎞に達した。
地球内部では、比重の大きい鉄が中心に沈んでコアを作り、その上をマントルが被った2層構造になる。宇宙の中の金属は、極めて含有量が少ない、その金属類から形成された地球は太陽系の中でも希少な存在と言える。
原始の地球の内部には、熱を保っていた放射性物質、ウランやトリウム、24種類の同位体が知られるカリウムなどの大量の放射性粒子が含まれていた。その放射性粒子が核分裂する際に熱を放出することで、すさまじい高温が続く。やがて放射性粒子の存在により、地球年齢ばかりか地球上の物質の年代測定ができるようになった。
厚く地表を覆った原始大気は、衝突で生じた多量の熱を閉じ込めてしまい、地表は千数百℃以上にもなり、岩石は溶け赤いマグマの海となり、文字通り地球全体が火の玉となる極端な様相であった。
やがて、地球を含め太陽系の成長もほぼ終わり、微惑星の衝突も減ってくると地表の温度も下がり始め、ちょうどその頃、大気中に漂っていた膨大な量の水蒸気が厚い雲となり、激しい雨となって地表に降り注いだ。この雨は何万年も降り続け、地球に広大な海をもたらした。更に地球表面が冷却すると、やがて地球表面から放出された水蒸気が雨水となって地表に溜まり海域を広げた。
水の起源については、初期の地質時代、盛んに突入してきた彗星の多くには、氷の塊となって地球に降り注いで、それが大量に含まれた水が元になったという、極めて有力と見られる説がある。水分子H2Oを作る原子の水素と酸素は、宇宙誕生の始期の核融合により作られている。地球に突入した原始的な隕石は、当然、太陽系と同じ組成を多く含んでいる。その中に大量の水を含み、以前から地球の水の起源として有力視されている。 地球上の水は、これらの隕石と小惑星と、同時に降着した可能性が高い。つまり、形成当時から表面に水を湛えた惑星だったことになる。
微惑星の落下が少なくなると、表面が冷えて固まり始める。オーストラリアのナリヤー地域の約30億年前の堆積岩から、〜44億年前の結晶化年代をもつジルコンzircon(ケイ酸塩鉱物;化学組成は ZrSiO4)と言う最古の鉱物粒子が見つかっている。ジルコンは非常に硬く化学的にも頑健な鉱物なので、浸食・運搬・続成作用diagenesis(地圧による圧縮や地熱による高温によって堆積物を固結するなど、粒子を再配列する物理的な圧密過程)を経てもマグマから結晶化した当初の情報が保持できる。ジルコンは、深成岩(マグマが地下深部で固結したものが深成岩。マグマの固結が地表か、浅い地下で行われたかによって、火山岩と深成岩に2大別される)の中に微小な結晶として広く産する珪酸塩鉱物ZrSiO4でダイヤモンドに次いで光学的分散が大きく、ファイアーと呼ばれる様々な色の光の反射で知られ、美晶は装飾用宝石として好まれる。
Zrは、「ジルコニウム」の元素記号、遷移金属に分類されるレアメタルの一つで、その酸化物は融点が高く優れたセラミックス材料として知られる。マグマの海などの高温下で酸化物や窒化物をはじめ、各種化合物となる。
35億年前以前の地質記録が極端に乏しいこともあるが、40~35億年前の岩石が占める表面積は、地球表面積の約0.002%しかない。これまでに見つかっている最古の岩石は、カナダのアカスタ地域に見られる40億年前の火成岩であった。
 陸には圧倒的に多いのが火成岩、その中でも、花崗岩とその変成岩である片麻岩(へんまがん)が一番多い岩石である。大陸は、高圧変成された岩石である花崗岩からできている。1,989年、アメリカの地質学者によって、カナダ北部 アカスタ川付近に存在する片麻岩の年代が測定され、約39億6,200万年前(誤差は300万年以内)という年代が報告された。年代は、片麻岩中のジルコンという鉱物に含まれているウランと鉛を分析することによって、決定された。
陸には圧倒的に多いのが火成岩、その中でも、花崗岩とその変成岩である片麻岩(へんまがん)が一番多い岩石である。大陸は、高圧変成された岩石である花崗岩からできている。1,989年、アメリカの地質学者によって、カナダ北部 アカスタ川付近に存在する片麻岩の年代が測定され、約39億6,200万年前(誤差は300万年以内)という年代が報告された。年代は、片麻岩中のジルコンという鉱物に含まれているウランと鉛を分析することによって、決定された。花崗岩や片麻岩は陸の地殻を構成する岩石、地球の誕生は約46億年前、その誕生から6億年経て、地球に陸が出現していたことを、アカスタの片麻岩は示している。
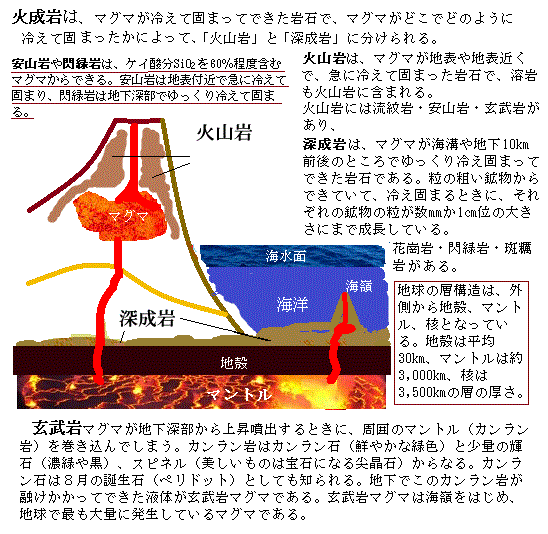
深成岩である花崗岩は、火山岩の流紋岩と同じく、ケイ酸分(SiO2)を70%前後含む粘っこいマグマからできる。
流紋岩はそれが 地表付近で急に冷えて固まるなど主に火山活動でできるのに対し、花崗岩はマグマが地下深部で数10万~数100 万年くらいかけてゆっくり冷えて固まってできる。流紋岩よりきめが粗い、平均して1mmより粗い。流紋岩は、マグマが直接冷えて固まったものよりも、高温の火山灰や火山礫などが急激に堆積し(火砕流堆積物)、それがそれ自身の熱で凝結してできたものが多い(溶結凝灰岩)。
これは、堆積作用でできた火砕岩だが、堆積岩ではなく、火山岩とされる。大量の花崗岩のマグマなど溶ける物質は、堆積物や大陸深部物質など、様々あるが、水が、そのような地球深部の物質に加わることによって、花崗岩のマグマが大量にできる。その水の供給源は海であり、その地球上の様々な変動の原動力は、地球の全表面を覆う十数枚の厚さ数10kmほどの岩盤plateの運動による。
プレートがぶつかる境界では、大西洋中央海嶺や東太平洋海膨などの海底山脈が形成され、その中に大きな裂け目が形成される。プレートテクトニクスplate tectonicsとは、海嶺を形成するプレートと呼ばれるものが、海底で冷えて、海溝で沈み込む、という一連の運動による地球の仕組みである。沈み込むプレートと共に、水を含んだ堆積物や岩石も沈み込み、潜るにつれて、圧力が上がる。やがて、水が絞りだされて、水は上昇し、上にある物質を溶かす。
高温高圧の条件に置かれた物質に、水が加わると、溶けはじめることがある。それで、今まで固体であったところに、水が加わるとマグマができることがある。その時に特徴的にできるマグマが、花崗岩質のマグマで、花崗岩と水とは密接な関係がある。大陸には古代の花崗岩が豊富にあり、しかも、各時代に花崗岩が存在する。ということは、花崗岩の存在自体が、海の存在の証明となる。
最古の花崗岩は、約40億年前のものが、カナダの北西準州のアカスタ地域で見つかっている。水の存在の可能性は、42.8億年前よりは、古くならないが、最古の堆積岩(38億年前)よりは、古いものとなる。
しかも、35億年前以前の大陸地殻の量は非常に少ない。したがって、35億年前以前には花崗岩の浸食・風化があまり進まず、海洋への栄養塩供給は制限されていたことが推測される。
「世界最古」とされる生物化石は、グリーンランド南東部の37億年前と推定される地層から見つかった。約37億年前であるのは、それ以前の海洋に栄養塩(水素・炭素・酸素以外の、無機塩類として存在する植物の生命を維持する栄養分として必要な、リン・窒素・カリ・珪素などの主要元素とマンガンなどの微量元素)が不足していたため生命活動が促進されなかったことを物語る。
花崗岩は言わば様々な鉱物の結晶体の集まりで、中でも組成される石英は水晶であり、他にピンク色のアルカリ長石や黒雲母といった鉱物と、あとは緑色を帯びた黒色の普通角閃石hornblende(ケイ酸塩鉱物の一種)の有色鉱物などが含まれている。1mm以上もある比較的粗粒の岩石から構成された火成岩、即ちマグマが地下深所でゆっくりと冷却し固結してできた完晶質の深成岩から、この花崗岩が形成される。
地球が形成された約46億年前から、シアノバクテリアなどの生命活動が始まる先カンブリア時代、古生代初期から出現するサンゴや貝類や最初の脊椎動物の魚類が登場する古生代、ジュラ紀・白亜紀の恐竜がいた中生代、最古の人類が登場した新生代といった永い年月を経る過程で、数十億年から何千何百万年もかけて地球が火山活動と地殻の変動で隆起を繰り返すごとに、地表にいろんな山脈や岩脈が様々に形を変え露出して来た。
 地球上最古の岩石は花崗岩である。カナダ北西部に分布するアカスタ片麻岩は、成分であるジルコン結晶から40億年前のウラン・鉛放射性同位体年代が得られている。このアカスタ片麻岩はトーナル岩tonalite(深成岩の一種、花崗岩と閃緑岩の中間のような性質を持つ)や花崗岩などから構成されている。
地球上最古の岩石は花崗岩である。カナダ北西部に分布するアカスタ片麻岩は、成分であるジルコン結晶から40億年前のウラン・鉛放射性同位体年代が得られている。このアカスタ片麻岩はトーナル岩tonalite(深成岩の一種、花崗岩と閃緑岩の中間のような性質を持つ)や花崗岩などから構成されている。いずれにしろ、水の惑星が誕生した。陸地を構成する主要な岩石は、海がないとできない花崗岩である。その存在は海があった間接的証拠と言える。発見された最古の花崗岩は約40億年前のものである。となれば、その時代には海ができていたことになる。
また、土砂が海底で堆積してできる堆積岩についても、最も古いものは40億年前のものと言われるなど、40億年前には海ができていた証拠はいろいろあるようだ。38億年以降には堆積岩が世界のあちこちから発見される。既に海が広がっていたようだ。その時代、大量の炭酸ガスで満たされ大気圧も高かったため、初期の海は100℃をはるかに超える高温であった。しかし、海ができると、それまで60気圧ほどもあった空気中の炭酸ガスは海水に溶け、カルシウムやマグネシウムと結合して炭酸塩(炭酸イオンCO32−を含む化合物の総称)として沈殿することで空気中の濃度が急速に低下し、数気圧にまで減少したと言う。温室効果は急速に低下し、地球は冷却していくが、大気圧が1気圧に下がるまでは、依然として海水温は100℃を超えていた。
海の誕生によってはじめて水を溶媒とした化学反応が可能になり、有機化合物が合成され、生命が誕生する条件が整う。海の誕生が40億年前だったとすると、生物化石が、グリーンランド南東部の37億年前と推定される地層から見つかったとなれば、僅か1~2億年後に、細胞が誕生していたかも知れない。海ができて化学反応が可能になると、直ぐに、無機物から有機化合物が合成され始めた。この過程を化学進化と言う。やがて誕生した生物が多様な変化をする。ここから生物進化が始まった。
その後の急激な化学進化や生物進化は、地球が冷えてきて原始大気が還元的になったからと言われてきた。しかし、依然として地球はマグマオーシャンであって非常に熱く、次第に冷えてきて海ができた時にも、海水は120℃とか130℃という高温であった。こういう経過を経た環境では還元的な大気とはならず、水蒸気(H2O)のほかは炭酸ガス(CO2)など、酸化的な分子で満たされていた。むしろ自由な酸素は存在せず、酸化された物質からなる環境であった。こういう酸化的な環境では、有機化合物の合成は容易ではない。
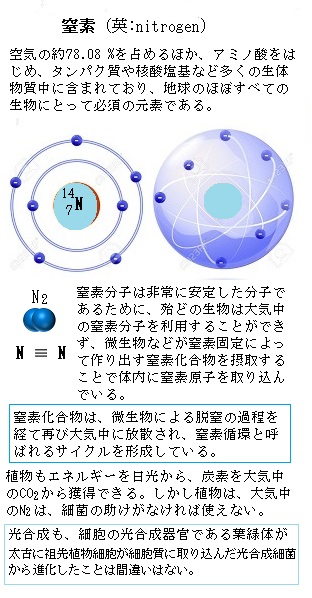
窒素原子(N)は、アミノ酸をはじめとする多くの生体物質の構成原子であり、地球のほぼ全ての生物にとって必須な原子でもある。大気の約78%を占める窒素分子(N2)は、三重結合 (N≡N) をして極めて安定しているため、活性化エネルギーが大き過ぎて化学反応による原子の組み換えは、通常の大気中では起こりえない。
目次へ
チムニーchimneyとは、英語で煙突という意味、海洋学では、海底熱水鉱床の活動により生成される柱状の構造をなす熱水噴出孔を言う。地熱で熱せられた水が噴出する割れ目で、煙突のように海底からつき出している形から、チムニーと呼ぶ。数百度の熱水は、重金属や硫化水素を豊富に含む。深海によく見られる熱水噴出孔周辺は、生物活動が活発であり、噴出する液体中に溶解した各種の化学物質を目当てにした複雑な生態系が形成されている。
有機物合成をする細菌や古細菌(アーキア)が食物連鎖の最底辺を支え、ジャイアントチューブワームgiant tubeworm(ハオリムシの仲間;wormとは、細長く足のない虫)や、環境中の化学合成細菌などを摂食するユノハナガニ・二枚貝・エビなどがみられる。
チムニーは、1977年、赤道直下のガラパゴス諸島の北東320kmあたり、深さ2,600mを超える深海底で、太平洋海膨で米国の潜水調査船「アルビン号」により熱水噴出口が発見され、その存在が初めて明らかになった。以来、太平洋や大西洋などのプレート発散境界にできる海嶺や火山フロントに沿うような、世界中の地殻変動が活発な場所にチムニーが分布していることが明らかになった。
チムニーの分布は、新しい海洋底が誕生する場所にあり、海底からしみ込んだ海水がマグマに熱せられ、周辺の岩石から金属イオンを大量に溶かし込んで、350℃にも達する高温の熱水になって海底に噴出する場所にある。周辺には、噴出する水素や硫化水素やメタンを餌にして、たくさんの硫黄細菌というバクテリアが生息している。また、大量に存在するバクテリアを共生させたジャイアントチューブワームをはじめ、硫黄細菌を餌として食べるエビやカニ、二枚貝の仲間、さらにはサカナの仲間まで、たくさんの多細胞動物が棲み着いている。このような場所に棲むバクテリアは、光合成能力もなく酸素を利用することもない古細菌の仲間で、この環境下で大いに繁栄している。
硫黄sulfurは、原子番号16・原子量32.066の元素で、自然界では、同位体組成 32S(95.018 % )、33S( 0.750% )、34S(4.215 % )、36S( O.Ol7% )の原子で広く分布し、また原油の中では硫化水素H2Sや二酸化硫黄SO2として、また各種金属の硫化物・硫酸塩などの形で存在し、生体内のタンパク質を構成する重要な原子となっている。
現代の海水中には、塩と微量金属が溶け込んでいるが、硫酸イオン(SO4 2-;硫酸H2SO4は酸性で、酸性の物質はイオンになるときに水素を放出する)は塩化物イオン(Cl−;水中に溶解している塩化物の塩素分のことで、水中で分解されたり、沈 殿したりすることなく水中にとどまっている)に次いで多く、その存在度は 28mmol(ミリモル; molとは溶液1L中に溶けている分子の数を表す物質量の単位、1 mol=6.02×1023個)である。
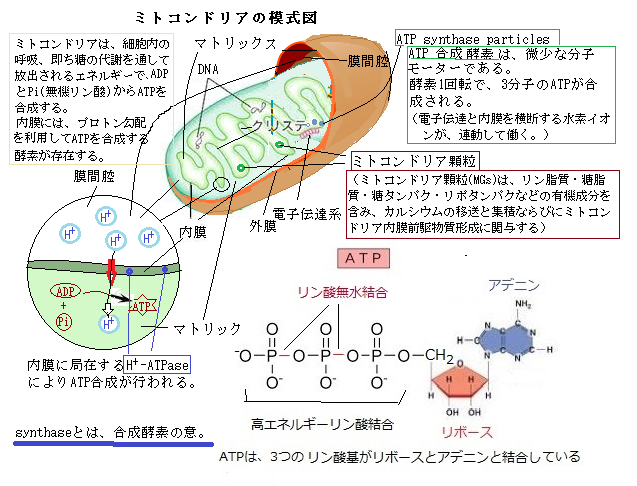 陸上植物では、硫酸イオンは根から吸収されて、維管束を経て植物体内の茎・葉・生殖器官・種子などに輸送される。また、老化した組織からの篩部を経由する転流輸送もある。硫黄は、硫化水素・亜硫酸・硫酸などで自然界に循環し、生物圏にも複雑に関わっている。硫黄の酸化還元反応は、生物のエネルギー代謝における重要な反応であり、酸素が乏しかった太古代においては、生物にとっての主要なエネルギー源であった。
陸上植物では、硫酸イオンは根から吸収されて、維管束を経て植物体内の茎・葉・生殖器官・種子などに輸送される。また、老化した組織からの篩部を経由する転流輸送もある。硫黄は、硫化水素・亜硫酸・硫酸などで自然界に循環し、生物圏にも複雑に関わっている。硫黄の酸化還元反応は、生物のエネルギー代謝における重要な反応であり、酸素が乏しかった太古代においては、生物にとっての主要なエネルギー源であった。非常に難しい微生物であっても、そのゲノム塩基配列が解読されて培養が可能になり、多くの謎に包まれていた様々な生命体の本質が解明されるようになった。硫黄を含む温泉や深海の熱水噴出孔のチムニーなど、生物の生育に適さない地球上で最悪の環境の中でも増殖している生命体がある。
殆どの動物細胞や植物細胞にとって、糖の段階的分解の解糖は、食物分子分解の第3の最終段階に入る前の序章に過ぎない。その第3段階では、酸素の消費に伴う酸化的リン酸化により、ミトコンドリアで大量のATPが生成される。しかし、酸素がない太古代Archean eonでは、酸素がなくとも成長と分裂ができる嫌気性菌にとって、解糖がATPを得るためには不可欠であった。
これは、酸素量が少ない条件下が働き続ける動物細胞、例えば骨格筋細胞にも当てはまる。
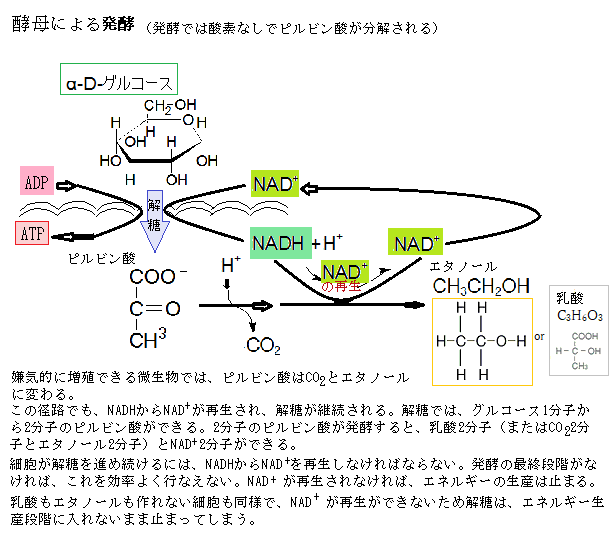
嫌気的環境下では、解糖で生じるビルビン酸とNADHは、細胞質に留まり、ピルビン酸(C3H4O3)は、他の物質に変わって細胞から排出される。例えば、強く収縮している筋細胞では、酸素不足の状態になると、解糖によって生じるピルビン酸を細胞質中で乳酸(C3H6O3)に変わり、醸造やパン製造に使われる酵母細胞では、エタノールethanol(C2H5OH;別名はエチルアルコール ethyl alcohol)とCO2に変わる。
NADHは、解糖反応を維持するため、電子を細胞質中に放出して、NAD+に戻る。酵素が無い条件で、原則としては酸素による酸化を行われないで、真核単細胞生物の酵素で、糖を分解してエネルギーを獲得する径路こそが発酵fermentationと呼ばれる生化学反応である。酵母菌は単細胞であっても核があるから真核生物である。単細胞の大腸菌は、核がないため原核生物に分類される。
 酵母の生成物(排泄物)の一つであるCO2によって生地膨張が進む。また同時にエタノールも排出するので、アルコール発酵といわれる。しかし酵母は、
酵母の生成物(排泄物)の一つであるCO2によって生地膨張が進む。また同時にエタノールも排出するので、アルコール発酵といわれる。しかし酵母は、小麦タンパクやでんぷん、砂糖を、直接、食べることはできない。何段階も分解酵素(消化酵素)によって多糖類→二糖類→単糖類と分解し、単糖類のブドウ糖や果糖になって初めて、酵母の体内に取り込まれ消化される。これを「糖化」と呼ぶ。また小麦タンパクも一部は消化酵素によってアミノ酸に分解され、酵母の餌となりその排泄物が旨味や芳香を醸し出す各種有機酸やエステル類を排出する。このように発酵と糖化が同時に進行する過程を「並行複発酵」と呼ぶ。
現実には、パン酵母の複雑な発酵が、少しでも酵母発酵がどのように進行していくのかを考えながらパン作をすることが、美味しいパンの優劣と好みを決定している。
例えば、酵母が糖をアルコールとCO2にするのをアルコール発酵、乳酸菌が糖を分解して乳酸を生成するのを乳酸発酵という。
アルコール発酵の反応は、以下の化学式で示すように、1分子のグルコース(C6H12O6)からエタノールとCO2が2分子ずつできる。
C6H12O6(グルコース) ⇒ 2C2H5OH(エタノール) + 2CO2
酵母は、酸素がない状態で、糖を分解してエネルギーを得る。その結果、エタノールと二酸化炭素が作られるのが、アルコール発酵である。このグルコースの分解反応系自体には、酸素は関わらない。このように有機物が酸素のない状況で分解されて、ATPを生成する過程を「発酵」と言う。発酵では解糖系のNADH は、ピルビン酸を乳酸などに還元することで、自身は脱水素酵素の働きにより酸化されて NAD+に再生される。
細菌のなかには、ヒト・家畜・作物などに病気を引き起こす有害なものがあり、また食べ物を腐らせる腐敗菌もある。その一方で、人類は食品を貯蔵する手段として、あるいは食品の素材自体には存在しない独特の味や香りを付与する方法として、細菌をはじめとする微生物の力を巧みに利用してきた。微生物microorganismによる発酵食品は、現在の進んだ技術でも、化学的に合成できない微妙な香味を醸しだし、人々の食生活を豊かにしてきた。その代表的な細菌が乳酸菌で、「乳酸菌」は、炭水化物の糖類などを発酵してエネルギーを獲得し、多量の乳酸を生成する一群の細菌類のことを言う。
量の多少に拘らなければ、乳酸を生成する細菌は豊富に存在する。乳酸菌は通常、消費した糖類から50%以上の割合で乳酸を生成する細菌と定義されている。乳酸菌は酸素の存在する環境でも増殖できるが、どちらかといえば酸素の比較的少ない環境を好む。乳酸菌の増殖には多くの種類の栄養素が必要であるため、乳酸菌は主として動植物界や食品など、人間の生活圏を中心に分布している。
ジャイアントチューブワームには、目も口も消化器官すらない、あるのは鰓(えら)と循環器と生殖腺だけで、その生き方は植物のような動物と言える。チューブ状の棲管から出ている明るい真っ赤な羽毛Plumeは、高度に導管化された器官で硫化水素・二酸化炭素・酸素などを交換できる能力がある。体内に硫酸塩還元菌などの化学合成細菌を共生させ、海底から噴出する熱水に大量に含まれている火山性ガス、特に硫化水素H2Sを、赤い鰓で酸素と二酸化炭素とともに取り込み濾過し、それを共生する硫黄栄養細菌に供給して、有機化合物に化学合成してもらい、それを栄養源にする。ジャイアントチューブワームの体内に共生しているバクテリアは非常に多く、体重の半分ほどに及ぶ。ある計測では2,850億個のバクテリアが含まれていた、と言う。今のところジャイアントチューブワームの発見事例は、太平洋の海底のみである。 二酸化炭素の濃度が一定の場合、水温が低いほど二酸化炭素は水に溶けやすい。水温が高くなると溶けにくくなるのは、温度が高くなると解けている二酸化炭素の分子運動が激しくなり、溶液から飛び出すからである。
ヘンリーの法則では、一定温度で一定の量の溶媒に対して、「溶媒に溶ける気体の物質量は、圧力に比例する」、「溶媒に溶ける気体の体積は、その圧力のもとで一定になる」。深さ2,600mを超える深海底のチムニーから噴き出される熱水は、350℃にも達すると言う。
現代の環境では、海水中の二酸化炭素は、海洋表層だけで大気中の二酸化炭素の約 1.4 倍の量が含まれている。この量は、大気中の二酸化炭素が増加するとそれに比例して海水に溶解する量も増えるが、大気温度が上昇すると逆に海水から大気中に二酸化炭素が放出される。一方、空気の温度が高くなると、空気の体積が大きくなるため、同じ体積中に含まれる気体分子の数は、その温度に反比例して少なくなる。ただ気温による実際の影響は、最大で8%程度と言う。気圧の影響も、気圧に比例して同一体積中に含まれる気体分子の数が増えるが、実際の影響は最大でも2%程度と言う。ジャイアントチューブワームが棲む異常すぎる海底環境における二酸化炭素の実際の濃度は、どうなるのだろうか?
一方、ボイル・シャルルの法則によれば、「体積を変えずに圧力を下げると、温度は下がる」。
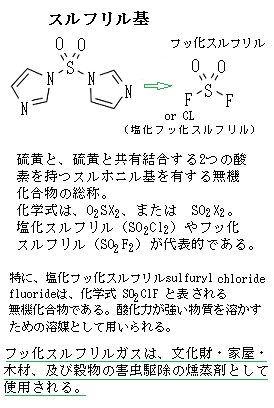 ジャイアントチューブワームの鰓が赤く見えるのは、血液中にヘモグロビンが多く在るからである。チューブワームのヘモグロビンは巨大で、血漿中に遊離している。通常、硫化水素と結合すると酸素の運搬能力は激減するが、チューブワームヘモクロビンは、高濃度の硫化水素の環境であっても酸素運搬能力は影響を受けない、と言う。
ジャイアントチューブワームの鰓が赤く見えるのは、血液中にヘモグロビンが多く在るからである。チューブワームのヘモグロビンは巨大で、血漿中に遊離している。通常、硫化水素と結合すると酸素の運搬能力は激減するが、チューブワームヘモクロビンは、高濃度の硫化水素の環境であっても酸素運搬能力は影響を受けない、と言う。チューブワームでは、硫化水素酸化酵素やチオ硫酸開裂酵素、ATPスリフリラーゼ(ATP sulfurylase;sulfurは、硫黄、原子記号:S、sulfuryとは、「硫黄(質)の」意味)などの酵素活性が確認されている。多くの細胞が用いている化学反応の一つに、分子にスルフリル基sulfuryl groupを付加するというものがある。スルフリル基は、通常の細胞条件下では、酸素原子を豊富に持っているため、負電荷を帯び、他の分子と水素結合hydrogen bondできる。これによりスルフリル化した分子は、水に溶解できるようになる。特に、ATPスリフリラーゼは、硫酸塩をATPに転移してアデノシン5’-ホスホ硫酸(APS)およびピロリン酸(PPi)を生成することにより、硫酸塩の活性化を触媒する。そのい反応は可逆的で、APSとPPiからATPを生成することもできる。
細胞質cytoplasm内には、低分子に作用する様々な種類の硫酸転移酵素がある。これらの酵素は何種類かの重要な機能を果たす。例えば、解毒作用において中心的役割を担う。多くの毒性分子は分子量が小さくて水に溶けないため、硫酸転移酵素はスルフリル基とこれらの分子を結合させ、細胞外へ排出し最終的には身体から排除する。 スルフリル基を持つ分子を作るために、細胞は多様な種類の硫酸基転移酵素sulfotransferaseを使う。また硫黄栄養細菌の多くは、分子状酸素O2を酸化剤として用いるため、硫黄栄養細菌は、光合成細菌由来であり、太陽光にも依存しているようだ。ただし分子状酸素に頼れない液体環境では、硝酸塩NO3-を酸化剤に用いる硝酸呼吸を行っているようだ。
硫黄はすべての生物の必須元素であり、適度の硫黄が環境に存在しなければ生存できない。殆どすべての微生物と植物は、硫黄を硫酸として取り込み、硫酸から必須な硫黄化合物を合成する。外界の硫酸をより効率良く吸収し、有機硫黄に分解し吸収して、得られる硫黄量を増加させるとともに、硫黄欠乏状態では機能しない不要なタンパク質を分解することによって、含硫アミノ酸(20種類の天然アミノ酸のうち、メチオニンとシステインが該当し、そしてシスチンがある)をより必須なタンパク質に振り分ける反応と見られている。高等植物では、硫酸吸収や代謝の活性が変動するだ けでなく、種子貯蔵タンパク質の組成が硫黄栄養に応じて変化することが知られている。
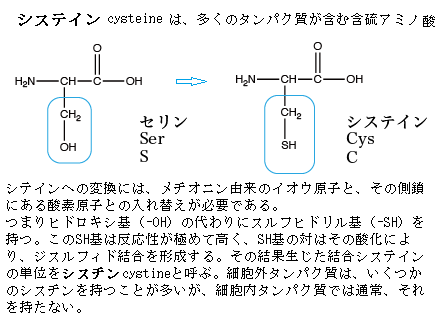 種子貯蔵タンパク質は、種子に蓄えられ発芽時に使われる貯蔵物質の一つであるため、種子においてのみ大量に発現される。高等植物では、硫酸吸収や代謝の活性が変動するだけでなく、種子貯蔵タンパク質の組成が硫黄栄養の環境に応じて変化することが知られている。
種子貯蔵タンパク質は、種子に蓄えられ発芽時に使われる貯蔵物質の一つであるため、種子においてのみ大量に発現される。高等植物では、硫酸吸収や代謝の活性が変動するだけでなく、種子貯蔵タンパク質の組成が硫黄栄養の環境に応じて変化することが知られている。チューブワームは、口も腸も肛門もない生物で、しかも一般の生物では致死量になるほどの硫化水素の濃い環境に生息している。そのため臭いが酷い生物であり、しかも、肛門がないため、化学合成の残留物である硫酸塩が、寿命の数十年の間、かなり体内に溜まっている。解剖の際、その臭いには閉口すると言う。
チューブワーム本体の大部分は、「化学合成細菌の共生袋」と呼ばれる栄養体である。その共生細菌は、主に硫黄栄養細菌である。チューブワームは、硫化水素を特異的なヘモクロビンで捉えて、「化学合成細菌の共生袋」へ送り、硫黄栄養細菌などが行う化学合成により栄養を獲得している。つまり植物の葉緑体による光合成に相当する役割を果たしていている。
植物では、葉緑体による太陽の光エネルギーを利用してATPなどの化学エネルギーと有機化合物を生合成する。言わば、地球生態系では、食物連鎖の起点は、太陽による光エネルギーである。しかし、チューブワームの場合は、炭素を含まない硫化水素などの無機物を酸化することで得られる化学エネルギーを利用するプロセスを歩む。現代の地球生態系の殆どは、太陽の光エネルギーを起点とする光合成による生合成を起点としているが、その生物群以前に、深海水熱水噴出孔やメタン湧水域で、地球内部の物質に依存する独自の生物群を誕生させていた。
チムニーから噴き出される熱水は、最も温度が高いブラックスモーカーで最高350℃にも達する。ブラックスモーカーとは、大洋中央海嶺のチムニーから噴出している、ほぼ300℃以上の高温の熱水に、鉛・亜鉛・銅・鉄や硫化物が多く含まれているため、海水と反応して墨汁のような真っ黒な熱水となって立ち上る状況を言う。その周辺の海域では、硫黄の化合物、メタンや重金属など、通常の生物にとっては有害な物質が豊富含まれている。それなのに、なぜか他の海底域よりも生物が多数集まっている。
海の生態系では、海草や植物プランクトンが太陽の光をもとに光合成をして生命の維持に必要な有機物を作り出す。それを他の生物が摂食する食物連鎖が行われている。これらの光合成生物群集は、水深200mを超える海底では十分な太陽光が入らないため光合成ができない。そのため、海底で生きる生物の数は限られている。
 一方、チムニーには、噴き出される300℃以上の熱水に含まれている化合物を食べて、有機物を合成する微生物が豊富にいる。太陽光が届かない深海底には、特にチムニー周辺には、他の海底よりも多くの生物がいる。その有機物を求めて、多くの生物がチムニーに集まって、化学合成生物群集を形成している。
一方、チムニーには、噴き出される300℃以上の熱水に含まれている化合物を食べて、有機物を合成する微生物が豊富にいる。太陽光が届かない深海底には、特にチムニー周辺には、他の海底よりも多くの生物がいる。その有機物を求めて、多くの生物がチムニーに集まって、化学合成生物群集を形成している。有機化合物を合成するのに必要な条件として、「外部から供給されるエネルギー源」と「還元性」の2つが特に重要である。深海底の熱水の環境下のエネルギーは「高温と高圧」であり、また、噴出する水素H2、硫化水素H2S、メタンCH4、アンモニアNH3などは還元性物質である。酸素により還元され、より安定する物質である。そのため、他の物質から酸素を奪いやすい。
当然、この環境では、高エネルギーが放出され、有機化合物を作る必要条件は満たされている。もう1つ有利に働くのが、熱水が含む高濃度の『金属イオン』である。金属イオンは、有機化合物を合成する際の触媒として働く。熱水噴出口は、その構造からみて高温状態で反応が起き、反応物ができた後はすぐに周囲の低温の水に接するため、できた有機物は分解されにくい。現在の熱水噴出口の周辺でも生き物が集まり、有機物を合成している。
こういう環境では、生物がいなくても有機物の合成が起きる可能性が高い。現在では、実験室内で有機化合物が合成できる。実験室で再現する模擬海水で、材料としてメタンや窒素を加えて高温高圧の条件を与えることにより、様々な種類のアミノ酸やタンパク質など、生体を構成する様々な有機化合物が作れるようになった。生物がいない熱水噴出口周辺の環境でも、有機化合物は合成され、次第に高濃度に蓄積されていく。
2016年8月31日付けの学術雑誌NATUREに「世界最古」とされた化石は、グリーンランド南東部の37億年前と推定される地層から見つかった。そのシアノバクテリア様化石が発見されたのが、海底で噴出したマグマである枕状溶岩のすぐ上に堆積したチャート(頁岩)という堆積岩からである。枕状溶岩の海岸では、つぶれた楕円体の枕を並べたような光景になる。
海底でマグマが噴出すれば、高温の溶岩流の表面は海水に触れて急冷されるため、その表面部分に薄い筒状の殻ができる。しかし、内部は高温状態のままで溶融している。更に、次々と溶岩が噴出し、その圧力で殻が破れ溢れれば、海水により冷却されて殻が重なる。断面で見ると、放射状の節理が積み重なり、この繰り返しで形成される枕状溶岩の存在が、海底に複数のチムニーがあったことを示す証明となる。その溶岩上に、後世、様々な微生物が、長年月、堆積物を層状に積み重ねることで堆積岩の一種、頁岩形成される。今回見つかったシアノバクテリア以外にも、頁岩を作るほどに、非常に単純な単細胞生物であるが、意外にも豊富に存在していたことを示している。
目次へ
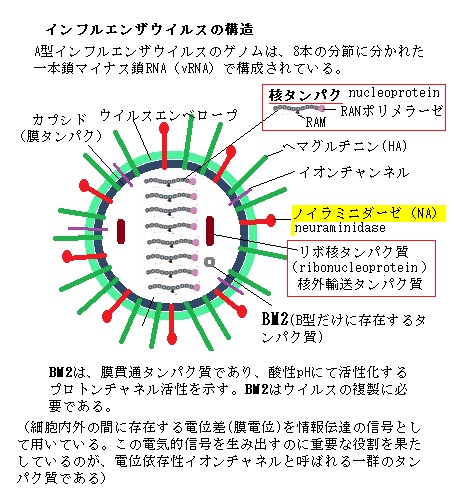 すべての生物には共通の性質があり、それが生物の特徴にもなっている。すべての生物は細胞からできており、それが単独で生きられる基本単位である。しかも、細胞という共通の構造だけでなく、細胞が生きていくための共通の機能が働いている。
すべての生物には共通の性質があり、それが生物の特徴にもなっている。すべての生物は細胞からできており、それが単独で生きられる基本単位である。しかも、細胞という共通の構造だけでなく、細胞が生きていくための共通の機能が働いている。すべての細胞は細胞から生じる。新しい細胞を作るには、既存細胞が分裂するしかない。増殖するために、親細胞は複雑であるが精密に制御された手順通りに、細胞の中身を倍加して2つに分けなければならない。この倍化と分裂の過程を、細胞分裂周期、または細胞周期と呼ぶ。これに関わる多くのタンパク分子のごく一部であっても欠損があれば細胞は大打撃を受ける。
細胞という共通の構造を支える物質的基盤には、遺伝子としてのDNA、様々に機能する高分子としてのタンパク質、細胞の膜構造としての脂質などの共通性がある。その物質的基盤の働きにより、エネルギー産出や代謝によって細胞(個体)の恒常性を維持し、環境変化に応答しつつ、細胞や個体の永続と繁栄に勤しむ。これらが生物に共通する性質、単一性unityである。これが生物の定義でもあるため、ウイルスの細胞には、その単一性にあたいする構造も機能を持たないため生物に含められていない。
ウイルスは、他の細胞に入り込んで生き、自身の遺伝子を発現させてタンパク質は作れるが、増殖するためには、他生物の生きた細胞に進入して、その分子装置を取り込んで、自己を複製させて増殖する、極微小な感染性の構造体なので、非生物とされる。しかしながら、ウイルスの生態は、生物の根源のような働きをしている。ウイルスもタンパク質の殻とその内部に入っている核酸からなる遺伝子を持っている。簡単な構造であるが、遺伝子の周りをタンパク質が包んでもいる。一番外側のタンパク質は、他の細胞に吸着する構造になっている。
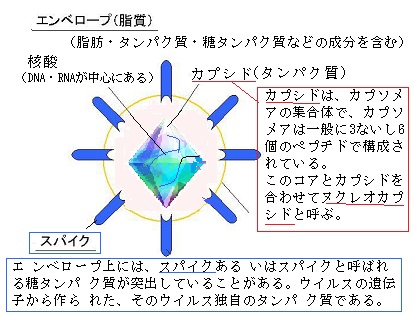 地球上の殆どの生物は、生命活動の基本となる構成では共通の特徴を持っている。即ち、4つの塩基からなるDNAを持ち、タンパク質には共通の20種類のアミノ酸を使い、しかも、DNAに書かれた遺伝情報を元に、機能分子であるタンパク質を作る仕組みなど、多くは共通している。
地球上の殆どの生物は、生命活動の基本となる構成では共通の特徴を持っている。即ち、4つの塩基からなるDNAを持ち、タンパク質には共通の20種類のアミノ酸を使い、しかも、DNAに書かれた遺伝情報を元に、機能分子であるタンパク質を作る仕組みなど、多くは共通している。更に、遺伝暗号も一部の例外を除けば基本的には同じである。要するに、地球上に現存する生物は一つの祖先生物の子孫であるか、少なくとも遺伝装置やタンパク質合成装置など生命活動に必須の遺伝子については同一のものを共有した一つの種から進化し、分化してきたと考える方が正鵠を得ている。
植物とは少なくとも祖先が一次共生色素体を共有する生物であり、一次共生色素体の獲得という進化の画期となる出来事に基づいている。
それによる「酸素発生型光合成能」などは、長い時間をかけて出来上がった仕組みである。生物が様々な代謝系を作り、それを細胞間で連携させるには非常に長い時間が掛かる。光合成の代謝系もまた同様で、生物が共有する遺伝子組み換えと言う、多少異なる性質を獲得した個体が生まれる仕組みを備えながら、やがて過酷な環境変化に適応できた元の生物種とは異なる新たな生物種が分岐と進化を重ねていく。その多様化する生物種であっても、代謝系は、植物界においてほぼ共通している。その中でも、光合成の代謝系は、植物界の進化の過程で突然現れ
 た代謝系であった。それが「一次共生」と呼ばれる細胞内共生である。シアノバクテリア自体を細胞内に取り込んで、細胞内の小器官として共生させたシアノバクテリアこそが、真核生物の植物界で共有する光合成器官の「葉緑体」となり、その分化と進化を促進する原動力となった。
た代謝系であった。それが「一次共生」と呼ばれる細胞内共生である。シアノバクテリア自体を細胞内に取り込んで、細胞内の小器官として共生させたシアノバクテリアこそが、真核生物の植物界で共有する光合成器官の「葉緑体」となり、その分化と進化を促進する原動力となった。地球上の生物多様性biodiversityは40億年という長い歴史の中で、様々な環境に適応して進化し、3,000万種ともいわれる多様な生物を誕生させた。これらの生命体一つひとつに個性があり、全て直接、あるいは間接的に支え合って生きている。生物多様性条約では、生態系の多様性・種の多様性・遺伝子の多様性という3つのレベルで生物の多様性diversityがあるとしている。単一性と多様性は、地球上生物の特徴の一つである。
生物の世界は非常に多様である。動物界においても顕微鏡がなければ見られない、ゾウリムシより小さいといわれるアザミウマタマゴバチは、寄生バチ世界最小のハチとして有名である。体長は約0.18mmしかなくゾウリムシの約0.2mmより小さい。アザミウマタマゴバチは、体長1mm前後の小さな昆虫アザミウマが、通常葉の組織の中に0.2~0.5mm程度の小さな卵を産みつける、その小さな卵に寄生するさらに小さな幼虫、世界最小の昆虫と言われている。こんなに小さな蜂にも、立派に触角と産卵管があり、雄雌がいて交尾し産卵するなど高度の生物活動している。
動物界で大型な恐竜がいた。爬虫類の一グループで、三畳紀中期(2億3500万年以上前)から白亜紀末(6600万年前)まで繁栄した全長30m以上まで様々な大きさ・形態の生物であったが、地球に二本足で歩く肉食動物として現れたと当初は、体のサイズも小さかった。それから1億7,000万年という地球上で最も繁栄し、生物の頂点へと上りつめていた。
 植物界では、藻類のような小型で比較的単純なものから、ジャイアントセコイアのように巨大で複雑なものまで様々な種がある。ジャイアントセコイアはスギ科(またはヒノキ科)の針葉樹で、アメリカ・カリフォルニア州シェラネバダ山脈の西斜面の標高1,500〜2,800mに生息し、世界一体積が大きい樹木として有名である。高さ約83.8m、根本の周囲約31.1m、樹齢は2,300年〜2,700年と言われている。世界一高い木は、同じスギ科セコイア属のカリフォルニア・レッドウッドCalifornia
redwoodといい、116mもある。セコイアSequoiaはスギ科の常緑大高木、1億数千年前、恐竜の時代に最も繁茂した裸子植物の生き残りと見られている。樹齢2,000年のジャイアントセコイアが、今も活発に成長を続けている。
植物界では、藻類のような小型で比較的単純なものから、ジャイアントセコイアのように巨大で複雑なものまで様々な種がある。ジャイアントセコイアはスギ科(またはヒノキ科)の針葉樹で、アメリカ・カリフォルニア州シェラネバダ山脈の西斜面の標高1,500〜2,800mに生息し、世界一体積が大きい樹木として有名である。高さ約83.8m、根本の周囲約31.1m、樹齢は2,300年〜2,700年と言われている。世界一高い木は、同じスギ科セコイア属のカリフォルニア・レッドウッドCalifornia
redwoodといい、116mもある。セコイアSequoiaはスギ科の常緑大高木、1億数千年前、恐竜の時代に最も繁茂した裸子植物の生き残りと見られている。樹齢2,000年のジャイアントセコイアが、今も活発に成長を続けている。
多様さは広がる一方である。原虫や酵母、細菌など多彩な生物が、水中や土壌中に生息し、時には他の生物体内や体表を棲みかにする。血液や組織に寄生する原虫の多くは、特定の吸血昆虫やマダニの腸管で増殖し、これらを媒介者として人体に感染する。マラリア原虫はハマダラカ、リーシュマニアはサシチョウバエ、アフリカのトリパノソーマはツェツェバエを媒介者とする。
原虫ような単細胞の原生生物は、土壌に棲むか病原性のものであるため日常おなじみであるが、古細菌は他の生物では生きられないような環境に居る。濃い塩水、熱い酸性の温泉、空気の無い深海底の泥、硫化水素ガス吹き出ている海溝のチムニー、汚水処理場のヘドロ、南極の氷の下の池の中、酸性で酸素の無いウシの胃の中に生息し、あるいはセルロース(地球上で最も多く存在する繊維質の炭水化物)を分解してメタンガスを作るものもいる。これらの極限状態にある環境は、大気に酸素が増える以前の原始の地球にあった過酷な世界である。それは、地球上の生命体が発生した当時の環境条件であった。
かつて生物の分類の対象になりえたのは、目に見える世界に生息するものに限られていた。現在では、生命の遺伝的多様性は、顕微鏡でしか見えない生物の世界の方が飛びぬけていることが明らかになった。最も重要なことは「細菌」と括られてきた生物の中には、進化の起源が原核生物と真核生物ほどにかけ離れている種が多数混同されていた。原核生物と分類された中には、地球上の生命の歴史の初期に分岐した「細菌」と「古細菌」という2つの別集団が含まれていることが明らかになった。生物は細菌と分岐した種から「古細菌」と「真核細胞」に更に分岐した。「古細菌」と「真核細胞」は、互いに「細菌」よりも近縁関係にある。現代の生物界では、細菌と古細菌と真核生物の3大部門(ドメイン)に分類する。
大きな生物は細胞の集合体であるが、その個々の細胞は、顕微鏡で観察される単細胞生物とかなり似ている。動物・植物・微生物いずれも細胞で形成されているが、これらの多様な生物の外形に関わらず、その細胞には、あらゆる生物に共通する性質を数多く持っていることが分かる。生化学の発達により、この見方はより強く裏付けられてきている。
細胞の「世界最古」とされた化石は、グリーンランド南東部の37億年前と推定される地層から見つかった。そのシアノバクテリア様化石が、細胞と言う小さな袋を持つ生命の誕生を物語る。
細胞と言う画期的な構造やシステムを作るのに必要な、周辺環境と独立した内部環境を形成できる切っ掛けとなった。それは現在の生物にまで受け継がれて来た大きな特徴である。地球上には、様々な細胞があるが、細胞膜で覆われた袋と言う構造は例外なく共通している。細胞膜に囲まれた小区画の形成により、外部環境から独立した特別な内部環境を作ることで、細胞の中に複雑で精巧なシステムを構築する長い道のりの第一歩が刻められた。地球上に細胞が登場した時が生命の誕生であった。
細胞の構造と機能は、遺伝子に支配されている。単一性を支配しているのも遺伝子である。他方、生物に多様性が生じるのは、遺伝子に突然変異が生じる、言い換えればDNAの塩基配列が変化するからである。その結果、構造や機能が変化した細胞や個体が生まれる。祖先を共通しているのに、遺伝子の変化により、多様性が生じ多くの子孫の中から、変異の蓄積により構造や機能が大きく変化した種が現れて、別の種として分岐していく。
ある生物の遺伝子1セット、物質的にはDNA1セットを、その生物の「ゲノム」と呼ぶ。生物の多様性は、ゲノムを根源にすると言える。
目次へ
顕微鏡で見える種々の細胞のうち、細菌は最も簡単な構造で、不要なものすべてを削ぎ落した生命の姿がかいまみられる。細菌は細胞小器官を持っていない。DNAを保持する核すらない原核生物である。その核の有無が、生物分類にとって基本的な基準になる。
核を持つ細胞から形成される生物を真核生物eukaryote(juːkǽriòut)と呼び、「eu」はギリシャ語で「十分な」や「真の」を意味する。Karyoteは、「粒」や「中核」を意味する。核を持たない細胞からなる生物は原核生物prokaryoteと呼ぶ。「pro」とは「~以前」の意味である。真核細胞は一般に細菌や古細菌より大きく精巧である。真核生物でもアメーバや酵母のように単細胞生物もいるが、多くは多細胞の集合体として生活をする。植物・動物・菌類fungi(葉緑体を持たないカビ・キノコ・酵母などを含む真核生物の一群)など複雑な多細胞生物は、すべて真核細胞でできている。
菌類の酵母
菌類は真核生物であるが、光合成能を欠くため、周辺の生物に腐生的・強制的・寄生的に生活し有機物を吸収することで栄養を得る。一般的には、菌類は肉眼で見えないものが多く、化石になっても発見しにくいが、菌類の分布は世界的であるため、種類によっては、特にキノコの化石などが相当数、発見されている。菌類は、植物が陸上をし始めたよりも、約4億年前に既に海から陸上していたと見られている。
グリーンランドの38億年前の岩のなかに炭素の粒が発見された。これはバクテリアだったと推定された。最も古い時代の菌類化石は、先カンブリア時代 (地球が誕生した約46億年~5億9000万年前まで、主に地質学で使われる時間の単位)のバクテリアや藍藻の化石が混じった岩石中に、2種の菌糸の化石が見出されている。水生菌であったとようだ。菌類は、20億年以上も前に既に出現していたようだ。
22億年前と8~6億年前に、海も凍る全球凍結Snowball Earthが起こった。その当時にできた氷河堆積物や氷河地形などが証拠となっている。氷河堆積物を手がかりに氷河の位置も知ることができる。平均気温は-50℃以下になった。
酸素がある大気は、地球特有のもので、酸素が発生し始めたのは、今から30~27億年ほど前と言われている。海に光合成を行うシアノバクテリアが現れ、酸素が放出されるようになった。当時の海には大量の鉄分が溶け込んでいた。そのため放出された酸素は、初期のころは海水中の鉄と化合した。この酸化鉄は二酸化ケイ素の層と交互に堆積し赤茶けた縞模様の縞状鉄鉱層を形成した。現在、工業的に使われる鉄鉱石の大半が、当時のこの縞状鉄鉱床から採掘されている。
シアノバクテリアはコロニーを形成する。それをストロマトライトstromatoliteと呼ぶ。シアノバクテリア類の死骸と水中に浮遊している泥粒や岩石砂粒などを石灰分で固めた層状の堆積構造を持つ。それがだんだん年輪のように大きくなり、ストロマトライトの縞模様を作る。シアノバクテリア自体は、ストロマトライトの表面に棲み続けている。水中の鉄分が減少すると、シアノバクテリアに放出された酸素は大気に流れる。約6億年前の大気には、現在の大気中の酸素量の1%が存在するようになった。
現在でもストロマトライトは形成されている。西オーストラリア州の西海岸中央部ガスコイン地域に存在するシャーク湾 Shark Bayの浅瀬には、直径50~60cmのただの黒い岩が密集する不気味な光景が見られる。巨大なまこのような黒い岩体のストロマトライトの群生があり、20億年以上も前から変わらず、海の中で酸素を泡状に産出している。シャーク湾の現生のストロマトライトの年間成長率は0.4mm程度だとする研究例もある。
酸素を生み出すシアノバクテリアは、生物の主要な系統の一つである古細菌Archaeaに含められる。古細菌は菌類でも細菌でも無く、系統が全く異なる。分類学上は菌類が真核生物ドメインに含まれ、細菌が細菌ドメイン、古細菌が古細菌ドメインを構成している。
 シャーク湾の「ハメリン・プール海洋自然保護区」には、世界最古の生命体と言われるシアノバクテリアは、日中は光合成を行い、夜間は泥などの堆積物を粘液で固め、呼吸のために上に上に分裂しながら、日が昇ると再び光合成を繰り返すという生態で、先カンブリア時代という太古の時代から生きながらえてきた。
化石となったものは世界各地で発見されているが、原生しているものがこれほど広範囲に見られるのは、ここハメリン・プールだけだと言う。海水の石灰砂や泥粒などが何層にも積み重なり、1年に0.4mm程度という非常に遅い速度で岩石質に成長したものが現在の光景である。
シャーク湾の「ハメリン・プール海洋自然保護区」には、世界最古の生命体と言われるシアノバクテリアは、日中は光合成を行い、夜間は泥などの堆積物を粘液で固め、呼吸のために上に上に分裂しながら、日が昇ると再び光合成を繰り返すという生態で、先カンブリア時代という太古の時代から生きながらえてきた。
化石となったものは世界各地で発見されているが、原生しているものがこれほど広範囲に見られるのは、ここハメリン・プールだけだと言う。海水の石灰砂や泥粒などが何層にも積み重なり、1年に0.4mm程度という非常に遅い速度で岩石質に成長したものが現在の光景である。砂漠に囲まれたハメリンプール一帯の海域は、海水が蒸発して高濃度の塩分を含有しており、シアノバクテリアの天敵である貝類や甲殻類は寄り付けない。シアノバクテリアはそういう過酷な環境でも生き抜ける原始的な構造であったため、天敵がいない世界で着実に コロニーを育むことができた。
シアノバクテリアは、1,970年代までは、クロロフィルαを持ち、光と空気の存在下で、最初に酸素発生を伴う光合成ができた、多様な細菌の一群に属す藻類(藍色植物門)のなかの一分類群とされていた。藍藻blue-green algaeと呼ばれていた。光合成を行う糸状のシアノバクテリアAnabaenaは、単細胞のものもあったが、球状の細胞が長く連なる繊維状体を形成しコロニーも作っている。シアノバクテリアには、空気上の窒素を固定できる種も多い。ただ葉緑体までは持たず、クロロフィルは細胞内の特殊な膜(チラコイド)で保持されている。
藍藻とは文字通り藍色の藻類のことで、他の藻類や陸上の植物と同じように、太陽エネルギーによって光合成を行う独立栄養生物である。しかし主要な光合成色素は、クロロフィルaとbを持つ被子植物などと異なり、クロロフィルaとフィコビリンphycobilinである。フィコビリンは、藻類、特に紅藻植物門やシアノバクテリアが持つフィコビリタンパク質に結合する発色色素の総称である。フィコビリタンパク質は光合成の赤色の補助色素として働く。
紅藻植物門はクロロフィルaのほか光合成色素のフィコエリトリンphycoerythrinなど、緑・黄・青・赤の4色の色素を含む。フィコエリトリンは、フィコエリスリンと読む場合も多いが、いずれも正確な発音ではない。フィコビリタンパク質の一種で、紅藻類および藍藻類に存在する赤色の色素タンパク質のことである。浅所に生える種は赤以外の色素を多く含むのに対し、深所に生える種は赤い色素を多く含むので、紅藻の仲間には多様な色の変化がみられる。アサクサノリ・テングサ(マクサ)・フノリ・マクリ(カイニンソウ)・ツノマタなど食用や薬用になる海藻が知られている。
33~35億年前の地層から、現在の藍藻に似た微化石が発見されている。藍藻の祖先は地球の酸素の生みの親と見られている。地質時代の早期に出現した藍藻は、その形態を殆ど変えることなく生息域を広げ、今日まで生き続けている。その姿はまさに“生きた化石”と呼ぶにふさわしい。藍色細菌は淡水・海水・土壌・岩石及び植物に着生あるいは共生し広く分布している。極地や高山から温泉にまで、非常に様々な環境に適応 し、他の生物と共生しているものもある。種類や生育場所によって色素組成が異なるため、藻体の色は藍色から赤色、青色、緑色、緑褐色、または黒色に近いものまで様々である。藍藻の体制は単純で、単細胞か群体を形成するか、あるいは糸状体である。有性生殖は知られていない。 また、藍藻は核という構造を持たない原核生物であるという点で、他の藻類や陸上植物と大きく異なる。そこで藍藻は原核生物の細菌類と同じ仲間と見なされ、最近ではシアノバクテリア、または藍色細菌と呼ばれることが多くなっている。
藍藻細胞と葉緑体は構造的にも機能的にもよく対応することから、シアノバクテリアの祖先が進化して、葉緑体の起源となったと考えられている。
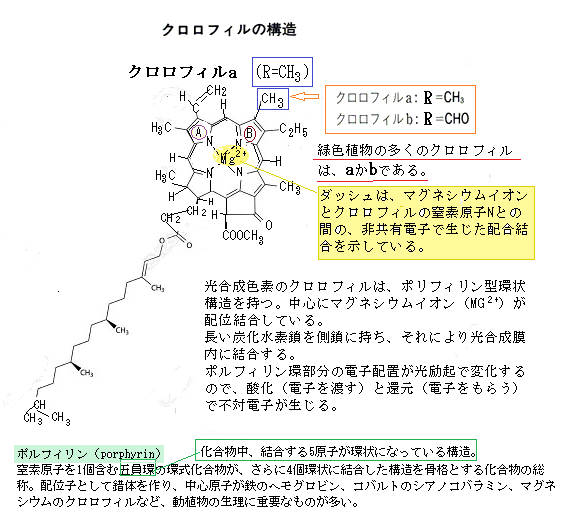
葉緑体は、独自のDNAとその複製と発現を行う系を持っている。しかし葉緑体は自律的に形成されるのではない。核DNAにコード化されたタンパク質も多数含まれているが、ミトコンドリアの進化と同様に、葉緑体は光合成微生物の細胞内共生の結果生じたと見られる。シアノバクテリアの祖先が、真核生物の宿主に取り込まれた可能性は極めて高い。緑藻類は、3つの藻類のグループのなかで最も一般的な陸上植物に近い構造と生態を持った藻類であり、光合成を行う細胞小器官である葉緑体は、種子植物やシダ植物やコケ植物といった一般的な陸上植物と同様に、緑色の色素である多量のクロロフィル(葉緑素)が含まれいる。.高等植物と緑藻類の葉緑体は、1回の細胞内共生で生じたと見られる。
紅藻類の 葉緑体の内には、クロロフィルの他に、フィコエリトリン(紅藻素)と呼ばれる赤色の色素や、フィコシアニン(藍藻素)と呼ばれる青色の色素も多く含まれることにより、 植物体の体色も、そうした三色の色素が混ざり合うことによって、紅色や紫色の体色をしている場合が多い。
褐藻類の葉緑体の内には、クロロフィルの他に、フコキサンチン(褐藻素)と呼ばれる赤褐色の色素が多く含まれている。 植物体の体色も、そうした葉緑体の内に含まれる色素の影響によって、黄褐色や黒褐色の体色をしている場合が多い。
それは、紅藻類と褐藻類の葉緑体は、少なくとも2回以上の細胞内共生で作られた体色と言える。
葉緑体のゲノムは、シアノバクテリアのゲノムより小さいが、両者のゲノムに重要な共通点がある。いずれも環状DNAで複製起点が1個、しかも遺伝子が、機能的に関連した複数の遺伝子が、共通した制御受けるように並んだオペロンoperonを形成している。進化の過程で、祖先葉緑体の遺伝子が、宿主細胞の核へ移ったり、時には完全に失われたりして、葉緑体が細胞の小器官的に働く現在のような関係になったと見られる。
真核生物では1分子のmRNAは1個のタンパク質しかコード化できない。即ち、真核細胞の mRNAは、翻訳開始点が一つなので、1つのタンパク質のコードしか読み取れない。
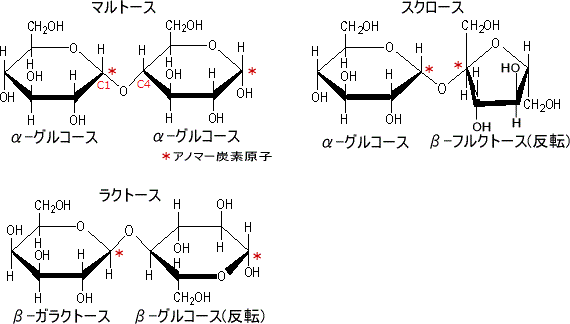 原核生物では大半のmRNAは、1分子あたり数個のタンパク質に対する読み取り枠を持っている。原核細胞のmRNAは複数の翻訳開始点を持ち、複数のタンパク質のコードを転写できる。この複数のタンパク質は、機能的に同時に発現される事が重要なものである。例えばラクトースの細胞への取り込みと、その分解を行う酵素群は1つのmRNAから翻訳される。転写調節により、必要な遺伝子群の発現を一度に調節する。このような転写単位となる隣接する遺伝子群と、RNAポリメラーゼによる認識部位となるプロモーターpromoterを合わせてオペロンoperonと言う。同一オペロン内にある各遺伝子のコードによって合成される酵素やタンパク質は、代謝あるいは機能のうえで関連し合っていることが多い。
原核生物では大半のmRNAは、1分子あたり数個のタンパク質に対する読み取り枠を持っている。原核細胞のmRNAは複数の翻訳開始点を持ち、複数のタンパク質のコードを転写できる。この複数のタンパク質は、機能的に同時に発現される事が重要なものである。例えばラクトースの細胞への取り込みと、その分解を行う酵素群は1つのmRNAから翻訳される。転写調節により、必要な遺伝子群の発現を一度に調節する。このような転写単位となる隣接する遺伝子群と、RNAポリメラーゼによる認識部位となるプロモーターpromoterを合わせてオペロンoperonと言う。同一オペロン内にある各遺伝子のコードによって合成される酵素やタンパク質は、代謝あるいは機能のうえで関連し合っていることが多い。原核生物では転写と翻訳(タンパク質合成)は同時に進行する。解糖系の酵素群のように、生物の生存に必要な最小限のタンパク質の遺伝子は、常にスイッチONの状態にあるが、タンパク質合成は多くのエネルギーを消費するので、生物にとって無駄な遺伝子の転写や翻訳は避けなければならない。そのため、多くの遺伝子のうち、どれを、いつ、どこで、どの程度発現させるかは、生物にとって最も重要な課題のひとつである。外界からのさまざまな刺激や生物が元来もっている発生・分化・増殖・加齢などのプログラムによって、個々の遺伝子のスイッチを入れたり切ったりして、転写を精妙に調節している。
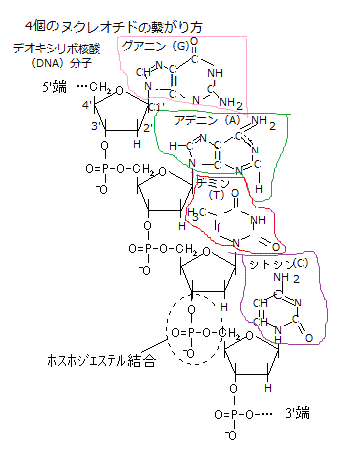 最も単純な単細胞の原核生物の細菌でさえ、遺伝子を選択し、時々に手に入る栄養源の種類に合わせて遺伝子のスイッチを入れたり切ったりして、必要な代謝酵素を作っている。
最も単純な単細胞の原核生物の細菌でさえ、遺伝子を選択し、時々に手に入る栄養源の種類に合わせて遺伝子のスイッチを入れたり切ったりして、必要な代謝酵素を作っている。転写を触媒する酵素はRNAポリメラーゼで、これには多くのタンパク質が関与する。原核生物の場合、プロモーターと呼ばれるオペロン内のヌクレオチド配列が、RNAポリメラーゼにより認識され、そのオペロン内の構造遺伝子の転写が開始される。プロモーター自体は転写されない。
多細胞の植物や動物のような真核細胞では、遺伝子発現はさらに精巧に調節されている。胚発生以降の過程では、1個の受精卵から、神経細胞や血液組織など、構造も機能も驚くほどの異なる多種類にして大量の細胞ができあがる。同じDNAから発現されたとは考えられないほどである。
北米の石炭層からは、見事なサルノコシカケの一種の化石が発見されている。デボン紀(4億800万年前に始まり3億6000万年前までの古生代4番目の時代、維管束植物の化石はデボン紀の地層に豊富)には、菌類は陸上植物に付随して上陸した。当初から陸上植物にかなり付着していたようだ。先カンブリア紀やデボン紀から既に、菌類は今日見られるような他の生物との関係を築いていた。
菌類は通常、キチンchitinが主成分となり細胞壁を形成している。単細胞で菌糸体か、その変形体である。キチンはN-アセチル-D-グルコサミンが直鎖状に結合したホモ多糖類(グルコースが重合して生成するセルロースのように、同じ単糖からできている多糖の総称)でセルロースに似た構造である。その鎖状分子は層状となり架橋を形成し軽い高強度の材質となっている。昆虫の体表面のクチクラの主要成分でもある。
1本のmRNA分子を、同時に多数のリボソームが翻訳する。それにより真核細胞の細胞質中にあるポリリボソームがタンパク質を合成する。mRNAを正確にタンパク質へと翻訳する能力は、地球上のあらゆる生物が保有する基本的な機能である。この複雑な役割を果たすリボソームやその他の分子は、ドメインが異なる生物てあっれも、そのすべてにおいて互いに酷似している。細菌と真核細胞では、RNAやタンパク質の合成方法に僅かな違いがあるだけだ。
現在使われている有効な抗生物質の多くは、細菌のRNA合成かタンパク質の合成を阻害するが、真核生物のそれらを害しない化合物である。細菌と真核生物のリボソームの構造や機能の僅かな差異を利点にして、細菌のタンパク質合成だけを妨げる化合物を、細菌を死なせるに十分な濃度にまで高めるが、人体を害するほどに至らない程度の抗生物質として投入する。個々の抗生物質は、それぞれ細菌のリボソームのどこに結合するかが決まっているため、タンパク質合成のどの過程で阻害するかは、それぞれで異なる。
現在使われている抗生物質の多くは、最初は菌類から単離された。菌類と細菌が好む生物的環境は同じであるため、生息の場では激しく競合する関係にある。菌類が登場した当初から20億年を超える細菌との熾烈な生存競争で優位に立つことが、菌類の進化の過程における最重要な課題であり続けた。菌類は発生当初から細菌を死滅させるが自分には害のない強力な毒素を常に進化させてきた。
菌類とヒトは真核生物同士である。細菌よりも両者の関係の方が近縁であるため、ヒトも脅かされる細菌の侵入に対して、菌類が開発した特効薬を借用できたのである。
酵母は単細胞の菌類で、ヒトと同じ真核生物であるが、小さく簡単な構造で、何よりも速く増え遺伝子的に操作しやすい。遺伝学の研究では大きく貢献し、細胞周期変異体の研究では著しい成果をあげた。細胞分裂を貫徹できない変異酵母によって、細胞分裂周期を制御する遺伝子のCdc遺伝子が発見された。この遺伝子とその産物タンパク質の働きが詳しく解明され、その研究者であるナースPaul M. NurseとハートウエルLeland Harrison Hartwellは、サイクリンと呼ぶ別の細胞周期タンパクを発見したハントR. Timothy Huntと同時に、細胞周期の重要な調節遺伝子を発見した業績により2,001年にノーベル生理学・医学賞を受賞した。
ナースらの実験の成果は、その後の生物学に大きく重要な貢献を果たした。例えば、非常に異なる真核生物間でも同じ役割を担うタンパク質であれば、交換しても機能することが分かった。現存するすべての真核生物では、その細胞分裂では似た方式で制御され、しかも真核生物の細胞分裂に関与する分子は、10億年以上もの進化を重ねながらも、ほぼ変化なく保存されていた。更に変異酵母は、ヒトタンパクのみならずヒトDNA断片の導入でも機能を回復した。単細胞の酵母細胞は、ヒトDNAのコードを正しく読み取り使用したのである。単細胞の酵母細胞ですら、ヒトの遺伝子に書き込まれていたコードを翻訳し、それにより完全なヒトタンパクを作るに必要な機構をすべて保持していた。真核生物のどの生物でも、どの細胞であっても、DNAコードを正確に読み取り使用する分子装置を共有していることが証明されもした。
目次へ
 すべての真核細胞は核を持つが、核を持つ細胞すべてが、多機能的な役割を果たす各種の細胞小器官を備える。その殆どが膜に包まれていることも、真核生物すべてに共通する。
すべての真核細胞は核を持つが、核を持つ細胞すべてが、多機能的な役割を果たす各種の細胞小器官を備える。その殆どが膜に包まれていることも、真核生物すべてに共通する。細胞は、生物を構成する微小な容器に入った自己複製システムと言える。容器にあたる細胞膜は、タンパク質が点在する極めて薄い脂質膜plasma memmbraneなので、光学顕微鏡では直接観察はできない。その構造は、細胞の周囲を取り囲む、主成分が脂質分子からなる厚さ約5nm、原子数で言えばほぼ50個分の、脂質二重層の薄い膜にタンパク質がはめ込まれだけの一見単純な機構に見える。以前には細胞壁も細胞膜と呼ばれていた時代もあったぐらいである。
細胞膜より細胞壁の方が、厚みがある。また、すべての細胞に細胞膜があるが、植物の細胞には細胞膜の外側に細胞壁がある。骨格がない植物は、細胞壁で生体を支える。細胞膜より強く隣りの細胞とくっつくことができるため、堅い 樹木の茎や枝などを作る。動物の細胞には、細胞膜、植物の細胞には細胞膜と細胞壁の両方がある。
細胞膜を用いて、細胞は、内部の化学成分を外部に流出するのを防ぐだけでなく、細胞膜がなければ生命活動ができなくなるほど、複雑で精妙な働きをする。細胞膜は、細胞の内側と外側を区分する境界であるばかりか、分解酵素のような危険なものや毒物的なものに対してはバリアとして内部への侵入を防ぐなど、物質の選択透過性や信号伝達、代謝反応物の濃度を上げることによる反応の加速など、細胞機能において本質的な役割を果たす。
細胞が生き続け、その生命体が成長するには、栄養素が膜を通って入り込み、その生合成反応から生じた老廃物を排出する重要な役割を果たす必要がある。そのため細胞膜は、タンパク質でできた選択性が極めて高いチャンネルと輸送タンパクを備え、特定の小分子やイオンを取り込んだり、排出したりする。また、膜には、細胞が環境変化の情報を受け取って適切に対応するセンサーや、受容体となるタンパク質も含まれている。
細胞膜の受容体タンパク質で、細胞は外部からのシグナルを受け取る。細胞が有する力学的な特徴も重要で、細胞の成長や変形に伴い、膜自体も新しい膜を付け加えて膜面積を拡張して、繋がったまま切れ目を作らず形を変えていく。細胞膜の柔軟性と拡張能力により、細胞は成長と変形を重ねながら運動する。また細胞膜に穴が開いても、裂けたり萎んだりせず、直ちに穴は塞がれる。
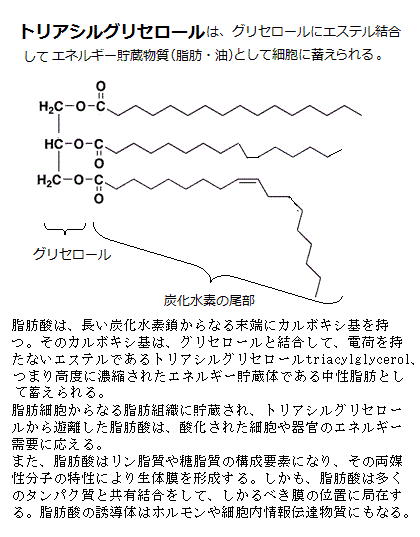 最も構造が簡単な細菌には、膜は細胞膜の一種類しかない。真核細胞には、細胞内区画を取り囲む細胞内膜もあり、小胞体やゴルジ体の膜など、そしてミトコンドリアや葉緑体の外膜と内膜など、様々な細胞小器官organelleを包み小区画を作っている。細胞内膜も、基本的には脂質二重層lipid bilayerの薄い膜構造をしていると考えられている。すべて脂質とタンパク質から組成されるが、僅かな違いは、特に膜に含まれるタンパク質群が異なることである。
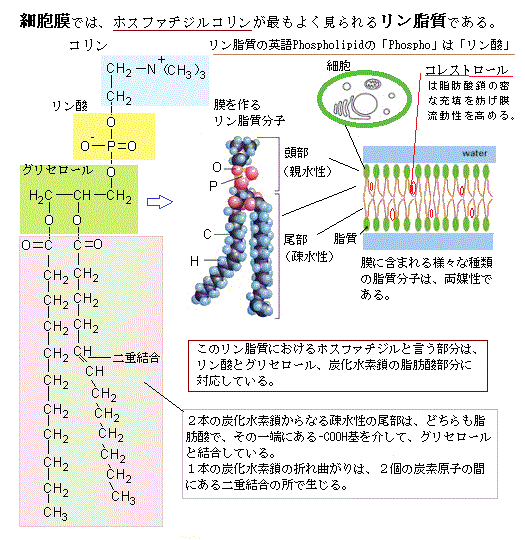
最も構造が簡単な細菌には、膜は細胞膜の一種類しかない。真核細胞には、細胞内区画を取り囲む細胞内膜もあり、小胞体やゴルジ体の膜など、そしてミトコンドリアや葉緑体の外膜と内膜など、様々な細胞小器官organelleを包み小区画を作っている。細胞内膜も、基本的には脂質二重層lipid bilayerの薄い膜構造をしていると考えられている。すべて脂質とタンパク質から組成されるが、僅かな違いは、特に膜に含まれるタンパク質群が異なることである。細胞膜は、すべて脂質とタンパク質からなり、基本構造は同じである。脂質はシート2枚が重なる脂質二重層を作る。この脂質二重膜が、殆どの水溶性分子を透過させない障壁の役割を果たしている。生体膜を作っている脂質の殆どは、リン脂質と糖脂質で、多くの細胞膜で見られる均一に分散するコレステロールも含んでいる。またリン脂質や糖脂質は、脳神経系にも多く存在している。
無機イオンや小さな水溶性の分子が膜を通過する。この移動を主導するのが輸送体とチャンネルである。その輸送体は形を変えて、小型の有機分子や無機イオンを膜の片側から反対側に運ぶ。チャンネルは膜を貫通する小さな親水性の小孔を作り、輸送体が運ぶ物質を拡散により通過させる。チャンネルの殆どは、無機イオンだけを透過させるからイオンチャンネルと呼ばれる。イオンは電荷を持つので、移動すると膜の内外に大きな電位差を生じさせる。この電位差が神経細胞の情報伝達に関わり人間の行動として表現される。
コレステロールは、脂質二重層のリン脂質分子の間にある隙間に収まり、細胞膜に剛直化された領域を作る。また、タンパク質は、それ以外の膜機能を担い、それぞれの膜に固有の性質を与えている。
細胞膜は、2本の疎水鎖と1つの極性頭部を有する両親媒性物質で構成されている。尾部の炭化水素間に二重結合がある部分では、尾部が折れ曲がる。水溶液中では、親水性基の頭部は水分子に引き寄せられて表面に出る。疎水性の尾部は水分子を避けるため、内側に封じ込められ他の疎水性同士で疎水結合をする。尾部が水分子を避ける疎水性のシッポを持つため、これにより細胞膜が二重層構造で一番安定することになる。親水性頭部には極性があるので水分子と水素結合を形成するが、疎水性尾部は無極性なので、疎水性の尾部が周りの水分子を避けることにより生じる疎水結合によって結果的に形成される。こういう集合体をミセルと言う。
核は真核細胞の中で最も目立つ細胞小器官であり、2枚の同心円状の核膜に包まれ、中にはDNA分子があり、生物個々の遺伝情報を暗号化する極めて長い重合体を作っている。細胞がまさに2つの娘細胞に分裂する時、DNAの巨大分子が次第にひも状の染色体chromosomeとなって密に凝縮するため光学顕微鏡で観察できるようになる。
目次へ
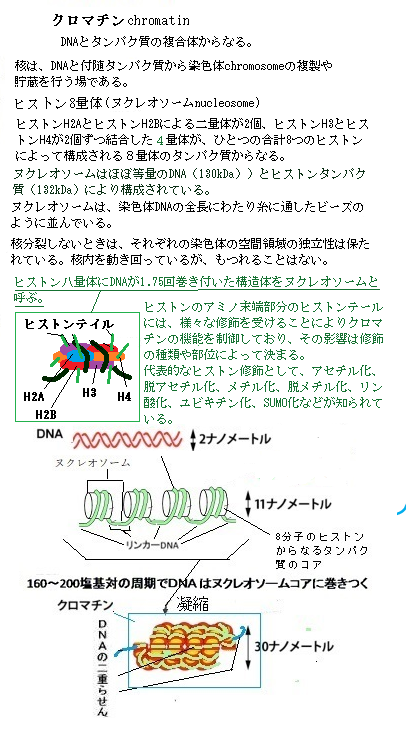 原核細胞でもDNAは遺伝情報をコード化している。ただ核膜がないため細胞質内では、独立した領域と見られていない。そのため原核生物prokaryoteは核を持たない、と言われる。
原核細胞でもDNAは遺伝情報をコード化している。ただ核膜がないため細胞質内では、独立した領域と見られていない。そのため原核生物prokaryoteは核を持たない、と言われる。真核生物euprokaryoteには核と言う構造を持つ。その英語の名前が由来である。真核生物には動物・植物・菌類・原生生物protist(アメーバ・ゾウリムシ・マラリア病原虫など単細胞の真核生物の総称)など様々な種類があるが、核は、2mもあるDNAのひも状の繊維が、ヒストンと言うタンパク質としっかり結合して約数10㎛(1m=106µm)程度に凝縮し、核膜の中に収納されている。原核生物のDNAは、完全に裸でないにしても、ヒストンがないためクロマチン構造を作っていない。
原核生物の大半が単細胞で、その細胞にはDNAがあっても真の「核」がない。DNAは原形質内でループとして存在する。他の特徴としては、葉緑体chloroplastやミトコンドリアが含まれず、小さなリボソームribosomeが存在する。リボソームはタンパク質合成の場で、DNA上の情報は、いったんメッセンジャーRNA(mRNA)に転写され、翻訳という過程を経てタンパク質を合成する。この翻訳で重要な働きをするのがリボソームとトランスファーRNA(tRNA)である。
真核細胞の大きさは、約直径30㎛程度と大きな構造体となっている。ただ単細胞の原生生物の仲間のゾウリムシの大きさは200~300㎛もあり、アメーバも、100~600㎛と大きい。魚や鳥の卵の黄身も1つの卵細胞である。ダチョウの卵は75 mmもある。ヒトの卵細胞は140µmである。ただ卵は大きくても、大部分は栄養物が詰まっていて、生きている部分それ程大きくない。
ヒトの細胞を、単独でシャーレの中で培養すれば、増殖するばかりか細胞としてそれなりの機能を果す。原核生物の殆どは直径1~5㎛程度と比較的小規模な構造となっているが、中には、その100倍以上大きい原核生物の種もいる。原核生物は、連鎖球菌などの球形か、大腸菌やサルモネラのような桿状か、梅毒トレポネマのようならせん形をしている。いずれも、細胞壁と言う頑丈な保護外被を持つものが多く、その下にある細胞膜が細胞質とDNAを含んだだけの1つの区画を包んでいる。
原核細胞は、ねずみ算式に分裂して増殖する。豊富な栄養条件であれば、多くは20分ほどで2個になり、11時間もあれば、その子孫は80億以上になり、現在の地球上の全人口を上回るようになる。
原核細胞が、ねずみ算式に増殖する成長能力は、栄養源となる食物が豊富であることが前提で、限りある食物は一般的に、原核細胞の急激な増殖により、豊富にあった食物は瞬く間に消尽される。同一の個体同士が、限られた資源を求めて競合するばかりか、その周辺の生活圏にある生物群は、好条件であれば侵入し、その勢力も自ずと広がり競合する。そのため増殖条件は、自ずと短期となり悪化する。生物全体が、限られた資源を求めてしのぎを削る。その時々の自然選択に勝ち抜いた変異体が、他の個体が利用しないものを食物とするなど、激変する環境に適応する変異体だけが、選択され種として残存することになる。
細菌は、環境の変化に反応する。例えば、ダンゴイカの発光器官に共生する発光バクテリアluminescent bacteriaのVibrio fischeriのコロニーにでは、菌の生息密度がある程度高くなると、その密度を感知する回路があり、それにより発光するようになる。個々の菌が環境中に低分子を放出すると、他の細菌細胞が取り込むと情報伝達カスケードが機能して、特定の遺伝子が発現するようになる。「カスケード」とは、シグナル伝達には多彩な経路があるが、一般には細胞膜上の受容体に、細胞外シグナル分子が結合すると、これに引き続き、セカンドメッセンジャーや酵素などにより、細胞内の因子が次々にシグナルを受け渡し、その過程が進むにつれ、関与する酵素や分子の数が増大していく。最終的には細胞の機能変化や核内の転写因子による特定遺伝子の転写調節、アポトーシスによる細胞死などを起こす。このような反応の連鎖を「カスケード」と呼ぶ。
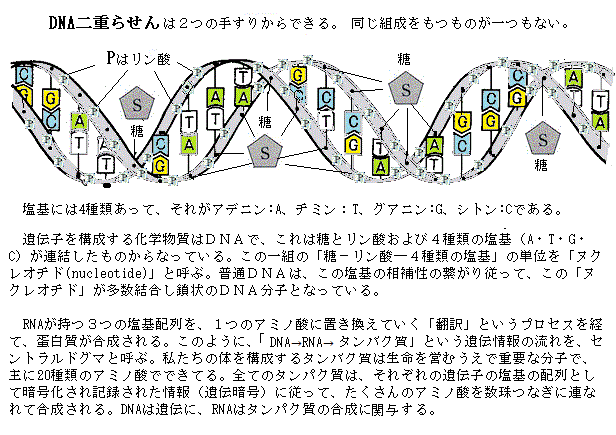 例えば、原核細胞が、代謝や環境変化に反応する多くは、遺伝子の発現を変化させて行う。遺伝子の発現は、RNAに転写されて、殆どの場合はタンパク質に翻訳される。ゲノムには、何千個もの遺伝子が存在しているが、その一部は常に発現する恒常的(構造的)発現constitutive expressionであるが、他の多くの遺伝子は、特定の環境と生理条件にある時に調節的発現regulated
expressionをする。細菌の遺伝子の中には、栄養素の供給条件や環境条件に応じて、発現量が1,000 倍も以上も変化するものがある。
例えば、原核細胞が、代謝や環境変化に反応する多くは、遺伝子の発現を変化させて行う。遺伝子の発現は、RNAに転写されて、殆どの場合はタンパク質に翻訳される。ゲノムには、何千個もの遺伝子が存在しているが、その一部は常に発現する恒常的(構造的)発現constitutive expressionであるが、他の多くの遺伝子は、特定の環境と生理条件にある時に調節的発現regulated
expressionをする。細菌の遺伝子の中には、栄養素の供給条件や環境条件に応じて、発現量が1,000 倍も以上も変化するものがある。 原核生物と真核生物の遺伝子調節機構は、多くの類似点がある一方、根本的な相違点もある。原核細胞の集団の進化は速く、新しい栄養源を利用する能力や新しい抗生物質への抵抗性を持つものが直ぐに現れる。
原核生物の遺伝子発現の調節は、最初に、また主として転写の段階で行われている。ある遺伝子が転写されるかどうかは、DNAの特異的配列の部位と、それに結合する特異的タンパク質との相互作用が関わっている。最も多いのが、特異的タンパク質が、ある特異的な遺伝子のプロモーターへRNAポリメラーゼ(RNA polymerase)が接近するのを妨げ、その発現を阻止する方法である。
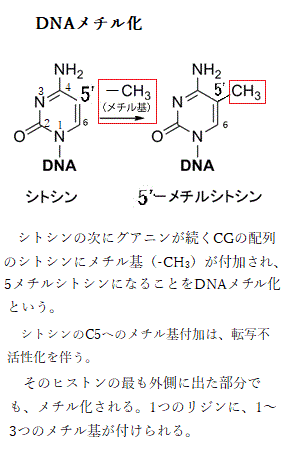 RNAポリメラーゼ酵素は、DNAの2本鎖をほどき、RNA鎖へ遺伝的情報を転写transcribeする精巧な仕事を行う。
RNAポリメラーゼ酵素は、DNAの2本鎖をほどき、RNA鎖へ遺伝的情報を転写transcribeする精巧な仕事を行う。細菌もポリリボソームを使う。真核生物より合成速度は、はるかに速い。mRNAにプロセシング(転写されたRNAが,酵素的切断や修飾などを経て,成熟したmRNA分子に変換される過程を言う)の必要がなく、しかも合成中のmRNAにもリボソームが接近できるからである。通常、細菌では、mRNAの転写完了の前に、その遊離末端にリボソームが結合して翻訳を開始する。DNAに沿って進んでいくRNAポリメラーゼのすぐ後ろを、リボソームが進んでいく。
原核生物の中には、逆に結合したタンパク質が、遺伝子の発現を活性化することもあり、協調させながら一群の遺伝子を調節する方法もある。また遺伝子の中には転写された後に調節されるものもある。
SUMO(スモ)修飾
エピジェネティクスの研究分野が近年、多くの生命科学に関する研究と関わりを持ちながら横断的に急速な広がりをみせている。翻訳後修飾の研究はエピジェネティックな現象の核心をつくもので、また、翻訳後修飾に関わる修飾酵素を制御する低分子化合物は、薬効として多くの可能性を秘めている。
DNAのコードを読み取る、DNAに直接結合する転写因子以外にも、その翻訳後修飾に関わるヒストン修飾酵素や染色体構造調節因子など様々な機能をもつ転写共役因子群が、協調的に厳密に制御されて働いている。
更に、核マトリクスや核膜、核膜孔などの核の基本的骨組みとなるタンパク質自体も、クロマチンと相互作用することで転写調節に関わっている。翻訳後修飾の中で、とりわけクロマチンや核膜の機能制御に関わるユビキチン様タンパク質SUMOとSUMOによる分子修飾、およびSUMO化を触媒する酵素活性を有する転写因子 、ユビキチン化やアセチル化、メチル化など、生化学や細胞生物学的アプローチからの研究成果が着目されている。
SUMOはSmall Ubiquitin-related Modifierの略である。つまり、その英語名で端的に表現されているようにSUMO化は、ユビキチンと構造が良く似た約100のアミノ酸残基からなる低分子量のSUMOタンパク質が、E1・ E2・ E3と呼ばれる3つの酵素によって、標的タンパク質の特定のLys残基にイソペプチド結合で付加されるタンパク質による翻訳後修飾のことである。
SUMOはヒトのみならず、動物や酵母から植物にまで及ぶ多くの生物種で観察されるタンパク質である。
SUMO修飾には、SUMOが一つの置換基と結合するモノSUMO化修飾のほか、SUMO分子同士が重合しポリマー鎖を形成するポリ SUMO化修飾がある。
近年のSUMO化基質を中心とした細胞生化学的解析や、遺伝学的な手法を用いた研究から、モノSUMO化およびポリSUMO化修飾が細胞増殖や分化の制御、神経細胞における細胞内封入体の形成といった生命活動の幅広い領域で深い関連性があることが分かった。
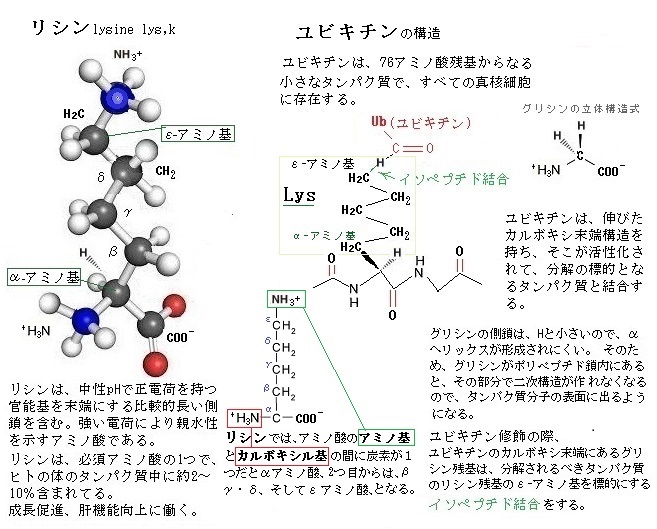 また、細胞内の多くのタンパク質のアミノ酸配列中にSIM(SUMO-interacting motif)と呼ばれるアミノ酸が含まれており、SIMを含むタンパク質はSUMO化したタンパク質と相互作用して、SUMO修飾に依存する複合体の形成を制御している。一般に細胞内のタンパク質はタンパク質同士が集合したり、会合したりすることで複合体を形成する。また、集合した複合体は分散もする。SUMOとSIMの相互作用はこうした動的な平衡状態を、どちらか一方に傾斜させる。
また、細胞内の多くのタンパク質のアミノ酸配列中にSIM(SUMO-interacting motif)と呼ばれるアミノ酸が含まれており、SIMを含むタンパク質はSUMO化したタンパク質と相互作用して、SUMO修飾に依存する複合体の形成を制御している。一般に細胞内のタンパク質はタンパク質同士が集合したり、会合したりすることで複合体を形成する。また、集合した複合体は分散もする。SUMOとSIMの相互作用はこうした動的な平衡状態を、どちらか一方に傾斜させる。複合体の形成に関わることで、SUMO修飾は、遺伝子発現やタンパク質の安定性とタンパク質の細胞内局在、タンパク質間の相互作用などに影響を与え、様々な細胞応答の制御に関わっている。しかもDNA複製やDNA修復などでも多くの反応を調節してようだ。
特に、SUMO-SIMによる制御破綻は、高等動物における発生異常を起こし、ヒトでは老化に伴うがん発症や神経変性疾患など顕著に現れる。
目次へ
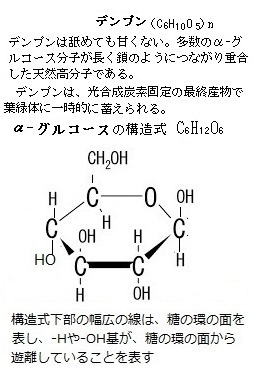 生化学は生命現象を化学的に研究する学問である。生命現象では様々な分子の相互作用がおこるが、これらの分子は大きく分けて、タンパク質や核酸のような生体高分子biological
macromoleculeと呼ばれる大きな分子と、生命現象の過程で化学的に変化させられる、グリコースやグリセロールのような代謝産物metaboliteと呼ばれる低分子量の分子の2つに分けられる。
生化学は生命現象を化学的に研究する学問である。生命現象では様々な分子の相互作用がおこるが、これらの分子は大きく分けて、タンパク質や核酸のような生体高分子biological
macromoleculeと呼ばれる大きな分子と、生命現象の過程で化学的に変化させられる、グリコースやグリセロールのような代謝産物metaboliteと呼ばれる低分子量の分子の2つに分けられる。生体高分子や代謝産物も僅かな違いはあるが、あらゆる生物に共通している。例えば、すべての細胞性生物の遺伝情報は、デオキシリボ核酸deoxyribo nucleic acidに保存され、重要な高分子のタンパク質であっても殆どの生物を構成する20種類のアミノ酸からできている。この成分は、あらゆる生物で共有し、しかも似たような役割を持つタンパク質の単量体であり、違う生物のものでも立体構造はよく似ている。
特に植物が光エネルギーを捉える際に起きる生化学反応は、動物がグルコースの分解で発生するエネルギーを捉える過程と極めて似ている。
生化学反応に伴って、熱が発生したり吸収されたりする。反応に伴って熱を放出する場合を発熱反応と言い、この場合、物質が持つ化学エネルギーは減少する。 反応に伴って熱を吸収する場合を吸熱反応と言い、物質の化学エネルギーは増大する。 放出されるエネルギーが熱だけではない 、化学エネルギーの場合が多いため、ギブズ自由エネルギーGibbs free energyという上位の概念を導入する必要が出てくる。物理学のエネルギーや「仕事」の単位である「エルグerg」の語源でもあるergonは、ギリシャ語εργονでは「仕事」を意味する。ギブズ自由エネルギーGibbs free energyを、単にGibbs energy と呼ぶこともある。通常は G で表される。
生きている生物は、ギブズエネルギーを継続的に投入する必要がある。アメーバ運動・繊毛運動・鞭毛運動・原形質流動や、平滑筋・横紋筋の筋収縮など細胞運動など力学的な仕事をする場合や、分子やイオンを能動輸送する際、あるいは単純な前駆体から巨大分子や他の生体分子を合成するなど、ΔG=0の平衡状態からかけ離れた状態で生化学反応するためには、ギブズエネルギーを環境から取り入れる必要がある。
光合成栄養生物が光エネルギーを化学エネルギーに変換する能力を獲得したことにより、その後の生物進化と競合で画期的な優位性を勝ち取ったと言える。光合成生物は、太陽光を利用してH2Oを酸化してO2とプロトンを作り、これを原動力にしてATPとNADPHを合成する。
 地質学的証拠から、酸素非発生型の光合成は、地球生命体が登場した35億年前の草創期の早期に出現している。光合成細菌は大きく、「紅色硫黄細菌」「緑色硫黄細菌」「紅色非硫黄細菌」の3つに分けられる。光合成細菌は、水田や河川、海岸の土、下水処理場など、水溜りがあれば殆どの場合存在している。その最適な生育温度は約30℃と言われているが、水温0℃の南極の氷の下や、90℃にもなる熱水でも生息が確認されている。耐塩性にも優れ、食塩濃度が30%にもなる塩水湖にも存在する。始原生物に近く、現在も生息している光合成細菌は、大きな環境変化を潜り抜け生きてきた、実に環境適応能が高い微生物と言える。そのため、光合成細菌は、一定の条件が整えば水質浄化に有効であることが、多くの研究者により発表されている。
地質学的証拠から、酸素非発生型の光合成は、地球生命体が登場した35億年前の草創期の早期に出現している。光合成細菌は大きく、「紅色硫黄細菌」「緑色硫黄細菌」「紅色非硫黄細菌」の3つに分けられる。光合成細菌は、水田や河川、海岸の土、下水処理場など、水溜りがあれば殆どの場合存在している。その最適な生育温度は約30℃と言われているが、水温0℃の南極の氷の下や、90℃にもなる熱水でも生息が確認されている。耐塩性にも優れ、食塩濃度が30%にもなる塩水湖にも存在する。始原生物に近く、現在も生息している光合成細菌は、大きな環境変化を潜り抜け生きてきた、実に環境適応能が高い微生物と言える。そのため、光合成細菌は、一定の条件が整えば水質浄化に有効であることが、多くの研究者により発表されている。
紅色非硫黄細菌の光合成機構は、その後に登場する酸素発生型の光合成機構と大部分で共通している。緑色硫黄細菌が行なう光合成反応も、明らかに酸素発生型よりも早期であるが、紅色非硫黄細菌以上に、酸素発生型と共通している。緑色硫黄細菌の光合成反応では、H2Sなどの還元型硫黄化合物が光合成全体としての電子供与体となる。
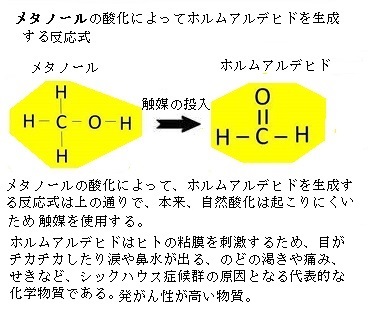
CO2 + 2H2S 光➡ (CH2O;ホルムアルデヒド)+2S+H2O
(CH2O;ホルムアルデヒドは、メチルアルデヒドとも呼ぶ。融点-92℃、沸点-20℃であるから、常温では無色透明の気体であり、しかも水によく溶ける。有機物の燃焼や光化学反応からも生成される。水溶液はホルマリンと呼ばれ、消毒薬や防腐剤として使われ、合成樹脂・塗料・インク・接着剤などの原料としても使われる)
「緑色硫黄細菌」と「紅色硫黄細菌」の光合成の電子供与体は、H2,H2S,Sである。
光を化学エネルギーに変換する能力は、生物誕生のごく近い早期から現れていた。しかも、それぞれの光化学系は、構造的に共通しているから、進化的に共通の起源を持っていると見られる。酸化的リン酸化とその構成、そして分子機構が類似しているため、光合成機構は初期のエネルギー変換機構が進化したことによると考えられる。
生命は、本来、光合成機構を備えて誕生したわけではない。アーキアの仲間は光合成反応の能力を持たない。光合成の能力は、アーキアと真正細菌が共通の祖先から分岐した後に、真正細菌だけの進化として現れている。一方、電子伝達系は、アーキア・真正細菌・真核生物の生物界3ドメインすべてが共有していた。
効率の良いエネルギー生産が、地球上の生命の進化に大いに貢献してきた。しかも、エネルギー生産とATP合成を行なう効率のよい機構が、生物の歴史の初期に出現していた。 むしろ、その機能があることにより、その仕組みは、細胞膜における電子伝達にも応用されている。その以後の進化が、今現在でも、地球上の生命が生存していくための中心的な仕組みとなっている。
細胞は、膜を使って行われるこの機構により、様々な材料からエネルギーを獲得する。光合成による光エネルギーの化学結合エネルギーへの変換や、細胞呼吸(cellrespiration)により食物分子から大量のATP生産などで、この仕組みが重要な役割を果たす。 膜における電子伝達は、最初は細菌において30億年前に出現した。その細胞の子孫たちは、現在、地球上の多種多様な生命体に進化し、陸上と水中のあらゆる場所に生存している。かつて取り込まれた真核細胞内にある葉緑体とミトコンドリアが、生命体の自律性を維持するためには不可欠な存在となっている。
Q-シトクロムcレダクターゼやシトクロムbfファミリーなどは、呼吸と光合成両方の電子伝達系に含まれている。つまりこれらの成分が、光エネルギー捕捉機構の進化の土台になっている。
酸素発生型の光合成生物が活発化したのは、現段階の地質学的証拠から約20億年前と考えられている。約20~24億年前、大気中の酸素濃度は殆どゼロの状態から現在の1/100以上のレベルにまで急激に上昇し、生命進化に決定的なな影響を与えた。酸素濃度の上昇が、約23億年前の大氷河期から温暖期への気候回復時に起きていた。急激な温暖化が、光合成生物の大繁殖となって、酸素が大気に広がっていった。
進化の過程で互いに分岐し何十億年を重ねた。好熱性アーキアやシロイヌナズナ、ヒトなどの異なる3種類の生物、特に「アーキア」は古細菌で、バクテリアや真核生物Eukaryoteとは30~40億年前に分岐したと考えられている。その古細菌アーキアは、酸素が少しでもあると生きられない微生物、温泉や海底熱水噴出孔周辺から噴出される90℃以上でも 生育できる微生物(水の沸騰温度付近で生育する「超好熱菌」が生産するタンパク質は、常温生物由来のタンパク質に比べて高い熱安定性を示す)、イオウや水素などの無機物からエネルギーを得て生きている微生物など特異な 種を多く含んでいる。それでも3種類の生物の、遺伝子調節の鍵となるTATAボックス結合タンパク質(TATA-binding protein)の分子の形はよく似ている。
プロモーターと転写の開始点は、DNAの塩基配列にある。DNAの塩基配列にはアミノ酸配列をコードしている領域と、転写の調節に関与する領域がある。調節領域には、タンパク質が結合するための目印が塩基の4文字で書きこまれている。RNAポリメラーゼが結合するこの領域は、開始コドンinitiation codon(各アミノ酸に対応する3つの塩基配列,ATG)のすぐ上流にあり、プロモーターと呼ばれている。真核生物では、このプロモーター領域のうち、開始コドン上流30塩基を中心にTATAAAという配列が共通して存在する。そのため、この領域のことをTATA boxと呼んでいる。転写の開始は、まずTATA boxに転写因子である「TATAボックス結合タンパク質」が結合することから始まる。これを目印に次にRNAポリメラーゼやその他の転写因子が結合し、その転写開始点からの転写が開始される。RNAポリメラーゼが、転写終了を示す終結コドンtermination codonまで達すると、転写は終了する。プロモーターはRNAポリメラーゼの着地点であるとともに、この酵素がDNA上を滑っていく方向も規定する。したがって、二本鎖のうちのどちらが鋳型鎖になるかは、プロモーターの配置によって決まる。
生物学は分析中心の科学から、作り出す化学へと変貌した。組換えDNAの技術の発展は、全く関係がない遺伝子同士の新たな組み合わせを、研究室で作り出せるようになった。その新たに組換えられた遺伝子は、適切な宿主細胞へ導入すると、その細胞のDNA合成機構によって複製され、クローンclone化されて何倍にも増殖される。挿入された遺伝子は、その新しい環境で転写・翻訳されため、宿主の遺伝的性質を当初の意図した通りに永久に変えていく。
DNAクローニングとは、あるDNA塩基配列の複製をたくさん作ることを言う。クローニングとは、生物学では、一つの細胞または個体から、全く同一の遺伝子構成をもつクローンを作成すること言うが、DNAクローニングでは、ある特定の遺伝子を単離して増やすことを言う。組換えDNA技術の開発により、ゲノムからDNAの任意部位をクローニングできるようになり、ゲノム内のDNAの各部位の機能も理解できるようになった。この組換えDNA分子recombinant DNA moleculeの作出により、細胞内部から得られる分子を活用できるようになった 。
人類は数千年も前から、選抜育種により、それとは気づかずDNA組換えの実験を続けてきた。しかし、1,970 年代に組換えDNA技術が開発されるまでは、遺伝子に直接手を加えて期待される性質を備えた生物の作出までは無理だった。
個々の遺伝子を取り出して操作することは難しい。タンパク質と違い遺伝子は細胞内では、独立した存在ではない。大きなDNA分子のごく一部であり、真核生物ほど複雑ではないが、大腸菌のゲノムさえも460万塩基対で構成されるため、極めて長い。更に長い大きな真核生物であれば、ゲノムから一個遺伝子を取り出せなければ実験室では扱えない。
この問題を解決したのが、制限酵素restriction enzyme(制限ヌクレアーゼ)と呼ばれる一群の細菌酵素の発見であった。細菌は、バクテリオファージbacteriophage(細菌を標的として感染するウイルスの総称。 バクテリオファージという名称は「細菌を食べる者」という意味)の感染など、外からの侵入に対して身を守る防御機構を備えており、外来の DNA を自分自身が持つエンドヌクレアーゼrestriction endonucleaseによって、DNAの特定の塩基配列を認識して切断する、これにより微生物の酵素を分解し、ファージの増殖を制限 restrictionする。この制限に関わるエンドヌクレアーゼが制限酵素であり、制限エンドヌクレアーゼとも呼ばれる。
この制限酵素は、細菌の菌株間でのDNAの移動を制限する働きをする。生物が保有する一見不可解な、この酵素の謎の研究により、細胞や分子の生物学における研究法を一変させる技術開発の引き金となった。
この一群の細菌酵素の発見が画期となり、その後の生物学の研究に大きく貢献した。制限酵素は二本鎖DNAを特定の塩基配列を標的にして切断する。制限酵素を使えばゲノムから特定される塩基配列の場所で切断でき、それを分離検出し、調べたいDNA塩基配列を含んだ断片を同定し、その遺伝子コードを読み解く。
菌種によって制限酵素の種類は異なり、それぞれが異なった特異的な塩基配列で切断する。制限酵素の標的になる塩基配列は通常4~8塩基対なので、長いDNA分子には、多数の切断部位がある可能性が高い。
各制限酵素は、ある特定のDNA分子を必ず同じ部位で切断するので、あるDNA試料を特定の制限酵素で処理すると、毎回同じ組成のDNA断片の集団ができる。制限酵素はDNAを特異的塩基配列で切断するため、その断片の大きさは決まっているのである。制限酵素は、主に細菌から得られるので、その名称は菌種に由来する。例えば、EcoRI(エコアールワン)は、大腸菌Escherichia coli(èʃəríkiə kóulai)から単離された酵素である。
生物の全ゲノムを扱うとなれば余りにも大き過ぎる。実験室での遺伝子研究の第一歩は、ゲノムを壊して小さくし扱いやすい断片にすることであった。これらの断片を繋ぎ合わせて、組換えDNA分子を作り増幅することができる。哺乳動物の細胞内では、全ての遺伝子の数はつねに厳密に一定になるように仕組まれているが、細菌や植物などでは、正常な発生過程で特定の遺伝子の数が増える場合がある。これが遺伝子増幅である。
組換えDNAを扱うのに欠かせないのがベクターvectorである。ベクターは適切な宿主中で自律的に複製できるDNA分子で、目的のDNA断片と共有結合して、簡単に受容細胞へと運べるように設計されている。
天然に存在する環状DNAで、寄生染色体として細菌中に見られるプラスミドplasmidや、バクテリオファージλ(λファージ)と言うウイルスは、E.coliなどの細菌のDNAの組み替えによるクローニング(分子生物学では、ある特定の遺伝子を 単離結合して、遺伝子を増やすことを意味する)に適したベクターである。
ベクターに新しいDNA断片を組み込むには、ベクターの特異的認識部分を一か所、制限酵素で切断する。この酵素により互いのDNAの二本鎖それぞれが、互い違いにずれた位置で切断される。これにより相補的な一本鎖部分を持つ末端が生じる。この末端は互いに親和性を持つことから、付着末端あるいは粘着末端と呼ばれる。
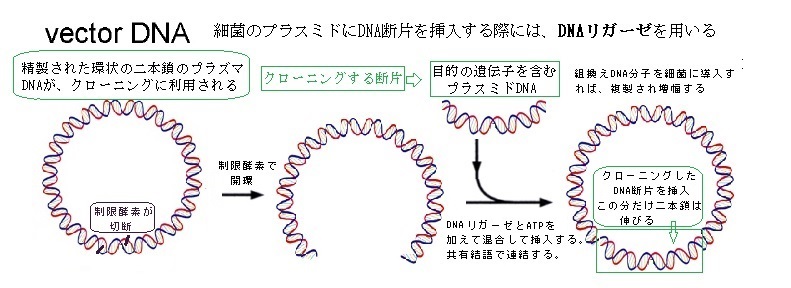 これと同じ付着末端を持つDNA断片なら、どのようなものでもプラスミドに挿入できる。挿入された断片は、プラスミドDNAの開環に使われた同じ制限酵素を使って、より大きなDNAが作られる。得られたDNA断片の末端と、切り開かれたプラスミドの分離した核酸の末端は相補的なので、互いに相補鎖同士を認識してアニーリングannealingが生じ、自然に再会合して二本鎖が形成される。DNAの二重らせんの切断と再会合が容易にできることにより、核酸の生物学的機能の活用が飛躍的に拡大した。
これと同じ付着末端を持つDNA断片なら、どのようなものでもプラスミドに挿入できる。挿入された断片は、プラスミドDNAの開環に使われた同じ制限酵素を使って、より大きなDNAが作られる。得られたDNA断片の末端と、切り開かれたプラスミドの分離した核酸の末端は相補的なので、互いに相補鎖同士を認識してアニーリングannealingが生じ、自然に再会合して二本鎖が形成される。DNAの二重らせんの切断と再会合が容易にできることにより、核酸の生物学的機能の活用が飛躍的に拡大した。この再生過程をアニーリングと呼ぶ。
従って、DNA断片をプラスミドベクターに挿入するには、精製したプラスミドDNAを1か所で切断する制限酵素で開環し、同じ制限酵素で切断したクローニングしたいDNA断片を、DNAリガーゼとATPを加えて混合して挿入する。すると付着末端同士で塩基対を形成し、DNA主鎖の切れ目をDNAリガーゼが連結して組換えDNA分子が完成する。その出来上がった組換えDNA分子を細胞に導入すれば、複製され増幅する。
ある種の細菌が周囲に存在するDNA分子を自然に取り込む性質を利用して、組換えDNA分子を細菌細胞へ導入する、この取り込み制御機構を「形質転換transformation」と呼ぶ。形質転換は裸のDNA分子を直接細菌に取り入れることにより起きる。形質転換植物transgenic plant、特に農作物ではGM作物genetically modified organismと呼ぶこともある。
ある生物から取り出した、あるいは合成したDNA分子を染色体上に組み込んで性質を変化させた植物で、導入された外来DNA断片は、植物個体を形成するすべての細胞の同一染色体上に1~数個のDNA断片が組込まれている。
遺伝子がDNAでできている最初の証明は、肺炎球菌の病原性菌株から精製したDNAを用いて、無害の細菌を致死性細菌に変える実験から得られた。ある細胞株の形質が、別の細胞株に変化することが観察され、生物学の研究が分析中心の科学から、開発する化学へと変貌する契機となった。
自然界の細菌集団では、死んだ細胞が環境に放出した内容物に含まれるDNAが自らの形質転換の素材に利用されている。現に、試験管の中の大腸菌などの細菌に、実験室で作られた組換えDNA分子を取り込ませることができる。しかも、この細菌を栄養豊富な液体培地で増殖することもできる。
細菌集団は、30分ごとに2倍に増える。そのたびに組換え分子も2倍になる。24時間もすれば、目的のDNA断片を持つプラスミドが数億個もできる。この細菌を溶かして得られたプラスミドDNAを、より大きな細菌細胞内で増殖させる。そのクローニングのためには、DNA断片をプラスミドベクターに挿入する。それにより作られた組換えDNAを細菌に挿入すると、その細菌が増殖するに伴いプラスミドが数百万個も複製される。
上記の事例は、1個のDNA断片の増幅であるが、全ゲノムを制限酵素で切れば、数百万個の異なるDNA断片が生じる。この中から調べたいDNAを持つ1個の断片を取り出すためには、回収した全DNA断片をプラスミドベクターに挿入する際に、個々のプラスミド分子にDNA断片1個のみ挿入する。この組換えプラスミドを、大腸菌1個当たり1個だけプラスミドを取り込むような濃度条件で行う。この細胞の培養にクローニングされたDNA断片の集合をDNAライブラリーlibraryと呼ぶ。
調べたい生物の染色体DNAから直接DNA断片を得るため、制限酵素で開環して切断すれば、数百万個の異なるDNA断片が生じる。その一個一個をDNAリガーゼとATPを混合して、別々のプラスミドに挿入すれば、数百万個の異なる組換えDNA分子ができあがる。その組換えDNA分子をそれぞれの細菌に分配すれば、その集合がゲノムライブラリーgenomic libraryとなり、その生物の全ゲノムを網羅することになる。
制限酵素とDNAリガーゼを用いれば、ヒトゲノム全体を網羅するDNA断片すべてが得られる。つまりヒトDNAの各部分ごとに由来するDNA分子を持つ細菌の集団で構成されるヒトゲノムライブラリーが作れる。
プラスミドは、ある種の細菌に、もともと存在する環状二本鎖のDNA分子で、大きさは様々あり、ゲノムサイズが概して小さいもので10~30kb、細菌あたり10~40コピーあるものと、大きいもので60~100kb、細菌あたり1から3のコピーしかないものとがある。プラスミドは、抗生物質の不活性化・毒素の生産・天然産物の分解などに関わる遺伝子を持っている。この寄生染色体は、宿主の染色体とは独立して複製され、必ずしも生存に必要でないようで、プラスミドを全く持たない細菌もあれば、1個の細菌細胞に40コピーを持つものもある。
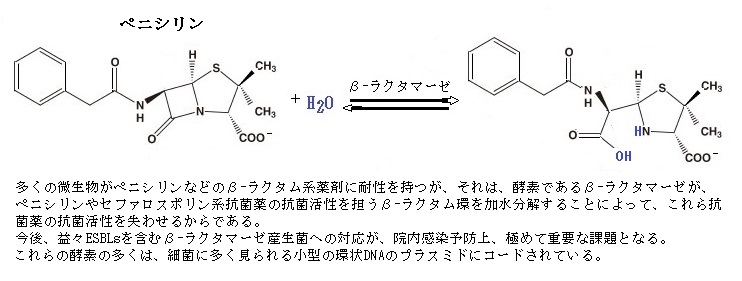
病原体の中には、特定の抗生物質を不活性化したり分解したりする酵素を持つものがある。多くの微生物がペニシリンなどのβ-ラクタム系薬剤に耐性を持つが、それはβ-ラクタマーゼと言う酵素を保有しているからである。この酵素はβ-ラクタム環を加水分解して薬を不活性化する。これらの酵素の多くは、細菌に多く見られる小型の環状DNAのプラスミドにコードされている。多くのプラスミドは、ある細菌細胞から別の細菌細胞へ簡単に受け渡されるため、その抗生物質耐性が蔓延する一因となっている。その一方、プラスミドは、組換えDNA技術にも多用され、植物へ外来遺伝子を挿入する種々の方法が 開発されている。
どこでもいるアグロバクテリウム Agrobacterium tumefaciensは、植物の根頭癌腫病に関連する土壌細菌で、カキ・ブドウ・モモ・リンゴ・ナシ・クリなどの果樹や、バラなど樹木など多種の植物細胞に外来遺伝子を挿入する方法で伝染し、世界中に蔓延している。
その植物の感染部位に、植物の腫瘍であるクラウンゴールcrown gallと呼ばれる塊が生じる。そのクラウンゴールは、オパインと呼ばれる数種のアミノ酸誘導体を合成し、アグロバクテリウムは、これを植物細胞への侵入経路にしてDNAを送り込み、植物の栄養分を窒素源または炭素源として増殖する。
腫瘍の形成とオパイン合成は、腫瘍誘導プラスミドtumor-inducing plasmid(TIプラスミド)の働きによる。TIプラスミドのごく一部(20kb)が、感染した植物細胞のゲノムの中に組み込まれる。この部分をtransferred DNA(T-DNA)と呼ぶ。
この腫瘍誘導体のTIプラスミドが、植物細胞に外来遺伝子を挿入するベクターとして使われる。
その一方で、TIプラスミドは、植物細胞に侵入し、遺伝子を細胞に挿入するので、この性質を利用して、そのプラスミドの中に、異種遺伝子を結合させ、植物細胞に挿入させることができる。この「組換えDNA技術」によりTIプラスミドは、植物細胞のゲノムの解析や、植物の農産物としての品質向上や収穫増などの品種改良に大いに貢献するものと期待されている。特に、ブドウなどの双子葉植物や数種の単子葉植物の形質転換には有効であるが、人類の食生活に欠かせないイネやトウモロコシとコムギ、その世界三大穀物と呼ばれているイネ科の単子葉植物には適さないようだ。
生物学的に「性」は、子孫を残す、言い換えれば自身の遺伝子を未来に託す際、雄が自身の DNA を雌に挿入するという手法が一般的で、細菌でもその例外ではない。大腸菌には雌雄の別があって有性生殖を行うことが、1,946年に、イェール大学で研究するジョシュア・レダーバーグJoshua Lederberg によって見いだされ、後にこの業績で、1,958年度のノーベル生理学・医学賞を受賞した。この大発見が、遺伝学を飛躍的に進歩させる画期となった。遺伝学研究における重要なモデル生物、エンドウ豆からスタートした遺伝学が、ショウジョウバエやアカパンカビを経て、より 世代時間が短い大腸菌Escherichia coli(E.coli; イーコリ)でも研究が可能になり、大幅に短縮された研究結果の検証により、研究速度が急激に向上した。
真核生物では、めったに起こらないが、異なる種の個体間で、遺伝子やゲノムの一部を交換することもある。この遺伝子の水平伝播horizontal gene transferは、接合によってDNAを交換できる細菌ではよく見られる。例えば供与菌が性線毛と言う微細な付属器官を伸ばして受容菌に張り付くと、接合が始まる。供与菌のDNAが性線毛を通って受容菌に移る、というのも、単細胞生物のゲノムは生殖系列germ lineであるため、どんな変化も次世代に伝わる。体を構成はするが、生次世代に引き継がれない体細胞であれば、遺伝子の水平伝播によって変化が生じても、次世代の細胞に影響はしないが、生殖細胞の細胞系譜であれば、次世代の生物を形成するのが、その役割である。
動物などの多細胞生物では、通常、生殖系細胞は体内に隔離され、外部の細菌やウイルス、そのDNAとの接触は極力避けられている。
しかしながら、その幼虫がアズキやササゲの豆の中で発育する、昆虫のアズキゾウムシのゲノムには、その昆虫に感染した共生細菌であるボルバキアより水平伝播したDNAが含まれている。既知のものを含めて160もの転移遺伝子があると言う。ボルバキアと呼ばれる共生細菌は、昆虫の細胞 の中で生息する特性を持っている。細菌から多細胞生物への遺伝子の水平伝播が、ヒトを含む高等生物においても、腸内や環境中に存在する細菌が、遠い種の隔たりを越えて遺伝子を送り込む可能性を示唆している。
また、アブラムシのゲノムには、他の昆虫のゲノムと異なり、天然色素のカロテノイドの合成に必要なタンパク質がDNAにコードされており、そのDNAは、菌類からの遺伝子の水平伝播によって獲得されたようだ。
大腸菌の雌雄を決めている小さな DNA 分子を「Fプラスミドplasmid」と呼ぶ。通常は、染色体から分離し、1個ないしそれ以上の遺伝子を持ち、その遺伝的情報は、各々の細胞から娘細胞へ、時には隣接細胞へと自律的に複製されるが、あるものは一時的に染色体に統合され、それとともに複製される。細菌の細胞質に存在し、「Fプラスミド」保有株が雄、非保有株が雌である。
「Fプラスミド」を保有する雄は、F繊毛を持ち、一方の雌はこの繊毛が全くない。雄のF繊毛は「Fプラスミド」が作り出すもので、雄のF繊毛は雌を抱え込み、雌の細胞内に DNA を挿入する。これを接合 conjugationと呼び、つまり遺伝子の交換が行われる。「Fプラスミド」は輪ゴムのようなリング状で、普通は細胞質中に存在しているが、時に染色体DNAに組み込まれてしまうことがある。そのようになった株を Hfr (High frequency of recombination;高い頻度の遺伝子の組み換え) 株と呼び、これによって極めて効率よく遺伝子の交換を行う。「プラスミド」は、細胞質にあって染色体とは独立に自己増殖し、次世代に遺伝される染色体外性遺伝子でもあり、特に「Fプラスミド」の遺伝子が重要で、例えば、細菌の宿主に特定の抗生物質に対する耐性を与えもする。
特に大型プラスミドのRプラスミドやFプラスミドの中には、接合に関わる遺伝情報を持つものがあり、これらと共存することにより、本来接合できない小型プラスミドも他の固体に遺伝情報を伝えることができ、接合だけが種の多様性に重要な役割を果たしているのではない。プラスミドと言う比較的小型の環状DNA分子には、細菌細胞内の染色体と独立して複製するための起点と、プラスミドを意のままに切って外来DNA断片を挿入するために使う制限酵素による切断部位が備わっている。
クローニング用のプラスミドは、自然界の様々な細菌が保有するプラスミドを使いやすくする技法として活用されているが、細菌のプラスミドは、ヒトの体内にある細菌が、抗生物質耐性を与える遺伝子を運ぶものとして、医師や科学者の研究過程で見いだされた。かつては極めて有効で多くの人命を救ってきたペニシリンなどの抗生物質が、抗生物質耐性を付与する遺伝子の水平伝播horizontal gene transferにより細菌間に広まったため、今では細胞感染症を惹き起こす多くの細菌は、DNAやRNAの変異により抗菌薬の作用点を変化させている。また、プラスミド上にあるDNAによる薬剤耐性獲得はもとより、細菌に感染するウイルス(バクテリオファージbacteriophage)を介してDNAを取り組む形質導入などにより、薬剤耐性を獲得することもある(水平伝搬)。なお、細菌に感染するウイルスを総称して、バクテリオファージと呼ぶ。
異なる種の個体間で遺伝子やゲノムの一部が交換される水平伝播は、真核生物では極めて稀であるが、接合により DNAを交換する細菌ではよく見られる。
例えば、大腸菌は、過去1億年以内に、そのゲノムの1/5を他の細菌種から獲得している。このような遺伝子交換は、新種の薬剤耐性菌の出現により、その抗生物質耐性を付与するプラスミドが、遺伝子の水平伝播によって細胞間に広がり、また種から種へ容易に伝達されるため、医療現場では、かつて細菌感染症では有効であったが、現在、その効力を失った抗生物質は少なくない。例えば淋病を惹き起こす淋菌の大部分は、ペニシリンに対する感受性の低下が著しい。
いずれにしても、細菌の有性生殖は、高等な真核生物とまったく同じで、雄が DNA を雌の体内に放出する。生物界には多くの性を持つ生物もいて、なん とある種の粘菌slime mould(単純に単細胞と言えないが真核生物で、変形菌、動菌ともよばれ、真核生物の中で原生生物界protistsに属している)では13種類もの性を持っている。
粘菌は、「変形多核体」または「偽変形体」のいずれかを形成する真核細胞を持つ微生物で、粘菌はよく菌類の分類体系に含まれるが、その類縁性は低い。動物の分類体系の原生生物か、もしくは植物における「粘菌門」が相当なのだろうか。
粘菌の殆どは、腐朽した樹木や切り株などに生育している腐生菌で、多量の粘液をもっている。細胞性粘菌などは、バクテリアや酵母などの微生物を捕食して分裂・増殖する単細胞アメーバとして、通常は土壌表層に広く分布している。単細胞のアメーバとして増殖するが、やがて走化性とアメーバ運動により集合するが、この場合、単細胞が集まっただけで融合することはなく、子実体fruit body(しじつたい)に変化するまでは単細胞のままである。周囲の餌を食べつくして飢餓状態になると、発生後、初めての分化段階に入り、多数の胞子(単核)が着生する塊とそれを持ち上げる柄からなる子実体と呼ばれる植物のような多細胞構造を作る。胞子は次世代へと遺伝情報を伝えることのできる「生殖細胞」であり、柄細胞は生殖細胞を支え、その世代で死滅する「体細胞」である。単細胞でありながら多細胞体制を築き上げることができ、細胞の役割分担をたった2種類に分化した細胞で行うので、発生と分化を研究するのに有用な生物である。
また、 ゾウリムシ・ラッパムシ・ツリガネムシなど原生生物界に属する多様な微生物の総称である繊毛虫Ciliataは、単細胞で卵形または楕円形で、繊毛がありこれで運動する。ミドリゾウリムシは、細胞内に数百の単細胞緑藻類クロレラを共生させている。クロレラと光合成産物のやりとりをする相利共生の関係にある。それぞれ単独で生活することも可能で、細胞内共生の段階的過程にあると言える。
通常、ゾウリムシは細胞分裂、無性生殖によるクローン(同じ遺伝子を持った細胞集団)で増殖する。しかし無性生殖としての細胞分裂には限界があり、ある回数以上は分裂が出来ない。分裂回数が限界に達すると、その前に、性的に成熟し、異なる個体同士の小核の遺伝子の半分を融合する有性生殖を行なう。
ゾウリムシ細胞には、大核と小核の2種類の核があり、大核は、生体を活性化させる代謝に必要なタンパク質をコードしている。それに対して小核は、代謝に伴う遺伝子損傷を避けるためて、通常は休止している。性的に成熟した個体が、同じく成熟したパートナーと出会ったときに、ペアとなって生殖を開始する。小核の減数分裂が始まり、1倍体に戻り、手順通りの細胞分裂て一対の配偶核と移動核が生じ、移動核がペア相手側に移動して相手の配偶核と融合して2倍体に戻る。その後小核が大核を作り出して若返える。以後限界まで分裂を繰り返してクローンを増やし続けまる。
細菌にも「性(雄雌の別)」が存在し、有性生殖が行われている。雑種強勢の原則に則って、異なる「性」同士で DNA の交換を行いながら進化して行く生物の方が主流なのである。「性」を捨ててクローンで生き残る道を選択して進化してきたのがウイルスである。
殆どの原核細胞は単細胞生物であるが、鎖や集合体などの構造を持つ多細胞体となるものもある。真核生物は直鎖状DNAを持つが、原核生物も直鎖状DNAを持つものもあるが、大部分は閉環状か開環状の違いはあるが環状DNAを持っている。真核生物には環状と言う例外はない。だが、何故そうなったかについては分かっていない。
目次へ
アーキアArchaeaは古細菌と訳されているが、進化的には真核細胞に似た特徴がある。20世紀の半ばまで、地球上の生物は細胞内に核をもつ真核生物と、核をもたない原核生物の2大系統に分けられると考えられていた。
1,977年、イリノイ大学の研究者カール・ウーズCarl Woeseは、見かけ上は同じ細菌なのに、系統的にはそれまで知られていた細菌とはまったく異なる分類群の存在を明らかにし、細菌と古細菌という2つの群に分かれるとした。
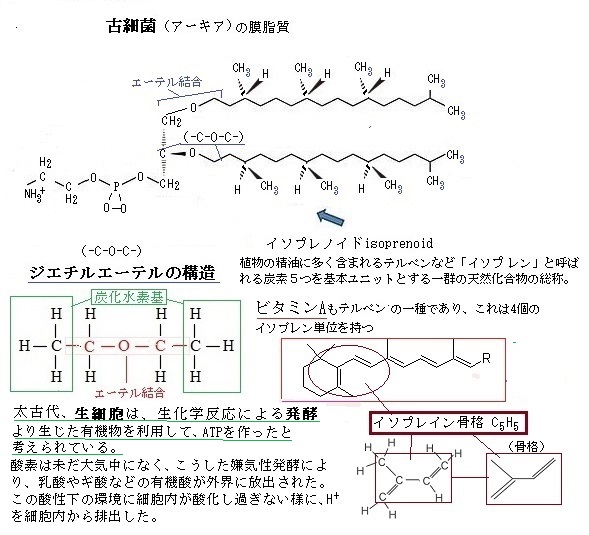 すべての生物は、細胞中のリボソーム内で、DNAの塩基配列によるコードに従ってタンパク質を合成する。ウーズは、リボソーム内のrRNAの塩基配列の類似度から、地球上のすべての生き物が、真核生物とそれまでに知られていた細菌類に加えて第3のグループあるとして、3大系統に分けられることを示した。同じ原核生物の2つのグループの塩基配列の違いは、原核生物と真核生物の違いに匹敵するほど大きかった。この第3のグループは「古細菌Archaea」と呼ばれ、それまでの細菌類は「真正細菌Eubacteria」と呼ばれるようになった。この細胞に似た古細菌は、進化の早い時期と言うより系統樹の根元のあたる約35億年前、共通の先祖にあたる原始生物から細菌と古細菌の2系統に分かれたと現在では考えられている。
すべての生物は、細胞中のリボソーム内で、DNAの塩基配列によるコードに従ってタンパク質を合成する。ウーズは、リボソーム内のrRNAの塩基配列の類似度から、地球上のすべての生き物が、真核生物とそれまでに知られていた細菌類に加えて第3のグループあるとして、3大系統に分けられることを示した。同じ原核生物の2つのグループの塩基配列の違いは、原核生物と真核生物の違いに匹敵するほど大きかった。この第3のグループは「古細菌Archaea」と呼ばれ、それまでの細菌類は「真正細菌Eubacteria」と呼ばれるようになった。この細胞に似た古細菌は、進化の早い時期と言うより系統樹の根元のあたる約35億年前、共通の先祖にあたる原始生物から細菌と古細菌の2系統に分かれたと現在では考えられている。ドメインは、古細菌と言う新しい分類群に対応するため、分類学上の界kingdomの上位の階級として設けられた。球形、棒状あるいは不定形の単細胞生物で、細胞の形や大きさでは細菌との区別はつかないが、その生態機構や遺伝子が全く異なる。
高度好塩菌・メタン菌・好熱菌(80~90℃以上の温度を好んで生育する超好熱菌もいる。それ以下の温度で生育する好熱菌とは区別される)などで良く知られている古細菌は、全生物の共通の祖先から細菌と別れた後に、真核生物と別れた。従って、核を持たない原核生物であるにも関わらず、生化学的性質を調べると、細菌と古細菌の2つのドメインの違いは、原核生物と真核生物の違いほど大きい。
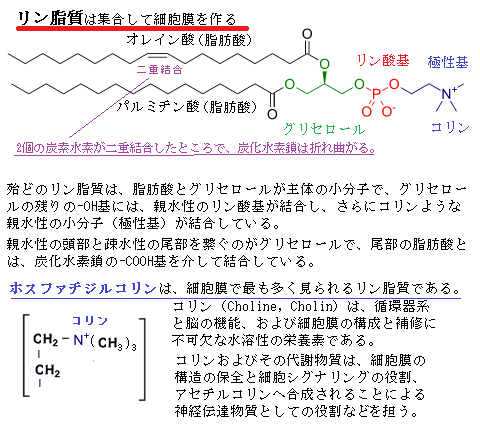 原核生物である細菌は、土壌に棲むものや病原性のものなど身近な場所に存在しているが、古細菌は他の生物が棲めない環境にも適応している。高濃度の塩水・熱い酸性の温泉・空気の無い深海底の泥・汚水処理場のヘドロ・南極の氷の下の池の中にもいる。また、酸性で酸素の無いウシの胃の中にいて、セルロースを分解してメタンガスを作るものもいる。
原核生物である細菌は、土壌に棲むものや病原性のものなど身近な場所に存在しているが、古細菌は他の生物が棲めない環境にも適応している。高濃度の塩水・熱い酸性の温泉・空気の無い深海底の泥・汚水処理場のヘドロ・南極の氷の下の池の中にもいる。また、酸性で酸素の無いウシの胃の中にいて、セルロースを分解してメタンガスを作るものもいる。メタン菌methanogenとは、嫌気条件でメタンを合成する古細菌の総称である。メタン生成菌とも呼ばれる。動物の消化器官や沼地・海底堆積物・地殻内に広く存在し、地球上で放出されるメタンの大半を合成している。起源は古く、35億年前の地層の石英の中から、生物由来と思われるメタンが発見されている。生物にとって極限環境は、原始の地球の過酷ではあるが、それが通常の条件であり、大気に酸素が増える以前の、最初の生命体が現れた環境でもある。古細菌の研究から全生物の共通の祖先や真核生物の起源が明らかとなる。
古細菌は火山口の黄色い硫黄沈殿物に囲まれたような厳しい生育地にも繁殖している。古細菌の細胞膜を構成する膜脂質も、親水性部分と疎水性部分を含んだ両親媒性分子である。多くの古細菌は過酷な生活環境にあるため、古細菌の膜の組成は、真核細胞や細菌と比べて3つの重要な特異性がある。
その全体的な形はほぼ真っすぐで、2個の疎水性脂肪酸が互いのほぼ平行に並び、水に対してリン酸などが持つ強い極性により親水性のコリンリン酸は、疎水性脂肪酸とは反対を向いている。
 |
| |
 |
コレステロールや糖脂質もまた細胞膜中に含まれ、コレステロールは特に細胞膜に強度を与え、糖脂質は細胞表面で膜の認識機構などに関与する。
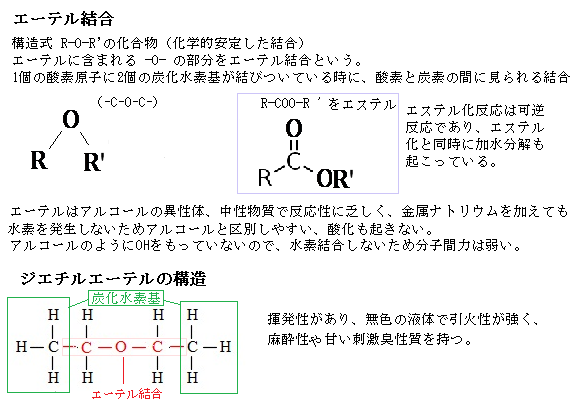
リン脂質のグリセロールには、ホスファチジルコリン(レシチン)がもっとも多く含まれている。レシチンは分子内に疎水性部分と親水性の部分を持つので、強い界面活性を有し、その乳化作用によって脂肪の消化吸収に役立っている。
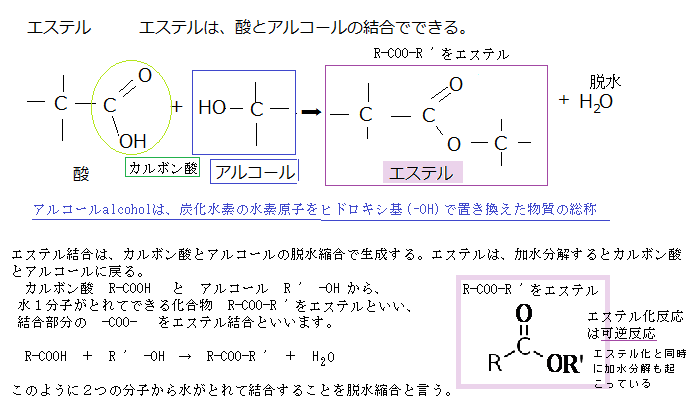
古細菌の細胞膜の組成も過酷な生活状況に適応している。無極性の炭化水素鎖とグリセロール骨格と結合は、エステル結合ではなく、エーテル結合による。
エーテル結合は加水分解に対して抵抗性が高い。エステル化反応の方は、可逆反応でエステル化と同時に加水分解が始まっている。
またイソプレンとよばれる5つの炭素原子を基本骨格とする炭化水素鎖は、直鎖ではなく分岐しており、真核細胞や細菌の膜脂質にある分岐してない炭化水素鎖よりも酸化に対して抵抗性が強い。この加水分解や酸化に対する強度は、例えば高温や酸性や高塩濃度の環境下でも生育できるからである。塩分濃度salinityは、水に溶けている塩の量で、ここで言う「塩分」とは、塩化ナトリウムNaCl だけでなく、硫酸マグネシウムMgSO4や硫酸カルシウムCaSO4、そして炭酸水素塩(HCO3- を含む塩)などの塩類も含む。
目次へ
地球上のあらゆる生物には、共通の先祖があり、現在の生物は共通の先祖から進化したと言う知見は、地質学や生化学によって、その進化の過程が多方面から 裏付けられている。
重要な代謝経路も、殆どの生物で共有されている。例えば、グルコースと酸素を二酸化炭素と水に変換する一連の化学反応は、大腸菌のような細菌と人間でも本質的に変わらない。
グルコースは酸素と反応し、次のような酸化還元反応をする。
C6H12O6 + 6O2 → 6CO2 + 6H2O
この反応は、二酸化炭素と水が発生する発熱反応である。 有機物を無機物に分解し、その過程で出るエネルギーを利用してATPを合成する。グルコースを分解し、ATP分子の形でエネルギーを取り出すことは、生物の持つ代謝経路の最も重要なものの1つである。大多数の細菌の細胞膜には、ミトコンドリアと非常によく似たATP合成酵素がある。エネルギーの獲得に電子伝達系を使う細菌では、電子伝達によってH+を細胞からくみ出し、そこにできるプロトン駆動力でATP合成酵素を働かせてATPを生産している。嫌気呼吸は、酸素の非存在下でグルコースを分解する経路である。それに対して好気呼吸は酸素の存在下でグルコースを分解する経路である。
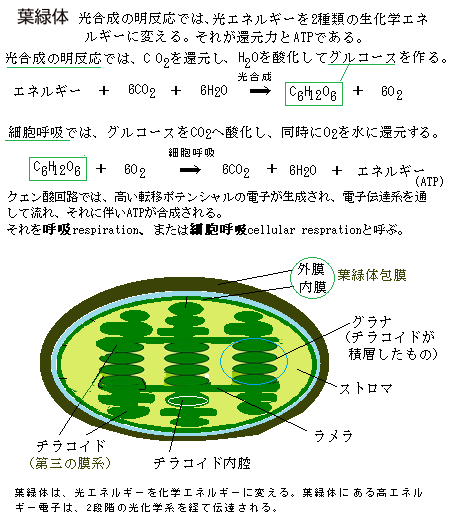 特に、植物が光エネルギーを捉えて起こる生化学反応の過程は、動物がグルコースを分解してエネルギー発生させる過程と極めて似ている。
特に、植物が光エネルギーを捉えて起こる生化学反応の過程は、動物がグルコースを分解してエネルギー発生させる過程と極めて似ている。現在、地球上の多様な生物は、生化学的特徴に基づいて、ドメインdomainと呼ばれる界よりも上の、最も上位のランクである3つのグループに分けられている。一つが真核生物Eucarya、二つが細菌Bacteria、 三つ目が古細菌Archaeaである。進化の過程で互いに分岐して何十億年も経ち、全く異なる3種類の生物群になっても、遺伝子調節の鍵となる分子・TATAボックス結合タンパク質が共有され、しかもその形がよく似ている。
様々な生物は進化の過程で、様々に激変する環境条件を克服してきたが、そのために、まったく新しい生体高分子を作るのではなく、既存の生体高分子を新しい課題に適応させて解決してきている。
原核生物の古細菌ドメインに含まれるシアノバクテリアcyanobacteria(藍色細菌)は、原核生物 の中で独立した大きなドメインを占め、形態・生理・生態において多様性を示し、環境適応能力に優れ地球上に非常に広く分布している。淡水で発生するアオコの中には、大量に発生した藍色細菌による事例も少なくない。地球上に最初に発生した酸素発生型光合成生物として、藻類や陸上植物の細胞内の葉緑体や原核緑藻と共通する祖先を持つ「古細菌」として認められている。他の細菌とは違い、シアノバクテリアは、葉緑体は持たないが、クロロフィルやフィコシアニンphycocyanin(青色の補助酵素、各種藻類で見られる色素タンパク質)などの色素タンパク質を含み、それにより光合成を行うことで藍藻デンプンを生成・貯蔵することができる、広く多様な古細菌の一群である。このことから、分類上光合成植物の一門として扱い、藍色植物と呼ぶこともある。
光合成生物は光を化学エネルギーに変換して生命を維持する。そのために光を効率よく取り込むクロロフィルやフィコシアニンなどの色素タンパク質が必要である。シアノバクテリアは、酸素発生型光合成を行う原核生物であるが、その酸素発生型光合成は、植物の光合成と基本的に同じものである。この光合成では、光エネルギーを化学エネルギーに変え、水を電子供与体として、水分子から電子を奪い、H+とO2を発生させる。シアノバクテリアの祖先は30億年前には、地球上に出現し、初めて酸素発生型光合成を始めた。水と光があればエネルギーが得られることから、当時の地球上で大繁殖した。その結果、それまでの酸素を含まない嫌気的な大気に酸素を供給することとなり、徐々に現在に近い酸素を豊富に含む好気的大気に変えていった。好気的生物
他の光合成生物との光吸収の競合や、海や陸でも深海や高山といった生息条件によって光質は変化する。それぞれの環境条件における光質の変化に適応できる、効率的な光合成を行うための戦略に応じた形態や生態に、生物は変化していった。
光合成生物の中でも、植物の葉緑体の祖先と考えられて いるシアノバクテリアは水を分解して酸素を発生させる原核光合成生物であり、水棲と陸棲が存在し、藍色(青 色)をしていることから藍藻や藍色細菌と呼ばれる。藍藻という名称が付けられたのは、かつては、藻類の一群とされたためだが、原核生物に属するが系統的には、「細菌」とは系統を別にするため、「古細菌」と呼ばれドメインに属する。シアノバクテリアと呼ばれる。
他にも「古細菌」には、好熱性古細菌(温泉や海底熱水地帯に棲む)や高度好塩菌(塩田や高濃度の塩湖に棲む)、メタン菌(腐った沼地やどぶ川、動物の腸に棲む)などが含まれている。地球の誕生は、およそ46億年前、その地球の35億年前の地層にある石英の中に、生物由来と思われるメタンがあった。地球が誕生して好熱性古細菌やメタン菌などは、いずれ も系統樹が立ち上がる原始生物近くで発生している。今でも存在する生物でありながら、その生命が誕生 した原始の地球環境は、高温で嫌気的という現在の超好熱菌などが好む生育環境と似ている。その超好熱菌の遺伝子数は、一般的に2千程度とヒト・酵母・大腸菌(それぞれ2万,6千,4千程度)と比べて少ないようだ。単純な生命機構を有していると考えられる。古細菌へ分類は、遺伝子の塩基配列の生化学的特徴に基づいている。古細菌は全生物の共通の祖先、原始生物から細菌と別れた後、次の共通する祖先生物から真核生物と別れた。
シアノバクテリアが持つ 色素タンパク質の名称には、「藻の」「海藻の」を意味するフィコphycoが接頭辞としてある。 フィコシアニンは青色の色素タンパク質であり、シアノ バクテリアが青色を呈するのはこの色素タンパク質を持 つためである。フィコシアニンに結合している色素は、 フィコシアノビリンでクロロフィルが吸収できない橙~ 赤色光を吸収する。また,、フィコシアニンに加えてフィ コエリスリンという赤紫色の色素タンパク質を持つシア ノバクテリアも存在する。フィ コエリスリンに結合して いる色素は、フィコエリスロビリンで緑色光を吸収する。色素の色は、白色光を当てたときに特定の光の色を吸収 した、その残った光の波長がヒトの目に届いた時に、色として感じられる(反射)。色として感じる範囲には幅があり、また、色を構成する光の性質には種類がある。ヒトの目に届く光は「放射」、「吸収・反射」、「透過」の3種類に分けることができる。
藻類を生命の進化を示す系統樹で見ると、藻類の仲間は、一か所にまとまることなく系統樹上に点在している。原核生物の細菌ドメインにも、真核生物のドメインにも存在する。真核生物を見てみると、5つの界に藻類が分かれ、緑藻と灰色藻は全て光合成をする生物であり、他の4つの界は、どれも光合成をする生物(藻類)と、光合成をしない生物が混ざっている。つまり光合成をする能力は、生物の分岐と関係がある部分と、関係がない部分がある。その理由は、生物光合成器官である葉緑体の獲得に深く関わっている。
化石のシアノバクテリアは、約35億年前の岩石で見つかっている。通常、池や水溜りなどで見られる微生物である。太古の地球では、海洋の浅瀬に菌糸状のシアノバクテリアが珊瑚礁のようなコロニーを作り、大繁殖していたようだ。ストロマトライトstromatoliteと呼ばれる、菌糸体の原核微生物が群集して作る堆積構造が岩石化石として残る。
オーストラリアの西北海岸、西オーストラリア州の最西端に位置する世界遺産シャークベイにあるストロマトライトは、35億年前から生息する世界最古の生物体と言われている。澄み渡る入り江の水際一帯に広がる無数の岩のような塊が、酸素形成の起源とされるストロマトライトで、今でも年に約0.3㎜ずつゆっくりと成長を続けている。シアノバクテリア類が、細胞から分泌粘液を出し、夜間には海中の石灰質やケイ質の粒をとらえ固着し、皮膜や薄層を作る。昼には、この皮膜や薄層の表面で更に藍藻類が成長し、夜間、再び皮膜や薄層を作る。
シアノバクテリアは、葉緑体を持たないが、クロロフィルは細胞内の特殊な膜、チラコイドで保持されている。しかも、空中の窒素を固定できる種もある。
高温の炉の中で溶かして得られた粗銅を電気分解したり、鉱石を選別せずに硫酸などを散布し、 鉱石から溶け出た銅分を濃縮後、電気分解によって銅地金として回収する毒性化学物質に依存する従来の金属抽出技術は、何世紀にもわたって環境や健康に多大の 被害をもたらしてきた。微生物を利用して鉱物から金属を溶出させる技術は、バイオマイニングBiominingまたはバイオリーチングBioleachingと呼ばれている方法で、低品位鉱山から金属精錬する際に実用化された技術で、溶剤で溶けにくい鉱石から金属を製錬する際に、細菌などの微生物の活性を利用して鉱石を溶解させる技術である。 溶剤に硫黄酸化細菌と鉄酸化細菌を加え、その細菌の活性により、硫化銅鉱石中に含まれる硫化鉄が酸化され、銅が硫酸銅の形で溶解して浸出leachingする。既に、全世界の銅の約15%がこの方法により生産されている。鉱石から金や銅、ウランなどの金属を取り出すのに細菌が使われているが、この バイオマイニングの採鉱技術により、菌を使って酸素や栄養分と鉱物を抽出している。この微生物群によるマイニング(採鉱)は、経済的に採算性がとれない低品位鉱石 や難処理鉱石の開発を可能し、その一方では環境負荷を低減するバイオマイニング技術の発展が今後益々重要になっ ている。
太古の微生物は海底火山の熱水孔の周辺の極限環境下で、熱水とともに排出される鉄や硫黄を酸化して得られる エネルギーを利用して生育していたと言われている。バイオマイニングの現場で働く微生物も、硫黄や鉄をエネル ギー源として、pH1~2の極端な酸性環境で働いており、太古の微生物 と同じ生態を保持している。
バイオマイニングを可能にするシアノバクテリアであるアナベナ・シリンドリカAnabaena cylindricは、藍藻の成長が最も速く、殆どの元素を抽出するため、水田を肥沃にする天然の肥料として使われている。
アナベナ・シリンドリカは、多くの細胞が長く繋がる糸状構造をしている。窒素固定、つまり大気中のN2を捉えてアンモニアNH3などの有機化合物にする細胞や、光合成によりCO2を固定する細胞、丈夫な胞子になる細胞がある。近縁のフォルミディウムPhormidium laminosumの細胞内の膜で光合成が行われる。原核生物にも簡単な多細胞体が存在している。 シアノバクテリアは、淡水や海水の中の他、土壌や岩石、更には植物にも着生し、あるいは共生するなどして広く分布する能力を持つ。分類学的には細胞形態や分裂様式から、「単細胞2分裂」・ 「単細胞多分裂」・「糸状性細胞」・「ヘテロシスト(異質細胞)を持つ糸状性細胞」・「異質細胞を持ち分岐を伴う糸状性細胞」の5つの「section」に分けられている。幾つかのグループは多系統に分かれているため、今後再編が予想されている。
1,970年代までは、藻類のなかの一分類群として取り扱われていたため、藍藻blue-green algaeと呼ばれていた。Algae(ˈældʒiː)とは、植物学で言う「藻類」を言う。5つ目の「section」に属するシアノバクテリア、即ち「異質細胞を持ち分岐を伴う糸状性細胞」に含まれる、最も複雑な能力を持つ菌糸状のシアノバクテリアで、2つ以上の面から細胞分裂ができるため、多方向へ菌糸を広げられる。
太古の地球では、海洋の浅瀬でこのシアノバクテリアが現在の珊瑚礁のようなコロニーを作り、大繁殖していた様子が想像できる。現代に残るストロマトライトと呼ばれる細菌が、シアノバクテリアの光合成によって少しずつ酸素を大気に排出することにより、現在の大気を作り上げたと考えられている。
約30億年前の岩石で見つかっているシアノバクテリアが、その上部では現在にも生き続ける。この時代は、大量の酸素が大気中に満たされる22億年前より8億年も時代を遡るgo back in time のである。それは、シアノバクテリアが酸素の少ない暗黒の環境下で生息していたことを示す。
かつて真菌は植物の一種と分類されたが、1,969年以降は動植物と区別されるようになった。現在の生物分類においては、真菌(類)という呼称は使われなくなった。一方、現在も医学・獣医学の分野では、病原体としての菌類を細菌と区別して真菌と呼ぶ。
葉緑体は、細胞内共生したシアノバクテリアの祖先細胞が進化して、現在の葉緑体になったと考えられている。葉緑体は、独自のDNAとその複製と発現を行う系を持っているが、それだけでは、葉緑体が自律的に形成されることはない。核DNAにコードされたタンパク質も多数含まれているからである。
ミトコンドリアの進化と同じで、葉緑体は光合成微生物が細胞内共生した結果生じた。シアノバクテリアの祖先が、真核生物である宿主に取り込まれた生化学的な証拠が残っている。高等植物と緑藻類の葉緑体は、1回の細胞内共生で、紅藻類と褐藻類の葉緑体では、少なくとも2回以上の細胞内共生があった。葉緑体ゲノムは、シアノバクテリアのゲノムより小さいが、双方のゲノムには重要な共通点がある。どちらも環状DNAで複製拠点が1個であり、しかも、機能的に関連する複数の遺伝子が、共通した制御を受けるように並ぶオペロンoperonを形成している。このように同調して発現する遺伝子群の単位をオペロンと呼ぶが、ある環境変化に適応する一群の酵素は、同時に寄与するように発現のレベルが調節されている。しかも、進化の過程で、祖先シアノバクテリアの遺伝子が、宿主細胞の核へ移ったり、あいは完全に失われているかしている。現在の葉緑体は、宿主細胞に完全に依存する器官となっている。
目次へ
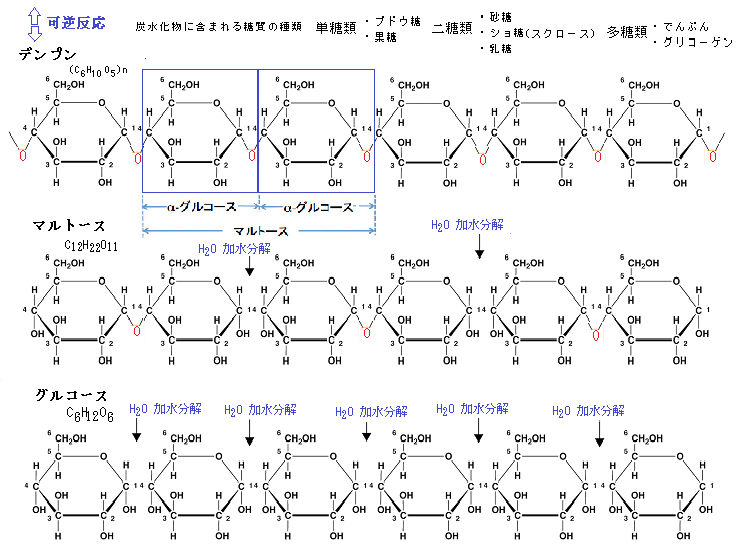
葉緑体
実は、光の方が熱よりもかなり高いエネルギーを持っている。光を当てると温度が上がる。太陽電池に光をあてると電流が発生する。この電流はモーターなどを介して、物を作ったり、加工したりする。つまり、光もエネルギーを持っている。
太陽の光エネルギーは、地球の全生命を維持し、地球上の環境を支配している。また、石油・石炭などの化石燃料や木炭などの燃料も過去の太陽の光エネルギーを化学物質として変換し蓄積したものである。この意味から地球上の大部分のエネルギーは、太陽の光エネルギーを由来にしていると言える。
葉緑体は、光エネルギーを、ATPと還元力の2つの化学エネルギーに変換する。葉緑体の中の光に由来する高エネルギー電子は、「光化学系Ⅱ」から「光化学系Ⅰ」を経て伝達される。光エネルギーを生物が利用できる化学エネルギーに変換するのは、葉緑体に含まれるクロロフィルの働きによる。この間に還元力が発生し、大気のCO2を還元し、H2Oを酸化し、グルコースと酸素を生み出す。
光エネルギーの源は、太陽の電磁放射であるが、地球上に僅か1%、しかも利用されるは、ごく僅か過ぎない。それでも地球上のすべての生命を十分に支えられる。
化学エネルギーに変えられる生物では、緑色植物が最も目立つが、実はその60%は藻類や細菌が光由来の化学エネルギーを使っている。
電磁波のエネルギーをATPと生合成のための還元力であるNADPHへと2つの化学エネルギーに変換する過程を、光合成photosynthesisと呼び、大気のCO2を還元し、土中のH2Oを酸化し、糖質と酸素を作る。
(光) + CO2 + H2O ➡ (CH2O)+ O2
(CH2O)で表される糖質は、主にスクロース(ショ糖)とデンプンであるが、光合成による糖質の合成は、地球上最も活用されている代謝経路と言える。それらの糖質が、生命活動のエネルギー源となり、生命体で働く様々な有機化合物を作る炭素分子の供給源となる。
太陽の電磁波エネルギーを使い大気のCO2を還元し、H2Oを酸化して、グルコースなどの化学燃料を合成して蓄積し、更に、その生命活動に使用するエネルギーを、グルコースなどから細胞質基質内で行われる解糖系やミトコンドリア・マトリックにおける好気代謝(クエン酸回路)によって回収している。
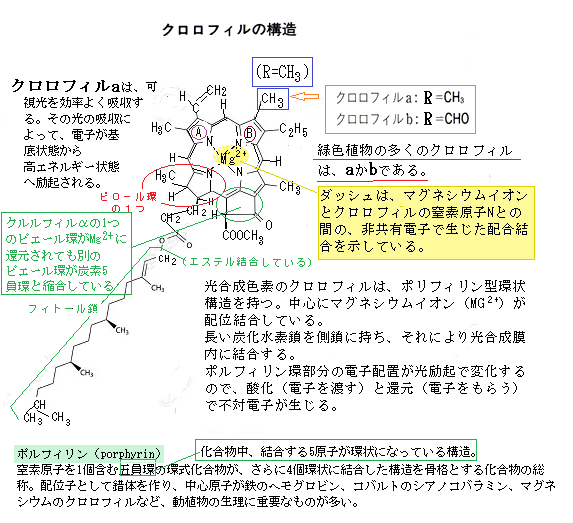 光合成で重要なことは、当然、光エネルギーの効率的な捕捉と吸収である。最初は、光受容体分子による光の吸収で始まる。殆どの緑色植物の葉緑体に含まれる主要な光受容体は、テトラピロールの置換体であるクロロフィルα(chlorophyllα)と呼ばれる色素分子である。ピロール環の4個の窒素原子がマグネシウムイオンMg2+を配位している。
光合成で重要なことは、当然、光エネルギーの効率的な捕捉と吸収である。最初は、光受容体分子による光の吸収で始まる。殆どの緑色植物の葉緑体に含まれる主要な光受容体は、テトラピロールの置換体であるクロロフィルα(chlorophyllα)と呼ばれる色素分子である。ピロール環の4個の窒素原子がマグネシウムイオンMg2+を配位している。キレートchelateとは、分子の立体構造によって生じた隙間に金属元素を挟む姿から「カニのはさみ」を意味する。中心に金属イオンを挟むような形で、キレート分子の2つ以上の配位原子が結合するクロロフィルαの配位結合では、ピロール環を形成する4個の窒素原子が、マグネシウムイオンMg2+を配位している。その結合電子が供与されて結合される、その化合物となる配位結合は、多くの錯体にその例がみられる。
クロロフィルのもう1つの特徴が、フィトールphytol鎖をもつことで、20個の炭素を持つ非常に疎水性が高く、側鎖のカルボン酸とエステル結合している。
量子化学の研究成果は著しく、電子に限らず、あらゆる物体は波として振舞う可能性が秘めていると見ている。すべての実験段階では、これと矛盾する結果は表れていない。 分子は複数の原子から構成されるが、その分子がどのようにでき、どの様に変化するかは、そのすべにおいて鍵とるなるのが、原子中にいる「電子」の存在である。
クロロホルムは単結合と二重結合を交互に含む共役二重結合のネットワーク構造を持つため非常に効率のよい光受容体となる。このような化合物を共役ポリエンと呼び、電子が特定の原子核に局在しないので、光エネルギーを吸収すると、この電子が低エネルギーの分子軌道から高エネルギーの分子軌道へ移る。
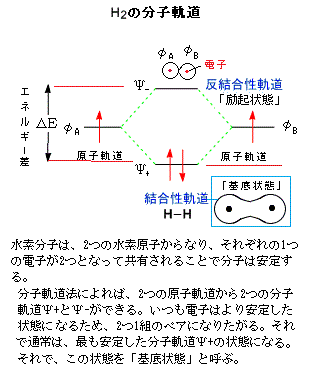 水素分子は、2つの水素原子からなり、それぞれの1つの電子が2つとなって共有されることで分子は安定する。分子軌道法によれば、2つの原子軌道から2つの分子軌道Ψ+とΨ-ができる。いつも電子はより安定した状態になるため、2つ1組のペアになりたがる。それで通常は、最も安定した分子軌道Ψ+の状態になる。それで、この状態を「基底状態」と呼ぶ。
水素分子は、2つの水素原子からなり、それぞれの1つの電子が2つとなって共有されることで分子は安定する。分子軌道法によれば、2つの原子軌道から2つの分子軌道Ψ+とΨ-ができる。いつも電子はより安定した状態になるため、2つ1組のペアになりたがる。それで通常は、最も安定した分子軌道Ψ+の状態になる。それで、この状態を「基底状態」と呼ぶ。しかしながら、すべての分子が基底状態で安定すると、化学反応が全く起こりえなくなる。そうなると化学反応で支えられている生物の生命は維持できなくなる。そのためには、分子にエネルギーを補給する必要がある。その方法は、2つある。1つが熱する事であるが、それよりも光(電磁波)を当てる方が有効である。
例えば、水素分子中の電子が取り得る状態は、Ψ+かΨ-である。Ψ+は安定した「基底状態」であり、Ψ-はエネルギーが高い状態であるため、通常では電子は入り込めない。ところがΨ+とΨ-間のエネルギー差(ΔE)に相当するエネルギーを持つ光を照射すると、Ψ+にあった電子が活動しΨ-に移る事が可能となる。Ψ+にΔEより少ないエネルギーを与えても、絶対にΨ-に移れない。
十分なエネルギーを与えると、「基底状態」の結合性分子軌道から「励起状態」の反結合性軌道に電子は移る。これを「励起」と呼ぶ。
つまり、波長に幅のある光が、特定の色素分子に働いて、その中の電子を励起することは、電子に必要なエネルギーΔEに相当する波長を持った光が、その分子によって吸収されたことを意味する。色素分子は、一般に複雑な分子構造をしているので、複数の分子軌道を持つ。そのため、特定の分子軌道にある電子が、特定の波長の可視光線によって励起され、その色素分子に固有の色を示すことになる。
単結合と二重結合を交互に含む共役系conjugated systemでは、単結合の場所で電子が染み出してから、共役系全体にある程度電子が自由に動けるようになる。
光は波と粒子の二重の性質を合わせ持つ。厳密な計算結果によれば、共役系が長くなるにつれ、吸収する光の波長が長くなることが分かっている。
分子は多くの電子を持っているが、その電子が入っているのが分子軌道である。電子を持っている分子軌道の中で最もエネルギーが高い軌道が最高被占分子軌道highest occupied molecular orbital(HOMO; ホモ)、電子が入っていない軌道で最もエネルギーの低い軌道を最低非占分子軌道lowest unoccupied molecular orbital(LUMO; ルモ)と言う。
たくさんある分子軌道の中で、特にHOMOとLUMOが反応や性質において重要となる。HOMOの電子が最も反応性が高く、エネルギーが高いので、これが反応に使われる。その電子をLUMOが受け入れる。反応の時、HOMOは電子を出す分子軌道であり、LUMOは電子を受け入れる分子軌道である。
電子が自由に動ける空間が広がるほど、HOMOとLUMOのエネルギー差は小さくなる。そのため励起に要するエネルギーが少なくてすむ。それで波長の長い光が吸収できるようになる。つまり、この波長が可視光線の領域に入れば、光エネルギーを吸収して、そのエネルギーを光合成反応中心へ伝える役割を担う補助色素accessory pigmentとなる。
光のエネルギーと光の波長の間には、密接な関係がある。波長が長いほどエネルギーは小さく、短いほどエネルギーは大きくなる。そのため、可視光線より波長の短い紫外線は、可視光線より高いエネルギーを持っている。逆に波長の長い赤外線は、低いエネルギーを持っている。
<波長が長い>赤→橙→黄→緑→青→藍→紫<波長が短い>
光の進路に障害物があると、波長の長い光(赤波)は通り抜けるが、波長の短い光(紫波)や中くらいの波長の光(青波)は、いろいろな方向に反射する。これを光の散乱と言う。
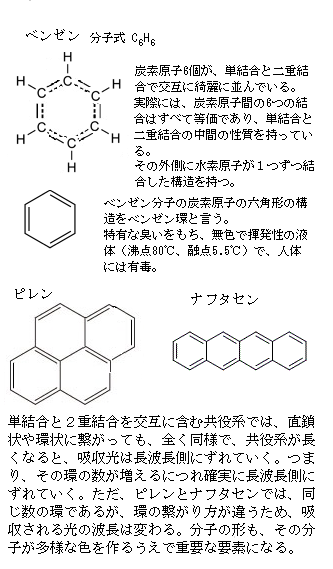 太陽光は波長の長い光や、波長の短い光を含んでいる。波長の比較的長い赤や橙色の光は大気の中を真っ直ぐ進む。波長の比較的短い青や紫の光は、大気中の窒素や酸素分子により散乱する。また、真空中での光速は、その値が決まっているが、物質に侵入した光は波長によって光速の値が変わる。可視光線が物質に侵入すると、一般に、波長が短い、振動数が大きい光の方は、光速が遅くなる。光速が遅いということは絶対屈折率が大きいということであり、波長によって絶対屈折率が異なってくる。
太陽光は波長の長い光や、波長の短い光を含んでいる。波長の比較的長い赤や橙色の光は大気の中を真っ直ぐ進む。波長の比較的短い青や紫の光は、大気中の窒素や酸素分子により散乱する。また、真空中での光速は、その値が決まっているが、物質に侵入した光は波長によって光速の値が変わる。可視光線が物質に侵入すると、一般に、波長が短い、振動数が大きい光の方は、光速が遅くなる。光速が遅いということは絶対屈折率が大きいということであり、波長によって絶対屈折率が異なってくる。分子構造が与えられれば、分子軌道法は、その分子の色を予測することができる。単結合と2重結合を交互に含む共役系では、直鎖状や環状に繋がっても、全く同様で、共役系が長くなると、吸収光は長波長側にずれていく。その環の数が増えるにつれ確実に長波長側にずれていく。
ただ、ピレンとナフタセンでは、同じ数の環であるが、環の繋がり方が違うため、吸収される光の波長は変わる。分子の形も、その分子が多様な色を作るうえで重要な要素になる。
光が波と粒子の二重の性質を併せ持つことの認識が、量子力学の基礎になった。その相矛盾する認識が前提となり、分子軌道法が成り立つ。
植物などの葉緑体には、クロロフィルやカロテノイドが主であるが、複数のタンパク質結合型色素が含まれている。光合成色素として光合成に必要な光エネルギーを捕捉する役割を担っている。緑色のクロロフィルは、最も多量に存在する色素であり、光合成に必要な光を捕獲するうえで最も有効である。クロロフィルには置換基の異なるいくつかの型があり、クロロフィル(Chl a,Chl b)とバクテリオクロロフィル(Bchl a,Bchl b) などがある。光合成色素の働きとしては、電子伝達反応に直接かかわる反応中心として働くものと、光を集めるアンテナ色素として働いているものがあり、クロロフィルの中でも働きには違いがあり、例えばChl aは反応中心として働き、Chl bはアンテナ色素として機能している。
人の目で感じられる可視光線visible lightの波長域380nm~780nm(ナノメーター)、それより波長が短い放射は紫外放射ultraviolet radiation、 波長が長い放射を 赤外放射infrared radiationと呼ぶ。
実際にはChl aでも反応中心として機能しているものは一部で、大多数はアンテナとして働いている。クロロフィルaとbはともに紫~青(400~500nm)と橙~赤(650~700nm)の波長の光を吸収する。 光合成色素の補助色素としてよく知られているのはカロテノイドcarotenoidは、β-カロテンcaroteneであり、こちらはクロロフィルと違い、赤橙色色素の一つである。
クロロフィルやカロテノイドは多くの光合成生物の細胞に含まれている。これらの異なる吸収波長を示すいくつかの色素をもつことで光合成生物が吸収できる光エネルギーの領域を広げている。光合成色素の光エネルギー吸収作用について 色素成分が光子を吸収すると、基底状態にある電子はより高いエネルギーの分子軌道に励起される。吸収された光子のエネルギーは基底状態とより高い軌道のエネルギーの差に等しいので、色素は光の特定の波長のみ吸収する。エネルギーを得た色素は基底状態と比べてより高い還元力を持つ。このように、色素はより正の還元電位を持つ成分から、より負の還元電位を持つ成分へと電子を伝達するのに利用される。
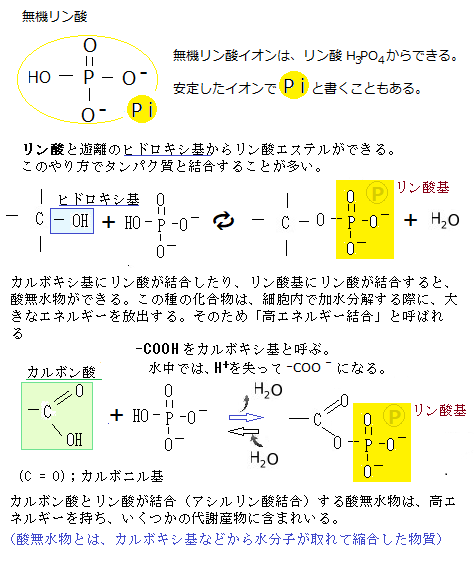 クロロフィルαは可視光を効率よく吸収するための強い吸収体を持っているため、地球に到達する太陽光スペクトルspectrumは、この領域で最大になる。クロロフィルαは、有機化合物が含む吸光能力の中では最大のものの1つである。
クロロフィルαは可視光を効率よく吸収するための強い吸収体を持っているため、地球に到達する太陽光スペクトルspectrumは、この領域で最大になる。クロロフィルαは、有機化合物が含む吸光能力の中では最大のものの1つである。クロロフィルのような色素分子に光が吸収されると、光のエネルギーにより、電子のエネルギー準位が基底状態から励起状態になる。原子は、その原子に特有ないくつかのエネルギー状態を持っていて、最もエネルギーの低い状態を基底状態、それ以外の状態を励起状態と呼ぶ。そのエネルギーの低いものから、第1励起状態、第2励起状態(n =1, 2, …)と名づけられている。原子内の電子は、光を吸収することによって段階的にエネルギーを得て、より高いエネルギー準位へと移動する。
一方、エネルギー準位の低い方へ原子が移動する時は、光を放射することによってエネルギーを外に放出する。この光を放出したり吸収したりして、エネルギー準位が移り変わる事を遷移と言う。
通常、光を吸収し高エネルギー電子を持った化合物の殆どは、吸収されたエネルギーを熱に変換して、電子は単純に元の基底状態に戻る。しかし、光合成系のクロロフィルのように、適当な電子受容体が近くにあれば、励起された電子は、もとの分子からこの受容体へ移動する。これにより、もとの分子は電子を失い正電荷が生じ、受容体は電子を獲得して負電荷を帯びる。これを光誘導性電荷分離photoinduced charge separationと呼ぶ。
葉緑体には、この電荷の分離が生じる場が、光化学系それぞれにあり、反応中心reaction centerと呼ばれる。光合成の機構は、光誘導性電荷分離へと進む電子を可能な限り多くするため、基底状態に戻る電子を少なくするよう巧みな配置がなされている。こうして光吸収で取り入れた分子から得られる電子は、還元力を持つようになり、その光から得られたエネルギーが、他の分子を還元する化学的エネルギーとして保存される。
光エネルギーが化学エネルギーへの変換効率efficiencyの実態は、極めて低く最適波長でも約27%である。しかも蓄えられたエネルギーの大半は、細胞の維持に利用され、バイオマスbiomass(それぞれの生態系に属する生物の乾燥重量)を作るのに使われる量は限られている。バイオマスは、化石燃料と違い光エネルギーを使って水と二酸化炭素から有機化合物を生合成するものなので、持続的に再生可能な資源であることが大きな特徴である。
吸収された光子は、ほぼすべてが、光化学系過程で利用されるが、各エネルギーの1/4のみが蓄積され、残りは熱に変換され、太陽光エネルギーの約半分のみが植物に吸収される。しかしながら、すべての損失過程を考慮すれば、全体としてのバイオマスへの変換効率は、C3植物(クロレラなどの藻類やイネ,コムギ,ダイズ,ナタネ,ホウレンソウなど多くの植物)で4.3%、C4植物(ベンケイソウ型有機酸代謝を行う植物)では6%と見られる。
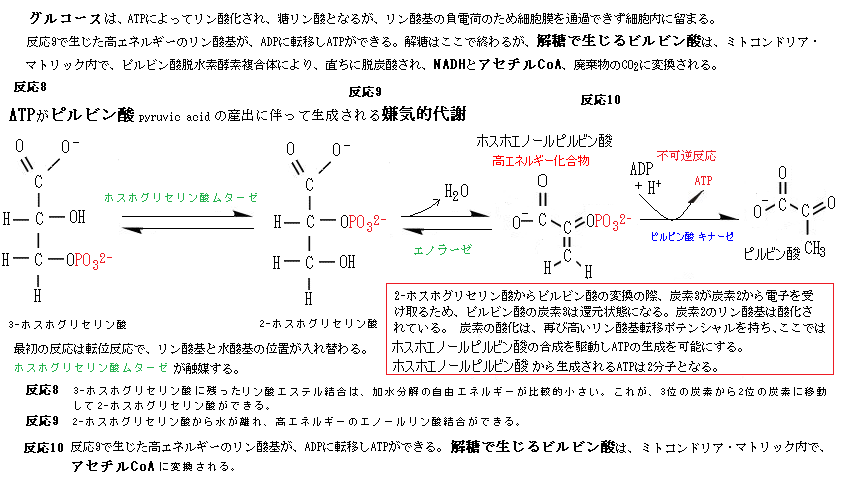
光合成は明反応light reactionと暗反応dark reactionの2段階からなる。明反応では、太陽光のエネルギーを利用して水と二酸化炭素から還元力とATPへと変換する。もう1つの段階は暗反応と呼ばれ、明反応によって作られた還元力NADPHとATPを駆動力として、完全に酸化された状態の二酸化炭素を還元して、より還元された六炭糖(ヘキソースhexose)を作る。六炭糖とは、単糖類のうち、分子式C6H12O6で示されるものの総称で6個の炭素原子を持つ。主なものはグルコース・マンノース・ガラクトース・フルクトース・タガトース・ソルボースなどの種々の糖質が作られる。いずれも、様々な過程で働く、特に炭素燃料として利用できる形で捕捉される。
光合成生物は、太陽光をエネルギー源にして、二酸化炭素と水からグルコースなどを合成し、燃料や生体分子の炭素骨格に使われる炭素原子を生物界へ取り込む働きをする。暗反応はカルビン回路Calvin cycleとも呼ばれ、明反応のように太陽光を直接必要としない反応である。しかしながら、光合成の明反応と暗反応が協同することにより、光エネルギーが炭素燃料へ変換されるのである。
細胞呼吸は、グルコースをCO2へ酸化するとともにO2を水に還元し、ATPを作る反応過程である。
細胞呼吸 C6H12O6 + 6O2 ➡ 6CO2 + 6H2O + ATP光合成
光合成では、その過程が逆で、大気中のCO2を還元し、土中のH2Oを酸化しグルコースなど合成する。
光合成 太陽光エネルギー + 6H2O + 6CO2 ➡ C6H12O6 + 6O2
細胞呼吸と光合成の化学的反応は、互いに逆反応であるが、両者の生化学反応の原理には一貫した流れがある。この2つを支配する生化学反応の原理に共通するのが、高エネルギー電子の存在である。
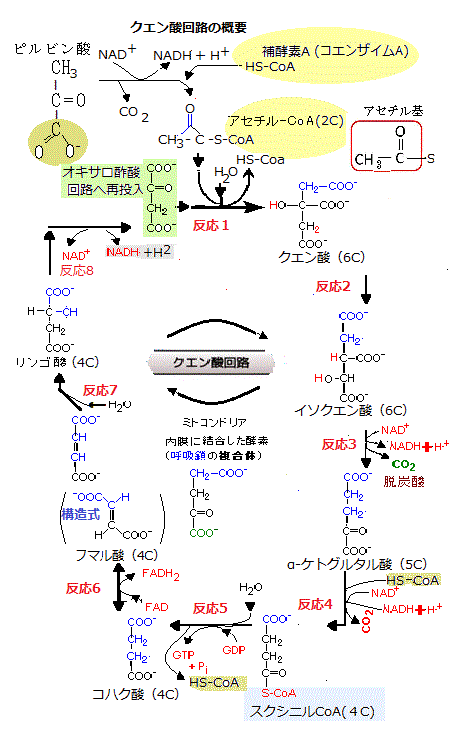 ミトコンドリアにおけるクエン酸回路citric acid cycleは、炭素燃料をCO2へと酸化することにより高エネルギー電子を産出し、この高エネルギー電子が電子伝達系に流れることによりプロトン駆動力が生じる。プロトン駆動力はATP合成酵素によって変換されATPが合成される。
ミトコンドリアにおけるクエン酸回路citric acid cycleは、炭素燃料をCO2へと酸化することにより高エネルギー電子を産出し、この高エネルギー電子が電子伝達系に流れることによりプロトン駆動力が生じる。プロトン駆動力はATP合成酵素によって変換されATPが合成される。このグルコースの好気的代謝は、グルコース誘導体を完全に酸化して二酸化炭素にするところから始まる。この酸化を行うのがクエン酸回路の一連の反応である。クエン酸回路は、グルコースの酸化によって、組織に燃料として供給するためのエネルギーの大部分を放出し、ATPとして捕捉する。クエン酸回路が1回転するごとに、12個のATP分子がつくられる。さらに、呼吸鎖における酸化的リン酸化によりATPが作られる。
クエン酸回路については、反応を進めるのに必要な大気中のO2が、廃棄物として放出されるCO2となると誤解されがちだが、実際は、クエン酸回路に入ったアセチル基をCO2にするのに必要な酸素原子は、大気中のO2ではなく地中のH2Oから供給される。
光合成は、すべての生物が必要とする基本的な有機成分を供給する。呼吸は、関連した炭素代謝とともに、炭素化合物に蓄えられた化学エネルギーを、厳密に制御された方法で、細胞内の必要性に応答して遊離し、それに伴い生合成に不可欠な多くの炭化化合物の前駆体も生産する。
動物細胞も植物細胞も、有機分子の化学結合に蓄えられた化学エネルギーに頼る。有機分子とは、植物が光合成の第2段階で自家消費用として作った糖や、動物が食餌により獲得する大小の分子の化合物である。生物は、このエネルギーを活用するため、緩やかな酸化、則ち制御された燃焼を行う。
酵素を要求する好気呼吸は、ほぼすべての真核生物に共通するが、植物の呼吸の概略も、動物や他の好気性の真核生物の細胞呼吸と類似し、解糖系・クエン酸回路・電子伝達系の3段階で進行する。しかし、植物の呼吸は、いくつかの点で動物のものと異なっている。
それを生み出した植物の功績により、地球の大気には、酸素が21%含まれている。その酸素は、エネルギー的に最も安定した形が、炭素と結合するCO2であり、水素と結合するH2Oである。細胞は、糖などの有機分子の炭素原子と水素原子を酸素と結合させている。これが酸化である。それぞれCO2 とH2Oに変えてエネルギーを獲得する。この過程が呼吸respirationである。
葉緑体が、CO2からグルコースを合成するためには、高エネルギー電子は2つの目的、CO2を還元するための還元力をNADPHの形で得るためと、還元の原動力となるATPを作るために必要になる。光合成においては、光エネルギー-を利用することで、電子が低いエネルギー状態から高いエネルギー状態へと励起される。高エネルギーの不安定な状態では、この励起された電子は周辺の分子へ移動できる。この励起された電子は還元力を作るのに使われ、あるいは膜を横切るプロトン駆動力を作るのにも使われる。更に、この駆動力が後にATPの原動力になる。光が吸収され、そのエネルギーは水から電子を奪いNADPHを発生させ、膜を通してプロトンを運搬するのに使われる。またこのプロトンは、ATP合成酵素がATPを合成するのに伴ってもとに戻る。太陽の光を原動力にする、この一連の反応を「明反応」と呼ぶ。
緑色植物の光合成は、2種類の明反応系によって行われる。光化学系Ⅰは、NADPHの形で還元力を生み出すが、その過程で電子が欠乏した状態になる。光化学系Ⅱは、水を酸化して得た電子を伝達することにより、光化学系Ⅰが失った電子を補充する。そして、これらの反応の副産物がO2である。光化学系Ⅱから光化学系Ⅰへの電子の流れによって、膜内外にプロトン勾配が生じ、水の酸化により放出されプロトンがこの勾配をさらに強め、これがATP合成の駆動力になる。細胞呼吸と光合成は、よく似た原理で行われているのを反映して、細胞呼吸はミトコンドリア、光合成は葉緑体と、どちらも二重膜のでできた細胞小器官で行われる。
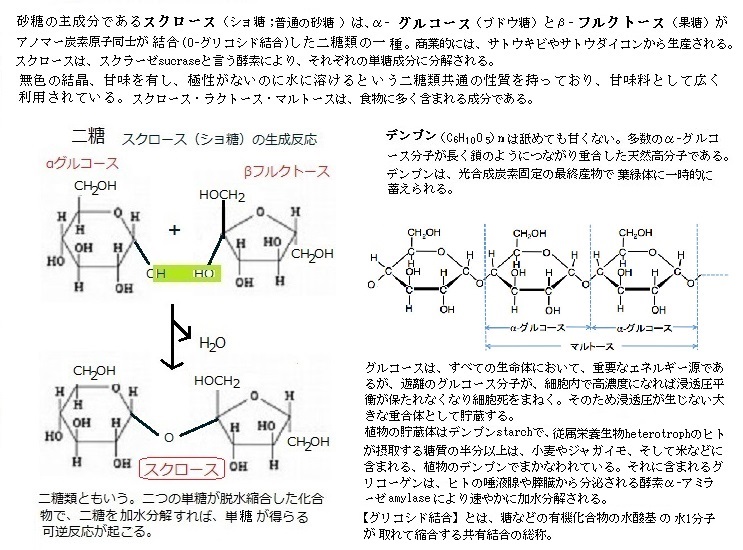
ミトコンドリア
植物界や動物界の真核生物は、多数の細胞が集まることで組織・器官を形成し成り立っている(多細胞生物)。その最小単位である真核細胞は、核を中心に小胞体やゴルジ体、さらにはミトコンドリアなどの様々な細胞小器官organelleが独自の機能を発揮して、それぞれが細胞の営みに関わっている。なかでもミトコンドリアmitochondrionは、特段、ユニークな構造と機能を持つオルガネルorganelleで、平均的長さは2µmで、真核細胞に大量に存在する。二重膜で包まれた構造で、内側の膜は折り畳まれたクリステcristae構造(ひだ状構造)となり、内部のマトリックスに入り込んでいる。
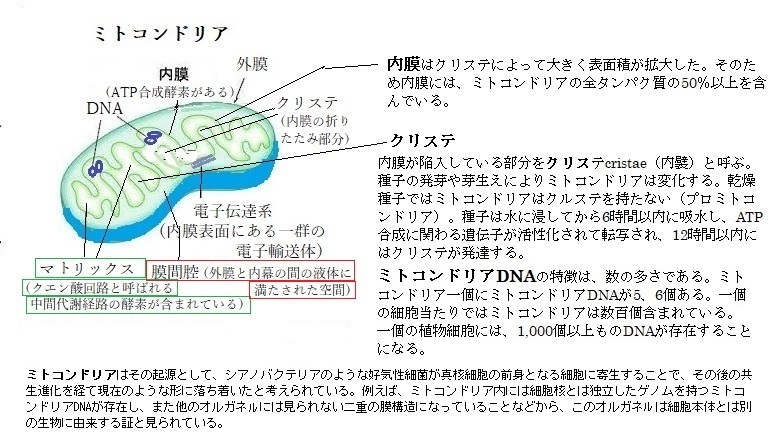
核内DNAとは完全に独立した環状DNAの殆どは、例外なく、父親の関与がないまま母親から子へと受け継がれる。また葉緑体と同様、半自律的な細胞小器官であるため、二分裂して増える。またミトコンドリアDNAは、その細胞小器官内に独自のリボソームribosome(細胞のタンパク質合成装置)を構成する特異的なRNAをコードしている。ATPを生産する主要部位であるため、クエン酸回路と酸化的リン酸化に関与する数種類の呼吸酵素もコードしている。
植物細胞には、核ゲノム以外に2つのゲノムがあり、1つがミトコンドリア・ゲノムmitochondrial genomeで、これは動物細胞にもある。もう1つが色素体plastidのゲノムplastid genomeである。色素体の内、専ら光合成を行うように分化したものを葉緑体chloroplastと呼ぶ。ここでいうミトコンドリアゲノムとは、ミトコンドリアDNA(mtDNA)の塩基配列情報のことを指す。ミトコンドリアゲノムの解析では、mtDNAに存在する遺伝情報に含まれるタンパク質コードのみならず、遺伝子間領域なども含むDNA塩基配列情報を研究対象にする。実は、mtDNAの姿自体、生物種ごとに大きく異なる。しかしながら、広く紹介されているのはヒトやマウスのmtDNAばかりであり、その他の生物種についての情報は、ヒトmtDNAのコードと共通するが、それぞれが進化の過程で重層的な発展過程をたどるため、特にmtDNAの多様性に注意する必要がある。合わせて、細胞の状態によってmtDNA分子の姿や量は大きく変化している。植物のmtDNAは、動物のmtDNAとは異なり、非常にゆっくり進化してきた。
DNAは化学的に非常に安定している。遺伝子の格納場所としては最適である。そのため適切な条件が整えば、DNAは永年、残存し続ける。ポリメラーゼ連鎖反応polymerase chain reaction(PCR)法により、1分子のDNAを解析や操作が行えるレベルの量にまで、DNA配列を何億倍にも増幅させることが可能になった。このため病原体の検出や遺伝子の同定、遺留 された毛髪による本人の特定ばかりか、何万年前に絶滅した生物の化石から遺伝子の配列を決定できるようになった。それでも、古代に生息する生物のDNAの塩基配列を正確に決定するためには、信頼できる増幅を可能にする十分な量のDNAを確保するとともに、他のDNAの混入を厳密に排除することが不可欠である。
コンビナトリアルケミストリーcombinatorial chemistryは、直訳すれば「組み合わせの化学」、それは化合物誘導体群の合成技術とその方法に関する有機化学の一分野である。コンビナトリアル・ケミストリーでは、構造的に関連する、少しずつ違う化合物を、一気に、しかも系統的に多種類にして多数の低分子化合物を生成する技術である。例えば、組み合せを利用して多数の化合物を効率的に合成するため、関連のある30種類の化合物群と別な30の化合物群を組み合わせて反応させ、900種類の生成物を作り出す。
コンビナトリアルケミストリーは、極めて多くの分子を一度に生成して、それらから生化学的な性質を持つ分子を選抜する方法であるため、進化のごく初期の段階にある分子を捉えることもできる。初めはアミノ酸を構成単位とするペプチドの合成のために開発された技術であった。ペプチドは医薬品にはなりにくいため、製薬会社からそれほど注目されなかったが、医薬品になりうる低分子化合物にも応用できることが分かり、現在、製薬会社を中心に「爆発的なブームを起こしている」ほどの化学技術である。
PCR法と高度なDNA配列決定法の開発により、古代のDNAも増幅できるようになり、その塩基配列決定が容易になった。この方法により3万8千年前と推定されるネアンデルタール人の骨から単離(生体や生物組織から、特定の細胞や遺伝子、タンパク質などを分離すること)されたmtDNAに適用された。ネアンデルタール人と現生人類Homo sapiens(‐séɪpiènz、homo;人(ラテン語)、sapiens;wise)のmtDNA完全長配列を比較すると、201~234の塩基置換が見られた。一方、チンパンジー同じ領域で比較した場合、約1,500の塩基置換があった。
約5万年前の骨から単離されたDNAを使うことで、ネアンデルタール人と、その近縁のデニソワ人Denisovansの完全なゲノム配列が得られた。その配列を比較すると、現生人類とネアンデルタール人の共通先祖は、約57年前に存在し、ネアンデルタール人とデニソワ人の共通先祖は、約38年前に存在していたようだ。
これらのmtDNA完全長配列に基づき進化系統図を描けば、ネアンデルタール人とデニソワ人共通の祖先は、570,000年前に現生人類と分岐し進化し、ネアンデルタール人とデニソワ人も380,000年前には、互いに分岐し進化したが、ともに正当な系統がとぎれた絶滅種となった。ネアンデルタール人は、28,000年前に絶滅した。それでも、ネアンデルタール人やデニソワ人、そして現生人類は、氷河時代のヨーロッパやアジアにおいて、ある程度、交雑していた。現代のアジア人やヨーロッパ人も、ネアンデルタール人とデニソワ人の遺伝子を保有している。デニソワ人には多くの謎があり、化石の断片から5万年以上前のものだということ以外は分かっていない。放射性炭素年代測定によって特定できる年代は、ここまでが限度であり、それより時代を下るIn more recent years 年代の化石は未だ発見されていない。
さらに、これらのmtDNA完全長配列の解析が進めば、これらのグループ間の異種交配の研究が加速し、その集団の生息範囲と、その環境が解明されるばかりか、未だ、mtDNA配列が知られていない新たなグループの追加も期待される。
かつては、細胞小器官の染色体は、細菌のプラスミドplasmidDNAのように、ゲノム全体が1つの環状となったDNA分子からなると見られていた。最近の研究では、ミトコンドリアや色素体の殆どは、むしろ、そのゲノムDNAは直鎖分子で、時には、ゲノム1コピー相当以上のDNAが縦に並んで繋がっていることもある。
顕微鏡観察では、細胞小器官の染色体DNA分子が樹の枝のように高頻度に枝分かれした様子が観察されている。複製途上にあるDNA分子の構造と見られている。細胞小器官の染色体は、核染色体のように単純な直鎖構造ではない。核の染色体は世代を重ねてもサイズに変化は生じないが、ミトコンドリアや色素体の染色体は、サイズを変えることがある。ミトコンドリアや色素体の染色体DNAサイズは、組織や細胞の発展段階で変化する。例えば、1コピーにも満たない断片しかないどころか、DNAが殆どない、もしくは全く持たない細胞小器官も観察されている。細胞小器官が、常に完全な1コピーのゲノムを含んでいるとまでは言えないようだ。
植物の 色素体のゲノムのサイズは、120~160kbp(キロベースペア;千塩基対単位)で、光合成や色素体ゲノムの発現に必要な遺伝子群をコードしている。ミトコンドリアゲノムのサイズの方は、180kbp~11Mbp(メガベースペア;万塩基対単位)とより大きく、しかもかなり幅もあり、更に色素体より格段に変化に富む。ヒトゲノムのサイズとなれば、3Gbp(ギガベースペア;億塩基対単位)にまで及ぶ。
かたや、動物や菌類のミトコンドリアゲノムの方は、15~50kbpに過ぎない。植物の方が格段に大きい。このゲノム間のサイズの差は、タンパク質をコードしていない繰り返しDNA配列の違いによるところが大きい。
 植物のミトコンドリアDNAは、電子伝達系に必要なタンパク質や、電子伝達に関わる補因子cofactor類をコードする遺伝子群を持っている。補因子は、タンパク質からなる酵素の触媒活性に必要な非タンパク質の低分子の有機化合物である。その単体や化合物として存在し、酵素と可逆的に結合する。
植物のミトコンドリアDNAは、電子伝達系に必要なタンパク質や、電子伝達に関わる補因子cofactor類をコードする遺伝子群を持っている。補因子は、タンパク質からなる酵素の触媒活性に必要な非タンパク質の低分子の有機化合物である。その単体や化合物として存在し、酵素と可逆的に結合する。酵素の多くは、それ単独だけでは、酵素活性を示さないものがある。単独で酵素活性を示さない酵素をアポ酵素apoenzymeという。アポ酵素は、補因子と呼ばれる非タンパク質性の低分子の有機化合物や金属イオンなどと複合体を形成して、初じめて酵素活性を示す。このアポ酵素と補因子の複合体をホロ酵素holoenzymeという。
接頭語の「apo- 」はギリシャ語の「…から離れて」や「…から別れて」に由来し、化学用語としては「分離した」あるいは「欠如した」の意味になる。「holo-」もギリシャ語由来で「完全」を意味し、生物学では「完全な」や「全体に」などの意を含める。
補因子は、大きく「補酵素coenzyme」と「金属イオン」の2種類に分けられる。補酵素の多くは、ビタミンで、酵素に弱く結合したり、強固に結合したりする。強固に結合している場合の補酵素を補欠分子族prosthetic group(ピリドキサールリン酸など、prosthetic;補綴(ほてつ)の;身体の欠損した部位の形態と機能を人工物で補うことを指す)と呼ぶ。一方、緩く結合している補酵素は、補助基質(ATPなど)と呼ばれ、ちょうど基質や生成物が酵素とくっついたり離れたりするように、酵素と相互作用する。補助基質と酵素本体のタンパク質との結合は共有結合ではなく、ゆるやかな結合である。補酵素としては約10種類が知られており、補酵素を必要とするの酵素は、酸化還元作用や、化学基の転移などを触媒する酵素である。加水分解反応をする酵素などは、補酵素を必要としていない。
補酵素とは、酵素の働きを助ける低分子量の有機化合物のことで、ユビキノンやビタミンなどが様々な反応系において補酵素として働く。主に、酵素の基質となって反応ごとに酵素の活性部位から離れて別の酵素の働きで元の構造に戻る補助基質(ATPなど)と、ビオチンがアポ酵素のピルビン酸カルボキシラーゼと強く共有結合するするなどの補欠分子族の2つがある。緩く結合する補助基質は、基質やその生成物が、酵素とくっついたり離れたりするように、酵素と相互作用をする。その一方、様々な酵素が同じ補酵素を利用することや、主にビタミン由来であることなどで、補酵素は通常の基質substrateとは異なる。通常、同じ補酵素を利用する酵素の反応機構は似通っている。
「補助基質」には、ATP・S-アデノシルメチオニン・UDPグルコース ・NAD+とNADP+・補酵素A(由来:パントテン酸)・テトラヒドロ葉酸(由来:葉酸)・ユビキノンなど、「補欠分子族」には、FADとFMN(由来:ビタミンB2)・チアミン二リン酸(由来:ビタミンB1)・ピリドキサールリン酸(由来:ビタミンB6)・ビオチン・レチナール(由来:ビタミンA)などがある。「補欠分子族」に含まれる補酵素は、B群のビタミンから出来ている。 食物から取り入れられたB群のビタミンが、体の中で修飾を受けて補酵素に変わるのである。 食物中のビタミンが欠乏すると、生体に欠乏症状を引き起こすことにからみても、補酵素が生体内の反応で 重要な働きをしていることが分かる。
このように、酵素には、補酵素(補助基質や補欠分子族)などの有機化合物を補因子とするものや、金属イオン(Mg2+・Fe2+・Ni2+・Moなど)などの無機物を補因子とするものがある。補因子が金属イオンなどである場合は、「金属イオン補因子」と呼ぶ。銅イオン・鉄イオン・マンガンイオン・ニッケルイオン・モリブデンなどがある。 タンパク質の一部を構成しており、常時結合しているものである。 多 くの酵素は、その活性において有機化合物(補酵素)の「補助因子」を必要とし、または金属イオンを「活性化因子」にしている。基質に対して官能基の受容体、あるいは供与体として作用することが多い。NADやNADPも「補因子」として働く。
アポ酵素とは、それ自体では酵素としての活性をもたない酵素のことで、アポ酵素に補因子が結合することで初めて活性をもった酵素として機能することができる。これをホロ酵素と言う。また多くの酵素の触媒活性には、小分子である補因子を必要としている。しかも、補因子と酵素の組み合わせにより、正確な役割は異なってくる。この補因子により、通常では標準的な20種のアミノ酸が行えない反応を起こすことが可能になる。すなわち、タンパク質のみのアポ酵素に補因子が結合したものがホロ酵素(タンパク質+補因子)になる。
アポ酵素 + 補因子(補酵素など) ⇆ ホロ酵素
すべての生物系において重要な活動とは、エネルギーを一つの形から別の形に変換することである。光合成では、光エネルギーを化学結合エネルギーに変換する。ミトコンドリアで起こる細胞呼吸では、食物から得られた小さな分子のギブズエネルギーが、まずイオンの濃度勾配というギブズエネルギーに変換され、それからアデノシン三リン酸(ATP)のギブズエネルギーに変換される。ATPは、生物の生命活動のエネルギー媒介物質でる。細胞内では、ATPがアデノシン二リン酸(ADP)と無機リン酸(Pi)に加水分解されるときに放出されるエネルギーが使われる。
生体系において、ATPは、長期間維持されるエネルギーの貯蔵体ではなく、短期のギブズエネルギーの主な供与体として存在している。ヒトの通常の細胞では、ATP分子は作られてから1分以内に消費さているのが実態である。そのせいか体内のATPの総量は、約100gほどと限られている。その余りにも少ないATPの量のため、ATPの代謝回転は非常に速い。
例えば、ヒトは安静時でも24時間に約40KgのATPを消費し、激しく運動する最中であれば、その消費速度は毎分0.5kgにもなる。言い換えれば、2時間のランニングでは、60kgのATPが消費されることになる。そのためATPの再生機構が重大な役割を担う。細胞内の小器官の動き・能動輸送・シグナルの増幅・タンパク質の生合成などは、ADPからATPの再生が継続する限り可能となる。ATPの合成には、異化作用が重要で、グルコースや脂肪なのどの燃料分子を形成する炭素が、CO2に酸化される度に放出されるエネルギーが、ADPとPiが脱水結合しATPが再生される際に使われる。
好気生物における炭素が酸化される際の最終段階の電子受容体はO2でであり、その酸化生成物がCO2となる。つまりグルコースなどの糖質より、脂肪の炭素原子の方がより還元されているため効率のよい燃料源となる。
燃料が酸化される際には、一度に一個の炭素が酸化され、それにより生じるエネルギーは、高いリン酸基転移ポテンシャルを持つ化合物を作るために使われ、あるいは、イオン勾配の形成にも使われもするが、いずれにしても最終目的は、ATPの生成である。
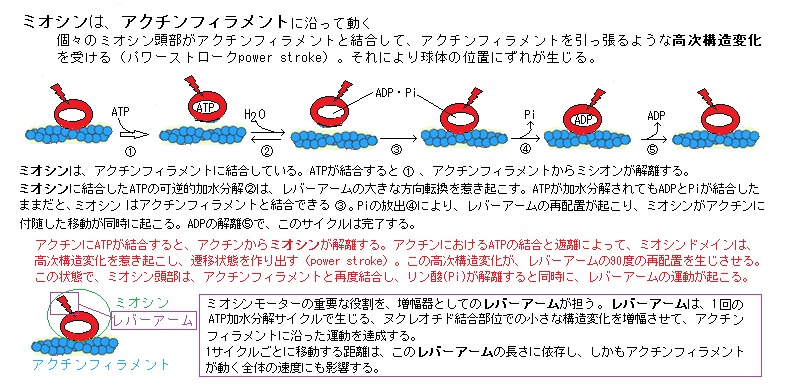
生体内では、酵素がエネルギー変換に中心的な役割を担い、光合成や細胞呼吸で重要な役割を果たしている。様々な酵素によってATPの化学エネルギーは、様々な形で利用されている。例えば、筋肉の収縮では、ATPの化学エネルギーを力学的エネルギーに変え、ミオシンmyosin酵素のコンホメーション変化を利用して、ATP加水分化と機械的仕事を共役させている。アクチンActinとともに働くモータータンパクは、すべてミオシンmyosinファミリーに属する。ミオシンがATPと結合して、その加水分解エネルギーを使ってアクチン・フィラメントF-Actinに沿って移動することで筋収縮が起こる。つまり、筋肉はミオシンとアクチンの複合体である。
アクチン分子は重合して連なり、繊維状のアクチン・フィラメントとなって細胞の骨格を形成している。またそれと同時にアクチン・フィラメントは、遊走・接着・移動といった細胞運動において中心的な役割を担っている。細胞質内には分子量約 42kDa(キロドルトン;1Daは、水素原子1個分に相当する質量を1とする質量単位、1kDa=1,000Da)の単量体アクチンの多くが、ATP が結合した状態で存在し、これら ATP 結合型アクチンが可逆的に重合し、アクチン・フィラメントを形成する。
このアクチンは、すべての真核細胞に多量に存在し、通常は、真核細胞のタンパク質の10%もの量を占め、極めて重要で、かつ多量に発現している。ミオシン類は、軌道として働く、長い重合体巨大分子のタンパク質アクチンに対して、異なった親和性を持った複数の状態間を遷移することにより運動する。つまり、筋肉の構造と筋収縮時の細胞の運動において、ミオシン類とアクチンが重要な働きをする。また、細胞骨格の主要な構成成分でもある。
ミオシン類は、アデノシン三リン酸を加水分解して、アデノシン二リン酸(ADP)と無機リン酸(Pi)を生成する反応を触媒し、その熱力学的に有利な反応と結びついたエネルギーを利用して、細胞内の分子の運動を駆動させる。ヒトの筋肉運動も、筋肉にあるミオシンによって触媒されたATPの加水分解に由来する。ミリオン類はすべての真核生物に存在し、ヒトゲノムには40種類以上の異なるミオシンがコードされている。
アクチン・フィラメントは通常、長い構造体となっているが、球状のドメインを持ち、この球状のATPアーゼaseドメイン(アーゼ(-ase)は、生化学において、酵素の命名に用いられる接尾辞である。酵素の最も一般的な命名では、基質名にこの接尾辞が付けられる)でATPを加水分解させ、その反応と結びついたギブズエネルギーを利用して、アクチン・フィラメント分子内に大きなコンホメーション変化を引き起こし、アクチン・フィラメント分子の長く伸びた部分の構造を増幅され、タンパク質やその他の荷が、細胞内の決して短くはない距離間で運ばれる。
多数のミシオン頭部を素早く、しかも独立して1本のアクチンフィラメントに結合させ、そのアクチンフィラメントを動かせることで、1分子のモータータンパク質よりも格段に大きい速度で収縮させられる。また、ミシオンモーターの重要な役割を、増幅器としてのレバーアームが担う。レバーアームは、1回のATP加水分解サイクルで生じる、ヌクレオチド結合部位での小さな構造変化を増幅させて、アクチンフィラメントに沿った運動を達成する。1サイクルごとに移動する距離は、このレバーアームの長さに依存し、しかもアクチンフィラメントが動く全体の速度にも影響する。
二酸化炭素は、好気代謝の主な最終産物である。哺乳類では、二酸化炭素は血液中に放出され、肺に輸送されて呼吸で排出される。赤血球中では、二酸化炭素は水と反応する。この時の反応生成物が、中程度の強さの酸である炭酸であり、これがプロトンを失って炭酸水素イオンhydrogencarbonate(HCO3-)になっている。この反応はたとえ触媒がなくとも、この水が付加される反応は適度の速さで進む。この逆反応の炭化水素イオンの脱水は、より一層速い。平衡状態での[CO2]:[H2CO3]の比は340:1である。
CO2+H2O ⇔ H+ + HCO3-
CO2の水付加とHCO3-の逆反応の脱水反応は、特に運搬過程と共役することが多い。そのため殆どすべての生物は、触媒がなくとも、その可逆反応はある程度自発的に起こっている。その反応を瞬息化するのが、カルボニックアンヒドラーゼcarbonic anhydrase(炭酸脱水酵素、carbonic ;炭酸の、hydrase;加水酵素、anhydrase:脱水酵素)と呼ばれる酵素である。カルボニックアンヒドラーゼは二酸化炭素と水から、炭酸、水素イオンproton、炭酸水素イオン(重炭酸イオンbicarbonateと呼ぶこともある)への変換またはその逆方向への変換を瞬息に行うのを助ける酵素である。例えば、カルボニックアンヒドラーゼによって、血液が肺を通る際に、血液中のHCO3-は、息を吐く際に脱水されCO2を形成し、眼球や他の分泌器官では、水性体液で潤すためCO2は、逆にHCO3-へ変換され輸送される。
呼吸は生命における基本的な機能である。肺胞では吸気とともに入ってきた大気中の酸素oxygenが血液に入り、血液中の二酸化炭素が肺胞に拡散する。つまり、酸素と二酸化炭素という2種類のガスが交換される。
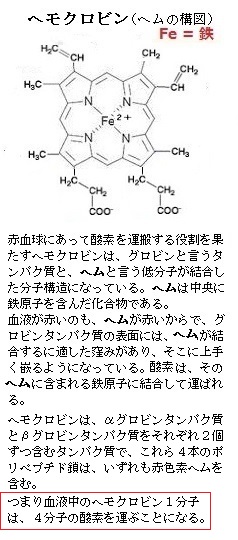 呼吸で吸い込む空気には、細胞内にある糖と脂肪を分解するための燃料を供給してくれる貴重な酸素を含んでいる。その発生するエネルギーは大きい。肺の中で、酸素は血液中に拡散して
ヘモグロビンhemoglobinと結合し、身体中のあらゆる細胞へと輸送される。ヘモグロビンは2種のαグロビンタンパク質とβグロビンタンパク質が2本ずつの計4本で形成されている。これら各々のポリペプチドに鉄イオンFe2+を含むヘムを1分子ずつ含有した構造をしている。つまり、1分子のヘモグロビンは4分子のヘムを持ち、その4分子のヘム各々が酸素と結合し、組織に酸素を運んでいる。
呼吸で吸い込む空気には、細胞内にある糖と脂肪を分解するための燃料を供給してくれる貴重な酸素を含んでいる。その発生するエネルギーは大きい。肺の中で、酸素は血液中に拡散して
ヘモグロビンhemoglobinと結合し、身体中のあらゆる細胞へと輸送される。ヘモグロビンは2種のαグロビンタンパク質とβグロビンタンパク質が2本ずつの計4本で形成されている。これら各々のポリペプチドに鉄イオンFe2+を含むヘムを1分子ずつ含有した構造をしている。つまり、1分子のヘモグロビンは4分子のヘムを持ち、その4分子のヘム各々が酸素と結合し、組織に酸素を運んでいる。糖と脂肪が酸化分解されると、副産物として二酸化炭素carbon dioxideが細胞で生成される。この排泄物を身体から除去する必要がある。そこで再び血液が輸送媒体としての役割を果たす。二酸化炭素は細胞の外へと拡散し、何種類かの方法で血液中を輸送される。10%未満は血漿blood plasma(血液に含まれる液体成分の一つ、血液の55%を占める)中に溶けて、約20%はヘモグロビンと結合して輸送されるが、70%位は、炭酸carbonic acidに変換されて肺へと輸送される。赤血球red blood cell中にあるカルボニックアンヒドラーゼが、二酸化炭素を炭酸と重炭酸イオンbicarbonate ionに変換する作用を助ける。赤血球が肺に到達すると、同じ酵素が重炭酸イオンを二酸化炭素に戻す変換を助け、できた二酸化炭素は呼吸によって排出される。この反応は酵素がなくても起こるが、炭酸脱水酵素により、その変換速度は100万倍にまで加速する。
さらにCO2や逆にHCO3-は、様々な酵素の基質や生成物となっており、その種の酵素に適する基質濃度を得るため、急速に相互交換をする必要がある。ヒトでは、これらの酵素は大変重要なので、カルボニックアンヒドラーゼの変異が、大理石骨病(遺伝子の異常により全身的に骨が異常に硬く脆くなり、 骨折をしやすくなる病気)の原因にもなる。大理石骨症では、骨の丈夫さが損なわれることから、骨折ばかりか、背骨のゆがみや骨髄や関節の感染症が生じることもある。骨病変に関連して、神経症状が引き起こされ、ひいては視力や聴力の低下、顔面の筋肉の麻痺などに及ぶ。成長障害や知的障害、てんかんなどが生じることもある。
カルボニックアンヒドラーゼは、CO2の水付を劇的に速める。この最も活性が高い酵素は、酵素分子あたり1秒間に100万回という速さでCO2を水和する。
カーボニックアンヒドラーゼは、水中でCO2と重炭酸イオンHCO3-との平衡反応を触媒する酵素で、活性中心に亜鉛イオンを配位する。
実は、数百の酵素が亜鉛を含んでいる。亜鉛は生体系では、亜鉛イオンZn2+状態だけで見出されている。しかも、全酵素の1/3が金属イオンと結合しているか、あるいは、その活性化のためには、金属イオンの添加を必要としている。金属イオンは、化学反応を高めるために、正電荷を持っている。その結合は強いが、反応速度は安定していない。加えて、pH(potential of hydrogen)の変化が、カルボニックアンヒドラーゼが触媒するCO2の水和反応速度を変える。カルボニックアンヒドラーゼは、pHが高い(アルカリ性)ほど最大活性になる。
金属イオンが持つこれらの化学反応性が、進化の過程で金属イオンが触媒として採用された重要な要素material factorとなったと見られる。ヒトには、少なくとも7つのカルボニックアンヒドラーゼが機能し、その各々の酵素は独自の遺伝子を持っている。しかしながら、アミノ酸配列の同一性が相当高いため、その7つすべてが共通する先祖に由来するホモログhomolog(相同遺伝子)である、と見られている。
植物のミトコンドリアDNAは、電子伝達系に必要なタンパク質や、電子伝達に関わる補因子類をコードするが、それに加えて、植物のミトコンドリアは、細胞小器官として、自身の遺伝子発現に必要なタンパク質、例えば、リボソームタンパク質やtRNAやrRNAをコードしている。 しかしながら、ミトコンドリアと色素体は、それぞれ細胞小器官の機能に必要な遺伝子の大部分を、自身のゲノムにコードしていない。長い共生進化の過程で、これらの遺伝子は、現生植物の核ゲノムに移されている。ミトコンドリアも色素体も原核生物を起源とするため分裂により増殖するが、その細胞小器官の分裂とDNAの複製は、核の分裂とは独立して制御されている。ミトコンドリアと色素体の分裂のタイミングも、細胞分裂とは独立している。しかしながら、分裂過程自体には、核にコードされているタンパク質が不可欠である。
細菌とミトコンドリアや色素体などの細胞小器官に共通しているのが、やがて分裂面になる領域の内膜上に分裂リンクを形成するタンパク質が、その分裂を促進することにある。このようなタンパク質をコードする遺伝子は、植物細胞の核のみに存在する。そこから発現されたタンパク質は、近接する小胞体を介して分裂する細胞小器官の周りに運ばれ、内膜上に分裂リングを形成するようだ。
エネルギーや光合成の必要性に応じて、ミトコンドリアや色素体を分裂させずに、それ自体の大きさを調整することもある。例えば、ミトコンドリアの分裂に関わるタンパク質を、実験的に不活性化すると、ミトコンドリアの数は減るものの、サイズの広げて細胞が要求するエネルギーの需要に応えようとする。
植物のミトコンドリアは、限られた数であるがミトコンドリア・タンパク質をコードしたDNAなど、独自の遺伝情報を保持している。 しかも、細胞分裂を続けている際、1つの細胞の中のミトコンドリアの数や大きさは、分裂や融合に伴いダイナミックに変化する。エネルギー代謝の際におけるミトコンドリアの役割に応じて、代謝が活発な組織には、より多くのミトコンドリアを細胞内に配置する。例えば、孔辺細胞にはミトコンドリアの数が極めて多い。 気孔の構造も様々で、ヨーロッパ原産のイネ科の多年草オオアワガエリ(日本でも広く分布している植物で、夏から秋にかけて花粉を飛ばす)の電子顕微鏡写真では、膨れた両端を持つ一対2つの孔辺細胞とその周辺の細胞からなる構造で、孔辺細胞間にでき、広がりを調節して開閉を行う。気孔は光合成が盛んに行われる晴天の時に開いて、葉から水を蒸散させ、根からH2Oや養分の取り込みを速め、同時に光合成に必要なCO2を取り込み、その光合成による排出物O2を放出する。蒸散は強い日差しで上昇した葉の温度を低下させる役割もある。
ミトコンドリアの細胞質のゲノムは、別の細胞に取り込まれた細菌細胞のゲノムが進化した名残である(細胞内共生説)。最初のミトコンドリアは、酸素を利用する好気的aerobic細菌が、別の原核細菌に取り込まれ、その後の長い年月の共生関係により、最初の共生体を単独では生きられない細胞内小器官organelleへと進化させた。これにより宿主細胞は、細胞内の共生体とともに1つの細胞の系譜を形成し、好気的代謝で酸素を利用できるようになった。この系譜は最終的には、すべての動物細胞に進化した。
また、植物細胞はその後の二次細胞内共生によって新たな系譜を積み重ねた。ミトコンドリアを共生させた細胞が、光合成を行うシアノバクテリアを取り込、それも長年月を掛けて細胞内の色素体として進化させた。そのため、ミトコンドリアも色素体も、原始的な好気的細菌や光合成細菌が、別の宿主の原核細胞の膜内に閉じ込まれた当時のままの状態で、細胞質内にありながら外膜と内膜を二重膜として残している。 それらの細胞小器官のゲノムは、原核生物のゲノムと配列が似ている、しかも細胞小器官のゲノムは、宿主が真核生物化した現在でも、原核生物のゲノムと同様に核膜がない核様体nucleoidのままである。
原核細胞には核膜がない、DNAは細胞膜や種々のタンパク質と結合して細胞質の一部分に 局在し、核様体を形成している。その様子は細菌切片 の電子顕微鏡像などで見ることができる。大腸菌を温和な条件で破壊すると、この核様体構造をある程度保持した複合体を分離することができる。その形態 を電子顕微鏡で観察すると、DNAは膜断片と付着し、DNAの2重鎖には切れ目が認められない。
また、細菌は細胞小器官を持っていないが、有性生殖に似た方法で遺伝物質の断片を交換する能力を有する。原核細胞は、分裂によりどんどん増殖し、栄養条件が良ければ、多くは20分で倍増し、11時間も経てば、その子孫は80億以上にもなり、現在の地球上における人口を上回る。そのため、原核細胞の集団は進化が速く、新しい栄養源を取り入れる力や、新しい抗生物質への抵抗性を持つものが直ぐに登場する。
光合成は、植物はもとより殆どすべての生物が必須とする有機成分を、太陽光エネルギーの助けを借り生合成する。呼吸は炭素原子を主とする炭素化合物を一連の炭素代謝とともに、その炭素化合物に蓄えられたエネルギーを精妙に制御された方法で、生体の細胞各々の必要性に応じて放出する。それに伴い「呼吸」と呼ばれる代謝で、その生合成に不可欠な多くの炭素化合物の前駆体が、諸段階的で化学合成される。
質量をmとすれば、重さはmに重力の加速度gを掛けたmgである。gは場所によって変化するから「重さ」もそれに伴い変化するが、「質量」は物質が持っている本来の特性であるから、場所によって変化することはない。
アインシュタインが1905年に発表した特殊相対性理論は、「質量とエネルギーとは相互に転換され得る」と、まさに革命的な結論に達した。これを契機に、物理学が大きく変容していく。「エネルギー」や「物質」という概念自体が大きく変わったのである。「E=mc²」という有名な式である(Eはエネルギー、mは質量、cは光速)。E=mc²という式が導く新たな法則は、「質量とエネルギーの総和は不変である」と言うことだ。E=mc²という式によって「物質(質量)とエネルギーは互いに転換され得る」ということを示す。このE=mc²が、「物質からエネルギーへ」転換する本質を解く鍵になる。
「エネルギー保存の法則」の「エネルギーの変換において、それに関わったエネルギーの総量は一定である」。変換前のエネルギーの総量と変換後のエネルギーの総量は変化しない。これを「エネルギー保存の法則」と言い、物理学で最も基本的な法則である。
「呼吸」と呼ばれる化学反応の際にも、質量がごく僅かずつ減っていく化学反応で発生するエネルギーも、この「エネルギー保存の法則」による。
酸素を要求する好気呼吸aerobic respirationは、ほぼすべての真核細胞に共通に見られるもので、植物の呼吸も、動物のものと異なるいくつかの点があるが、大筋は、動物や他の好気性の真核生物で見られる呼吸と類似している。好気呼吸とは、還元された有機化合物が、厳密に制御される方法で酸化される生物学的プロセスである。
呼吸によって自由エネルギーが放出され、そのエネルギーは一時的にアデノシン三リン酸adenosine triphosphate(ATP)として蓄えられ、成長や生命維持に必要な細胞での反応に利用される。そのATPは、アデノシンadenosineに 3 分子のリン酸、つまり三リン酸triphosphateが結合したヌクレオチドnucleotide(核酸の単位構造)である。生体内のエネルギーの貯蔵・供給・輸送を仲介している。そのATPが、アデノシン二リン酸adenosine diphosphate(ADP)への加水分解に伴いエネルギーを放出する。
生体内での加水分解の反応は、
ATP + H2O → ADP + P1
ATPより質量がより小さい2の分子、ADPと P1 に分解されるため、質量とエネルギーの総和は不変であるから、その過程でエネルギーが放出される。
グルコースは、呼吸の基質として一般的に利用されているが、殆どの植物細胞における還元炭素は、スクロースか、その他の糖、あるいは有機酸や光合成から得られるトリオースリン酸、脂質やタンパク質の分解によって得られる代謝産物などの化合物から得られている。
化学的に見ると、植物の呼吸は12個の炭素からなるスクロース分子の酸素の還元として表されている。
流れとしては
C12H22O11 + 13H2O → 12CO2 + 48H+ + 48e-
結果としては
C12H22O11 + 12O2 → 12CO2 + 11H2O
と表記される。
化学式に表れるように、この反応は、光合成とは、逆方向になっており、共役した酸化還元反応であり、スクロースは完全に酸化されてCO2になり、一方では電子の受容体としての役割を果たす酸素は還元されて水になる。
反応全体での標準ギブス自由エネルギーの変化(ΔG’)は、酸化されたスクロース1モル(342g)あたり、-5,760kJである。この大きな負の値は、平衡が右に大きく片寄っているため、右向きの反応が容易で、しかも多くのエネルギーがスクロースの分解によって放出されるようになる。ATPの合成に共役して起こるこの自由エネルギーの放出は、これが唯一と言うことではないが呼吸代謝の主要な役割である。
熱による細胞構造のダメージを防ぐために、細胞は一連の段階的生合成反応を踏まえてスクロースを酸化する。それらは、4つの主な過程、即ち解糖系・酸化的ペントースリン酸径路・クエン酸回路・酸化的リン酸化に分けることができる。これらの径路は、個別に分かれて機能しているのではなく、お互いに代謝産物を交換し合いながら機能している。次に呼吸の基質は、径路の異なったところで呼吸のプロセスに入って来る。
ホルモース反応
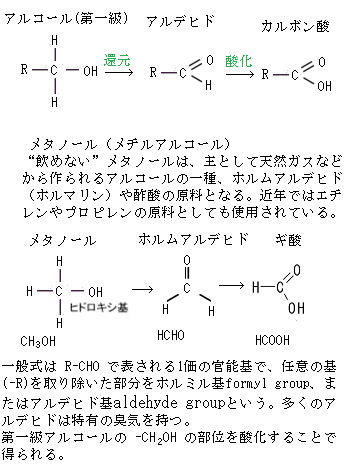 炭水化物とは、Cm(H2O)n と書くことができるものを指すが、糖質であるデオキシリボース(C5H10O4)は、例外となり、一方では糖質ではないホルムアルデヒド(CH2O)がこの定義に当てはまってしまう。
炭水化物とは、Cm(H2O)n と書くことができるものを指すが、糖質であるデオキシリボース(C5H10O4)は、例外となり、一方では糖質ではないホルムアルデヒド(CH2O)がこの定義に当てはまってしまう。CHO を持つ有機化合物をアルデヒドaldehydeという。またアルデヒドの -CHO の部分をアルデヒド基aldehyde groupという。アルデヒドは第一級アルコールが酸化したもので、アルデヒドをさらに酸化するとカルボン酸になる。
アルデヒドは反応性が高く、様々な反応を起こすので有機合成化学には欠かせない化合物である。ホルムアルデヒドformaldehydeは、アルデヒドとして最も代表的なものである。
ホルムアルデヒドの水溶液から、糖質が合成されることが発見された。この得られた混合物のことをホルモース(ホルムアルデヒドから人工的に作られる糖類という意味)と名付け、このような変換反応のことを「ホルモース反応formose reaction」と呼ぶようになった。
また、この反応は地球上の生命起源の黎明期に糖類が合成された過程として考えられ、バイオテクノロジーとしても、非常に安価な糖類合成のための原料となるホルムアルデヒドが、炭素と水から大量かつ容易に生産される原材料であることから重要である。
グルコースC6H12O6は、前生物的合成の条件でホルムアルデヒド(水に溶けるとホルマリン;主に防腐剤や接着剤に用いられ、安価であるので古くから建材などに使われてきた。しかしアレルギーの原因物質のみならず発ガン性の可能性がある)から作られる単糖の1つである。
グルコースは、大部分の臓器における共通した重要な燃料である。哺乳類では、グルコースは非飢餓状態でも脳が利用する唯一の燃料であり、また、肺で受取った酸素を全身に行きわたらせ、逆に不要となった二酸化炭素を全身から回収して肺に戻し、体外へ排出する赤血球が利用できる唯一の燃料である。殆どすべての生物は、グルコースを利用しており、大部分の生物は同様の様式でグルコースを代謝する。炭水化物は多種類存在するが、グルコースの方が他の炭水化物よりも燃料として優れているからである。
前述するように、炭素と水から大量かつ容易に生産可能な原材料であるホルムアルデヒドから、前生物的合成の条件で作られる単糖であれば、グルコースは原始的な生化学系の燃料として利用されていたと見られる。また、グルコースは、他の単糖と比較して、タンパク質への非酵素的な糖鎖形成を起こしにくい。グルコースは環状構造で存在する傾向が強く、結果としてタンパク質を修飾する傾向が少ない。
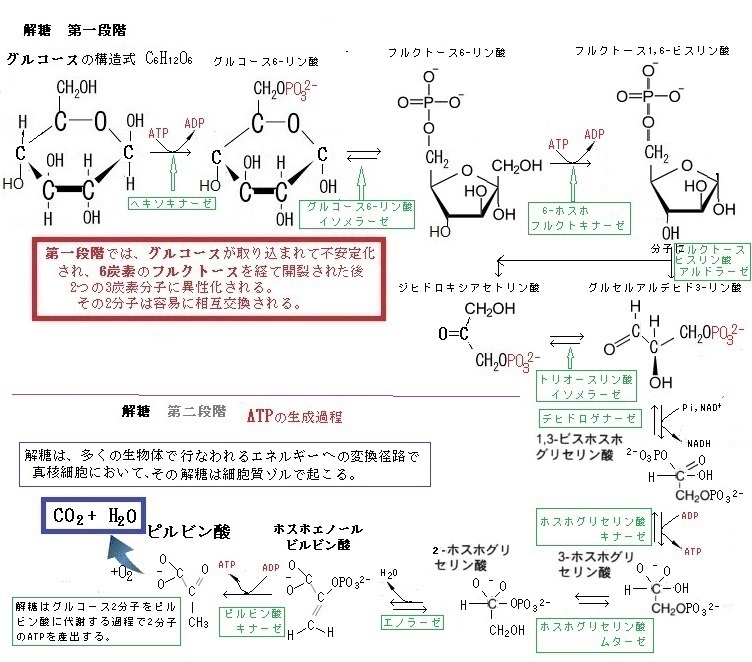
酸素の運搬が十分であれば、グルコースは、より効果的に二酸化炭素と水に代謝され、通常の生命活動の需要を満たすためのATPを産出することができる。解糖系glycolysis(「糖」と「分解」を意味するギリシャ語の「glykos」と「lysisi」を由来にする)は、サイトゾルcytosolとプラスミドplasmid(多くのバクテリアに存在する小型の核外遺伝子)の両方に局在する酵素によって触媒される一連の反応からなる。解糖は多くの生物体におけるエネルギー変換径路で、この径路は真核か原核を問わず、すべての細胞に共通する。
酸素があれば、グルコースはより効果的に二酸化炭素と水に代謝され、植物細胞間の原形質流動や動物の筋収縮の駆動などの需要を満たすためのATPを産出することができる。解糖は多くの生物体におけるエネルギー変換径路で、この径路は真核か原核を問わず、すべての細胞に共通する。 真核細胞において解糖の反応は、サイトゾル(細胞質基質;細胞質cytoplasmから細胞内小器官を除いた部分)で起こる。この径路は二段階からなる。第一段階では、グルコースがリン酸化・異性化・第二のリン酸化などの3つの過程をたどりながら、フルクトース1,6-ビスリン酸に変換されるが、未だ捕捉と準備の段階であるためATPは、段階的に投入されるが生成されない。これらの解糖の初期段階は、細胞内にグルコースが特異的な輸送タンパク質を介して取り入れ、ヘキソキナーゼhexokinaseによるリン酸化に始まり、6炭素のフルクトースが、最終的に、リン酸化されたグルセルアルデヒド3-リン酸化とジヒドロキシアセトリン酸の3炭素化合物に開裂し異性化 isomerization(ある分子の原子配列が変化して、原子の組成は全くそのままに、それぞれが異なる分子構造を持つ化合物に変換することである。それぞれの異性体は、物理的・化学的性質を異にする)することで完了する。
リン酸基転移は、生化学において基本的な反応で、キナーゼkinaseはATPからのリン酸基を受容基に転移させる反応を触媒する酵素である。その一つであるヘキソキナーゼは、グルコースやマンノースのような種々の六炭糖(ヘキソースhexose)へのATPからのリン酸基の転移を触媒する。 第二段階では、この容易に相互交換され得る3炭素化合物・グルセルアルデヒド3-リン酸がピルビン酸に酸化されるまでの過程でATPが生成される。
例えば、最初の段階では、スクロースは六炭糖リン酸(ヘキソースリン酸)に変換され、その後各々のヘキソースリン酸は、2つの三炭糖リン酸(トリオースリン酸)に分解される。次に起こるエネルギーを保存する段階では、各トリオースリン酸は部分的に酸化され、主に有機酸であるピルビン酸1分子へと変換される。別の有機酸であるリンゴ酸も植物の解糖の最終産物である。解糖系はクエン酸回路で酸化される基質を合成し、少量の化学エネルギーをATPやNADHとして蓄えっている。
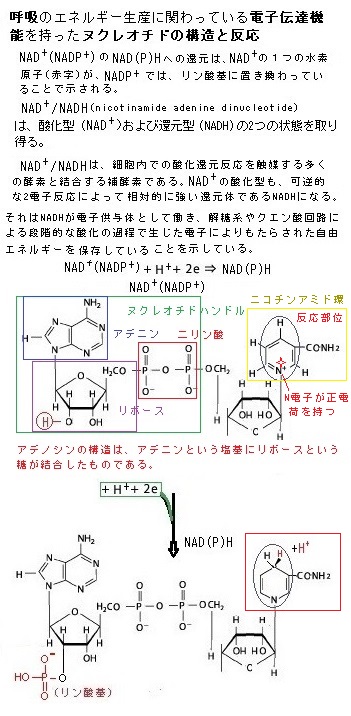 NADHは、酸化還元反応において水素の授受に関与する。最近では還元型ニコチンアミドアデニンジヌクレオチドreduced nicotinamide
adenine dinucleotideと呼ばれる方が多い。構造的にはNAD+とはリン酸基が付いただけの違いで、ともにデヒドロゲナーゼ(ピルビン酸からアセチルCoAを生成し、クエン酸回路に投入する働きをする酵素。逆反応を触媒する酵素はない)の補酵素となる。しかし、NAD+とは異なり、異化代謝ではなく、通常、脂肪酸合成や光合成のような同化代謝で利用される。補酵素の分子中には左の図のようにアデニンヌクレオチドAdenosine
diphosphate (ADP)を含むものが多い。アデニン、リボース、および二つのリン酸分子からなる化学物質、この部分は「ヌクレオチドハンドル」と呼ばれ、一般に補酵素の機能には関与しない。ヌクレオチドハンドルは酵素分子に補酵素を認識させる役割をもつ。
NADHは、酸化還元反応において水素の授受に関与する。最近では還元型ニコチンアミドアデニンジヌクレオチドreduced nicotinamide
adenine dinucleotideと呼ばれる方が多い。構造的にはNAD+とはリン酸基が付いただけの違いで、ともにデヒドロゲナーゼ(ピルビン酸からアセチルCoAを生成し、クエン酸回路に投入する働きをする酵素。逆反応を触媒する酵素はない)の補酵素となる。しかし、NAD+とは異なり、異化代謝ではなく、通常、脂肪酸合成や光合成のような同化代謝で利用される。補酵素の分子中には左の図のようにアデニンヌクレオチドAdenosine
diphosphate (ADP)を含むものが多い。アデニン、リボース、および二つのリン酸分子からなる化学物質、この部分は「ヌクレオチドハンドル」と呼ばれ、一般に補酵素の機能には関与しない。ヌクレオチドハンドルは酵素分子に補酵素を認識させる役割をもつ。ニコチンアミドアデニンジヌクレオチド(NAD+)は、燃料分子の酸化の際における主要な電子伝達体である。NAD+では、R=H で、NAD+の反応部位は、そのニコチンアミド環であり、これはビタミンの1つであるナイアシン(米国ではビタミンB3と呼ぶ)から生体内で合成されるピリジン誘導体である。基質の酸化においては、NAD+のニコチンアミド環が水素イオンと2個の電子受け取るが、これは水酸化イオンと等価である。この伝達体の還元型が、NADHと呼ばれる。一方、酸化型がNAD+と表されるように、窒素原子が正電荷を持つため、多くの反応で電子の受容体となっている。ニコチンアミドアデニンジヌクレオチドリン酸(NADP+)の方は、高エネルギー電子の重要な伝達体である。NADP+では、R=PO32-である。
NADPHは脂肪酸合成、コレステロール合成、光合成などに必須の補酵素であり、生体内での需要が多い。動物ではヘキソースリン酸側路hexose monophosphate shuntで大部分が合成される(hexose;六炭糖、monophosphate;リン酸塩、shunt;側路)。
植物の組織は、低酸素あるいは無酸素状態の環境にさらされることがある。酸素分子が利用できない、冠水あるいは水浸しになった土壌の植物の根は、酸素の拡散がかなり制限されるため、根の組織が低酸素状態になる。この嫌気的条件下では、酸化的リン酸化は機能しない。細胞内へのNAD+の供給が制限されるため、解糖の機能は停滞する。すると、一旦は、すべてのNAD+が還元状態のNADHになり、そのためグリセリンアルデヒド3-リン酸脱水酵素により反応が止まる。解糖が主なエネルギー源となる。解糖が機能するためには、解糖により生じたHをリサイクルするためには、サイトゾル内にある「発酵径路fermentation pathways 」がピルビン酸を還元しなければならない。嫌気条件下において、植物は主にピルビン酸を初期基質として用いる3つの経路、即ちアルコール発酵系・乳酸発酵系・アラニン合成系を働かせる。
アルコール発酵では、ピルビン酸デカルボキシラーゼ(PDC)による触媒でピルビン酸をアセトアルデヒドへ変換、その後、アルコール脱水素酵素(ADH)による触媒でアセトアルデヒドがエタノールに変換され、同時にNADHからのNAD+の再生が起こる。酸化的リン酸化の不活化で生じるNADH/NAD+サイクルを維持できるため、アルコール発酵の最も重要な役割としてこのNAD+の再生があげられる。
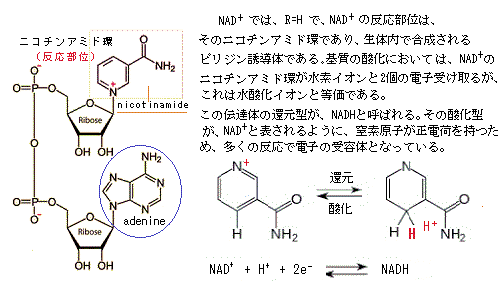 スクロースは、サイトゾルで常に合成される。葉で生産された光合成産物の殆どは、スクロースに変換され、分裂組織の、特に展開中の葉・根・花・果実・子実などの成長中の器官に転流される。
スクロースは、サイトゾルで常に合成される。葉で生産された光合成産物の殆どは、スクロースに変換され、分裂組織の、特に展開中の葉・根・花・果実・子実などの成長中の器官に転流される。葉のサイトゾルの中の濃度は、日中のトリオースリン酸triose phosphateと夜間の葉緑体から流出されるマルトースに由来する炭素分から、ソース葉以外の他の組織におけるエネルギー要求量と、多糖合成のためのソース葉のサイトゾルから送り出されるスクロースに由来する炭素分との差になる。trioseとは、三炭糖で、化学式 C3H6O3 生体内で解糖系の中間体として生成される。
光合成生物は、大気中の二酸化炭素を固定することにより生態系に有機炭素源を供給する。葉緑体をもつ植物や藻類は、固定された炭素をジヒドロキシアセトンリン酸やグリセルアルデヒド-3-リン酸などトリオースリン酸のかたちで葉緑体から細胞質へと運び出す。
実験におけるサイトゾルcytosolでは、ヘキソースリン酸から糖ヌクレオチドへの変換が、スクロース合成に先立って行われていることが明らかになった。
糖鎖は末端に単糖が付加され、その伸長によって形成される。糖鎖では、「糖転移酵素」が糖を次々に転移させることで糖鎖が形成されていく。このとき、付加反応に利用されるのは、そのままの単糖ではなく、ヌクレオチドと結合して活性化された糖供与体である糖ヌクレオチドが使われる。つまり、「糖転移酵素」は、糖ヌクレオチドを糖鎖の供与源として使っている。
生化学の様々な局面で、糖質の重要性が改めて明らかになり、糖鎖生物学glycobiologyと呼ばれる研究分野が新たに加わった。つまり、糖質の合成や構造、加えてタンパク質などや他の物質などと、どのように糖質が結合し認識されるかなどを研究する分野である。 新たなオミクスomics(生体中に存在する分子全体を網羅的に研究する学問領域)に、グリコミクスglycomicsが、ゲノミクスgenomicsやタンパク質proteinを研究するプロテオミクスproteomicsなどの研究に、新たな研究領域として加わった。グリコミクスでは、細胞が産出するすべての糖質やその関連分子、つまり、生物が持つ全ての糖の構造や機能を網羅する研究領域である。単独で存在している糖や、他の物質と複合体を形成している動的な糖も含まれるため、細胞相互間やその環境条件の変化の影響など、その研究領域は余りにも広い。
解糖系では、少量のエネルギーがATPとして得られ、還元力も還元型ニコチンアミドアデニンジヌクレオチドreduced nicotinamide adenine dinucleotide(NADH)として得られる。すべての生物種に存在するニコチンアミドアデニンジヌクレオチドnicotinamide adenine dinucleotide(NAD+)は、細胞内での酸化還元反応を触媒する多くの酵素と結合する補酵素である。NAD+はその酸化型であり、可逆的な2電子反応でNADHとなる。即ちNADHが電子供与体として働く、相対的に強い還元体として、解糖系やクエン酸回路の段階的な酸化の過程で生じた電子によってもたらせられる自由エネルギーを保存していることを示している。
陸上植物の葉緑体内での光合成の光化学系反応と炭素固定反応では、チラコイド膜では、光より光合成電子伝達系photosystem(PS)Ⅱ+PSⅠにおいてATPとNADPHが生産されるが、ストロマでは、大気CO2を炭水化合物のトリオースリン酸に取り込む一連の酵素反応からなるカルビンーベンソン回路によって、ATPとNADPHの両方が消費される。
酸化的リン酸化は、ミトコンドリアの内膜にある電子伝達系で起こる一連のリン酸化反応を呼ぶ。電子伝達系では、NADHやFADH2が酸化されて、電子と水素を失ってNAD+やFADとなる。その際に放出された電子は酸素と結合し、その酸素原子は還元されて水分子となる。
一方、マトリックス内に侵入したH+は濃度勾配を形成し、ATP合成酵素を通る。その際のエネルギーを利用してADPにリン酸を結合させ、ATPを効率的に生産する。
細胞内におけるミトコンドリアの重要な役割としては、エネルギー(アデノシン三リン酸;ATP)の産生である。それ以外にも、細胞内カルシウムイオン濃度の調節や脂質の酸化、また、細胞死や活性酸素種Reactive Oxygen Species(ROS)産生に関与し、自然免疫反応体として機能するなど、様々な重要な働きに関与していることが明らかになってきた。
活性酸素種は、人体におけるDNA・脂質・タンパク質や酵素などの生体高分子と反応し、その結果脂質過酸化やDNA変異、タンパク質の変性や酵素の失活の原因となる。この酸化ストレスの上昇が、分子レベルの生体酸化損傷を増加させ、様々な疾病や老化の亢進につながり、がんや糖尿病
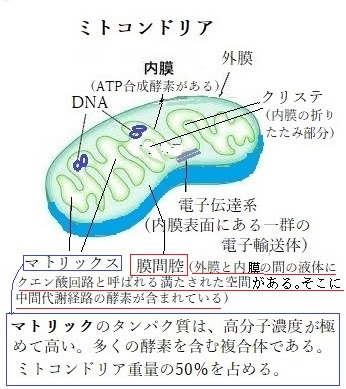 、高血圧といった生活習慣病をはじめとして数多くの疾病に深く関わっていると考えられている。その一方、活性酸素種は、シグナル伝達や免疫機構において重要な生理機能を担っている。このように、ミトコンドリアは細胞の営みにおいて、重要な役割を担う未知の領域も多く、更なる役割を解き明かすための研究が盛んに行われている。
、高血圧といった生活習慣病をはじめとして数多くの疾病に深く関わっていると考えられている。その一方、活性酸素種は、シグナル伝達や免疫機構において重要な生理機能を担っている。このように、ミトコンドリアは細胞の営みにおいて、重要な役割を担う未知の領域も多く、更なる役割を解き明かすための研究が盛んに行われている。クエン酸回路(Citric Acid Cycle)は、ミトコンドリアのマトリックスで行われる9段階からなる環状の代謝経路である。ただし、反応7ではミトコンドリア内膜に結合した酵素複合体が実行する。
グルコースからピルビン酸への解糖による嫌気的代謝では、グルコースから得られるはずのATPは、その一部しか取り出せない。植物におけるスクロースのピルビン酸への分解は、スクロースの持つ全エネルギーの25%以下程度しか放出できず、残りのエネルギーはピルビン酸に蓄えられたままである。
この代謝では、「反応8」での3-ホスホグリセリン酸からのリン酸基の転移と、「反応9」おける2-ホスホグリセリン酸の脱水により高エネルギーのエノールリン酸結合が起こりホスホエノールピルビン酸になる。
最終的には「反応10」で、高エネルギーのリン酸基がADPに転移しATPができると同時に、リン酸基が離れることでピルビン酸に変換される。
解糖での最終産物であるピルビン酸は、ミトコンドリア・マトリックス内に入り脱炭酸と補酵素A(CoA)との結合により、アセチル-CoAに変えられる。実は、ピルビン酸と脂肪酸の他に、アミノ酸の一部も細胞質からミトコンドリア・マトリックスに入り、アセチル-CoAか、クエン酸回路の中間体のどれかに変化する代謝が起きている。
真核細胞に共通するのは、エネルギーを獲得するための異化反応は、糖・脂肪・タンパク質のいずれから始まっているが、それぞれミトコンドリア・マトリックに集まって来ている。ミトコンドリアを持たない好気性細菌では、解糖やアセチルCoA生成、そしてクエン酸回路に類似した反応が細胞質で起きている。
基本の原理は、グルコースや脂肪などの燃料分子中の炭素がCO2に酸化され際に多量のギブズエネルギーが遊離され、その放出されたエネルギーがADPとPiを脱水結合されてエネルギーの通貨と呼ばれるATPが再生させる。脂肪がグルコースなどの糖質よりも効率の良い燃料源であるのも、脂肪中の炭素原子の方が、より還元されているためである。好気生物であれば、炭素の酸化における最終的な電子受容体はO2で、その酸化生成物はCO2である。炭素の還元レベルが高いほど、その酸化によって段階ごとに多量なギブズエネルギーが遊離されるようになる。
代謝で得られるATPの殆どは、グルコースの好気的代謝の過程から得られる。この過程は、グルコース誘導体を完全に酸化して二酸化炭素にすることから始まる。この酸化を行うのがクエン酸回路citric(sɪ́trɪk) acid cycleの一連の反応である。クエン酸回路では、糖質・脂肪酸・アミノ酸などの燃料分子を酸化する最終的な共通径路で、実体は細胞内における生化学的環状径路で、その大部分の炭素燃料はアセチルCoA(acetyl coenzyme A)の形となってクエン酸回路に入ることが多い。そこでCO2に酸化すると同時にNADHの形で蓄えられる高エネルギー電子となり、CO2は廃棄物して排出される。NADHの高エネルギー電子は、ミトコンドリア内膜にある電子伝達系に渡され、最後はO2と結合してH2Oとなる。
ミトコンドリア・マトリックスで起こるクエン酸回路自体がO2を使うのではなく、回路の進行にO2が必要なのである。電子伝達系がO2を最終受容体に用いてNADHから電子を取り除き、サイクルを回し続けるのに必要なNAD+を再生するからである。
生命体は35億年前には存在していた。しかしながら、地球大気のO2が豊富になったのは、10億年前~20億年前の間であるから、クエン酸回路によるエネルギー生成反応の起源は比較的新しい。
酸素は地球上の化学物質の中で、特に安定しない物質で、化学反応を起こしやすい。生物はこうした酸素を、呼吸という代謝で体の中に取り込み、その化学反応によりエネルギーを獲得する。
「好気性生物」とは、酸素を必要とする好気呼吸という代謝機構を備えた生物のことで、細胞の呼吸では、「好気性菌」は、例えば糖や脂質のような基質を酸化してエネルギーを得るために、酸素を利用する。
殆どすべての動物、菌類、そしていくつかの細菌は「偏性好気性生物」である。偏性好気性生物は、好気的な細胞呼吸に依存し生存するために酸素は欠かせない。
30億年以上前に、原核生物の光合成反応系が進化し、生物は漸く既存の有機化合物に頼ることなく、自前でCO2ガスから必要な有機分子を作れるようになった。その光合成を行う間に、水を分解しO2を発生させる細菌が現れた。それでも、大気中に酸素が十分な濃度となって行き渡るのに、10億年ほどの年数が必要であった。
古代の海洋中の溶存酸素が、既に大量に海水に溶け込んだ2価の鉄イオン(Fe2+)を酸化し尽して、初めて酸素が大気中を満たし始めるようになる。その大気の酸素濃度が上昇するにつれ、光合成を行わない好気性の生物が登場し、大気中に酸素濃度が漸く一定に保たれるほどに向上する。 大気中の酸素が安定して使えるようになると、好気的代謝によりATPを合成する細菌が登場する。このような原核生物は、糖などに還元された有機分子を、CO2とH2Oにまで酸化する過程を経て完全に分解し、その際に発生する多量のエネルギーを利用した。
光合成の副産物として有機化合物が蓄積されると、大腸菌の祖先を含む一部の光合成細菌が光エネルギーに依存する能力を失い、細胞呼吸のみに依存するようになる。このような好気性細菌を、原始時代の真核細胞が取り込んだことによりミトコンドリアが生じた。その後間もなく、初期の好気性真核生物が光合成細菌を捕獲した。これが葉緑体の前身である。真核生物が、やがてミトコンドリアや葉緑体に進化する細菌共生体を獲得したことにより、進化が加速し遂には、豊富な動的能力を持つ複雑な多細胞生物を誕生させていった。
好気性細菌は地球上に藍藻類が誕生し、大気中に酸素が増加してきたことによって誕生したとも考えられている。ある種の好気性細菌はミトコンドリアの祖先ともいわれている。
一方では、酸素を好まない生物もいる。「嫌気性菌」とは生育に酸素を必要としない細菌を呼ぶ。嫌気性菌には、酸素存在下でも生育できる「通性嫌気性菌」と、大気レベルの濃度の酸素に晒されれば死滅してしまう「偏性嫌気性菌」に分けられる。
「嫌気性菌」は、発酵または嫌気呼吸という代謝系で生育に必要なエネルギーを獲得する。「通性嫌気性菌」は、酸素の有無に関わらず発酵または嫌気呼吸でエネルギーを獲得するが、酸素の存在下では好気呼吸でエネルギーを獲得する。腸内フローラ(腸内細菌叢)を構成する主な腸内細菌であるビフィズス菌Bifidobacterium、バクテロイデス、ユーバクテリウム、クロストリジウムなどは「偏性嫌気性菌」で、大気の酸素に晒されれば死滅する。乳酸桿菌、大腸菌、腸球菌などは「通性嫌気性菌」である。
善玉菌の代表格であるビフィズス菌と乳酸菌は、混同されがちであるが別物、乳酸菌は比較的酸素に強いため、酸素がある程度残っている環境でも生育は可能である。一方、ビフィズス菌は、酸素がある環境では死滅するため消化管の最も奥に潜み、酸素が殆どない大腸に局在している。また、ビフィズス菌も乳酸菌も、乳酸を産生するが、ビフィズス菌はそれに加えて殺菌・抗炎症作用があるとされる酢酸を産生する。酢酸は短鎖脂肪酸の一種で、酢酸や乳酸は大腸を活発にし、大腸の健康を保ち、病気を予防するとされている。
嫌気性生物とは、増殖に酸素を必要としない生物のことで、殆どの嫌気性生物は細菌である。代表的なものは、嫌気性バクテリアとよばれるもので、地中や海中など酸素のない場所に生息している。人の腸の中に生息するビフィズス菌も嫌気性の菌になる。また、いくつかの嫌気性細菌は、人を含む高等生物に対して極めて危険な毒素、例えば破傷風毒素やボツリヌス毒素(神経症状を呈するボツリヌス症を起こす)などを産生する。
嫌気性生物はその生息過程で酸素を必要としないため、急激な活動はできないが、有機物を分解し、物質の浄化に役立っている。 地球上では好気性と嫌気性の生物が共存して、環境バランスを整えている。
ミトコンドリアmitochondria(複数形)は、殆どの真核細胞にあって、細胞質にある細胞小器官の中でも最も目立つものの1つである。ミトコンドリアは、細胞に必要な化学エネルギーを作り出す。ミトコンドリアは、糖などの食物分子の酸化で得られたエネルギーを利用して、アデノシン三リン酸(ATP)を作る。ATPは、細胞が活動する動力源となる化学燃料で、ミトコンドリアが働くと酸素を消費し二酸化炭素を放出するので、この細胞反応を細胞呼吸と言う。
ミトコンドリアがなければ、動物や植物、菌類も酸素を利用して栄養源となる食物分子から、必要なエネルギーを取り出すことができない。ミトコンドリア自体、独自のDNAを持ち、二分裂で増えることから細菌と同じでと見られている。つまりミトコンドリアは、現在の真核細胞の祖先細胞が飲み込んだ細菌であった。飲み込まれたミトコンドリアと共生関係が生まれ、宿主である真核生物と飲み込んだ細胞は互いに共生し現在に至った。
地球上には、太陽光エネルギーのたかだか1%を集めて化学エネルギーに変換できる生物が存在している。緑色植物が最も目立つが、このエネルギーの変換の60%は、藻類や細菌が行っている。生化学を研究する限り出合う様々なエネルギー変換すべての中で、このエネルギー変換が最も重要で、これが無ければ、現在、地球上で見られる生命は存在していないだろう。
生物の外形に関わらず、体内の物質は常に入れ替わっている。その生体内で起こる物質の合成や分解などの化学反応を代謝と言う。屈性と傾性などの環境変化に応じる運動以外にも生体物質の合成にも、たくさんのエネルギーが必要である。代謝に伴うエネルギーの受け渡しには、ATP という物質が重要な役割を果す。
生物は、環境から物質とエネルギーを取り込み、必要な物質の合成と不要になった物質の分解を繰り返し、物質レベルや細胞レベルで常に体を更新している。生体内での物質の合成反応を同化、分解反応を異化という。生体内でのこれらの化学反応をまとめて代謝という。同化は反応にエネルギーを必要とする吸熱反応で、異化は反応にエネルギーを放出する発熱反応である。
すべての生物は生命活動に必要なエネルギーを、細胞内で有機物を分解する異化反応で得ており、この働きが呼吸である。肺における酸素と二酸化炭素の交換は外呼吸とも呼ばれる。有機物に蓄積されたエネルギーの元をたどれば、太陽の光エネルギーに行き着く。植物は光エネルギーを化学エネルギーに変えて、空気中の二酸化炭素と土中の水から有機物を合成する。光合成とは、光エネルギーを有機物のエネルギーに変換する同化反応でもある。
呼吸による有機物の分解で放出されるエネルギーは、生命活動に直接利用することはできない。呼吸で放出されたエネルギーは、一時的にATPという物質に蓄えられる。全ての生物が共通に用いるATPは、そのエネルギーが、分子の合成・タンパク質の合成・細胞内物質の移送・運動などの様々な生命活動に使われるので、エネルギー通貨と呼ばれる。
ATPは、アデノシンという物質にリン酸が3つ結合したアデノシン三リン酸の略称で、リン酸同士の結合は、高エネルギーリン酸結合High‐energy phosphate bondと呼ばれる。呼吸により有機物から放出されたエネルギーでADP(アデノシン二リン酸)とリン酸が結合してATPが合成される。ATPがADPとリン酸に分解されるとき、比較的大きなエネルギーが放出され、このエネルギーを用いて生命活動が営まれている。ATPが分解されるときに放出されるエネルギーは、生命活動を支 える反応を起こさせるのには過不足のない大きさで、再合成も容易である。ヒトは1日に 体重に近い量のATPを消費する。ATPは細胞内でADPとリン酸に分解されると、呼吸で放出されたエネルギーを用いて直ちに再合成され、これが繰り返されているのである。
脂肪は他の有機物と比べて、同じ重さで蓄えられるエネルギー量が格段に大きいので、ある程度の期間エネルギーをコンパクトに貯蔵するのには向いている。過剰に摂取された炭水化物は代謝により脂肪に変換されて貯蔵される。
炭水化物は糖質とも呼ばれ、グルコースglucose (ブドウ糖とも呼ばれる) は呼吸の材料としてよく使われる。
細胞は、エネルギーと還元力を環境から取り出し、高分子の構成要素を合成し、さらに巨大な高分子を作り上げている。これらの過程は、高度に統合された化学反応のネットワークによって成し遂げられる。その全体を代謝metabolismあるいは中間代謝intermediary metabolismと呼んでいる。
ミトコンドリアmitochondria(複数形)は、殆どの真核細胞にあって、細胞質にある細胞小器官の中でも最も目立つものの1つである。ミトコンドリアは、細胞に必要な化学エネルギーを作り出す。ミトコンドリアは、糖などの食物分子の酸化で得られたエネルギーを利用して、アデノシン三リン酸(ATP)を作る。ATPは、細胞が活動する動力源となる化学燃料で、ミトコンドリアが働くと酸素を消費し二酸化炭素を放出するので、この細胞反応を細胞呼吸と言う。
殆どの原核生物は単細胞生物だが、鎖や集合体などの構造を持った多細胞体もある。原核生物は形や構造が簡単で自ずと制約が多いが、化学作用の面では、各種細胞の中でも際立って多様な創意に満ちている。
古細菌に分類されている、熱い火口付近の超好熱菌や、高塩濃度など極限環境下で生育する高度好塩菌、特に、牛の反芻胃や数は少ないものの人の結腸などにも存在するメタン菌は、偏性嫌気性菌とはいえ、他の菌と共生あるいは基質の競合の中に生育し、二酸化炭素を始め、様々な炭素化合物からメタンを作る。これをメタン発酵と言う。メタン菌は、酸素に敏感な菌で、過酸化水素(化学式H2O2)を水と酸素に分解する酵素カタラーゼを欠いているため、細胞内に酸素が入ると細胞毒性がある過酸化水素が蓄積し、細胞構造が破壊されてしまう。 太 陽光が届かない深海で、硫黄の酸化還元サイクルで生命が維持されている硫酸塩還元菌をはじめ、他の生物の細胞の中など、ある意味では広大な領域に生息する原核生物の数は、地球上の真核生物全体より圧倒的に多い。真核細胞でエネルギーを作る細胞小器官のミトコンドリアは、現在の真核生物の祖先の細胞の内部に取り込まれた好気性細菌シアノバクテリアの祖先が進化したと見られている。
ミトコンドリアがなければ、動物や植物、菌類も酸素を利用して栄養源となる食物分子から、必要なエネルギーを取り出すことができない。ミトコンドリア自体、独自のDNAを持ち、二分裂で増えることから細菌と同じと見られている。つまりミトコンドリアは、現在の真核細胞の祖先細胞が飲み込んだ細菌であった。飲み込まれたミトコンドリアと共生関係が生まれ、宿主である真核生物と飲み込んだ細胞は互いに共生し現在に至った。
単離されたミトコンドリアの大きさや形は、その祖先細胞に似通っている。ミトコンドリアは、あくまでも細胞小器官であるため、独立して生存はできないが、独自性と適応性が非常に高く、形態や数は様々な細胞の役割に適合して変異している。しかも、配置なども変化させている。例えば、心筋細胞内のミトコンドリアは、収縮装置の近傍に配置され、精子では尾部の鞭毛の一部に局在して巻きついて、エネルギー消費が非常に高い部位に、直接ATPを供給している。その一方で酵母の細胞では、ミトコンドリアは融合して、ぴったり付着した細胞膜から伸びた管からなる細胞質全体に広がる網目構造を作ると言った特異性がある。
ミトコンドリアの数は、非常に多く、1つの肝細胞に1,000~2,000個もある。その数は細胞の種類によって異なり、細胞のエネルギーの必要量で応じて変化している。例えば、筋肉が収縮刺激を繰り返し受けると、骨格筋細胞のミトコンドリアは分裂を繰り返し、5~10 倍に増大することもある。
目次へ