| 元素の周期表 | ||||||||||||||||||
DNA DNAが遺伝物質 生物進化と光合成 葉緑素とATP 植物の葉の機能 植物の色素 葉緑体と光合成 花粉の形成と受精 ブドウ糖とデンプン 植物の運動力 光合成と光阻害 チラコイド反応 植物のエネルギー生産 ストロマ反応 植物の窒素化合物 屈性と傾性(偏差成長) タンパク質 遺伝子が作るタンパク質 遺伝子の発現(1) 遺伝子の発現(2) 遺伝子発現の仕組み リボソーム コルチゾール 生物個体の発生 染色体と遺伝 減数分裂と受精 対立遺伝子と点変異 疾患とSNP 癌変異の集積 癌細胞の転移 大腸癌 細胞の生命化学 イオン結合 酸と塩基 細胞内の炭素化合物 細胞の中の単量体 糖(sugar) 糖の機能 脂肪酸 生物エネルギー 細胞内の巨大分子 化学結合エネルギー 植物の生活環 シグナル伝達 キク科植物 陸上植物の誕生 植物の進化史 植物の水収支 拡散と浸透 細胞壁と膜の特性 種子植物 馴化と適応 根による水吸収 稲・生命体 胞子体の発生 花粉の形成 雌ずい群 花粉管の先端成長 自殖と他殖 フキノトウ アポミクシス 生物間相互作用 バラ科 ナシ属 蜜蜂 ブドウ科 イネ科植物 細胞化学 ファンデルワールス力 タンパク質の生化学 呼吸鎖 生命の起源 量子化学 ニールス・ボーアとアインシュタイン 元素の周期表 |
||||||||||||||||||
|
||||||||||||||||||
1)常温常圧において、元素は、単体でどのような状態、つまり、固体・液体・気体なのか?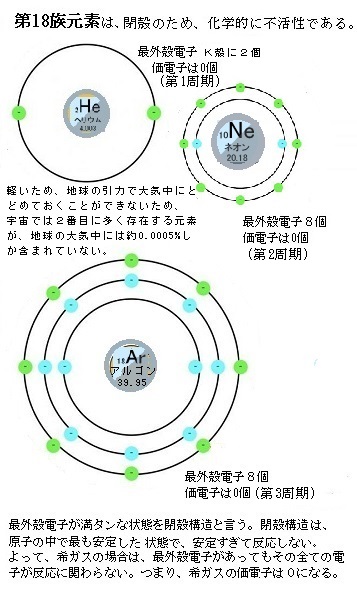 気体は、水素H2、窒素N2、酸素O2、フッ素F2、塩素Cl2、希ガスrare gas(第18族元素すべて、ヘリウム・ネオン・アルゴン・クリプトン・キセノン・ラドン・オガネソンの7個)の合計12個。 第18族元素は、原子における最外殻電子に含まれる電子の数が8(ヘリウムのK殻のみ2)であるもの、つまり閉殻closed shellとなっているため、化学的に非常に不活性であり、しばしば単原子分子として存在する。 かつて第18族元素には化合物が知られていなかったために、化学反応を起こさないという意味で不活性ガスinert gas類と呼ばれた。 また、化学的な不活性さの度合いは、第1周期元素のヘリウムを筆頭として、周期が進むにつれて弱くなる。 安定核種が存在する最後の周期である第5周期のキセノンに化合物が見つかったことを皮切りに、現在では他の第18族元素にも化合物が見つかっており、完全に不活性というわけではない。 ヘリウムを除いて、常圧かつ凝固点以下で弱いファンデルワールス結合による結晶を形成する。 18族元素を希ガスと言う「希」は「まれ」という意味で、アルゴンを除いてその存在量は少なく、室温で気体であることより希ガスと呼ばれるようになった。 |
||||||||||||||||||
ヘリウムは気球などに、ネオンはネオンランプなどに用いられている。 アルゴンargonは、レアーガスの一種に数えられるが、窒素、酸素に次ぎ大気中に3番目に多く含まれる気体である。しかし、その比率はわずかに約0.93%程度でしかない。 アルゴという名はギリシャ語で「怠惰な」「不活発な」を意味する「αργον」という単語に由来するように、他の物質と反応しない不活性な物性を持っている。 この物性を活かす、代表的なアルゴンの用途に溶接がある。 電気の力を使って金属同士を溶接する際に、電極間に電位差が生じることにより起こる、電極間の電弧(Arc)状の閃光を「アーク」と言う。 負極・正極間の気体分子が電離しイオン化が起こり、プラズマを生み出し、その中を電流が流れる。 通常は、伝導性のない気体中が励起状態になり高温と閃光を発する。 そのアークを熱源として利用する溶接方法が「アーク溶接」である。空気の成分は約80%の窒素ガスと約20%の酸素ガスである。 それらのガスと溶融金属が反応しないように、シールドshielded(遮断)用のガスとして、アルゴンが使われる。 外販用アルゴンの最大のユーザーは、半導体を構成する部品素材となるシリコンウェハーの製造現場で、金属シリコンを溶融し、純度99.999999999%(イレブンナイン)という超高純度の単結晶シリコンを作る際の雰囲気ガスとしてアルゴンが使われている。 アルゴンの不活性な雰囲気の中で、品質の高いシリコンウェハーが製造されている。シリコンウエハーの形状は極めて薄い円盤状をなし、その表面が厳密に平滑であることが、高い性能を保証する。 半導体とはシリコンのこと、半導体や太陽電池に使われるシリコンSiliconとシリコーンSiliconeとは別のもの、シリコンはケイ素(Si)のこと、シリコーンはケイ素をもとに作り出された人工の化合物である。  大気中ではない、地球の岩石や土壌の主成分として、酸素の次に多い元素がケイ素、そのケイ素は、単体では自然界には存在せず、酸素と結びついてケイ石silica
stone(ケイ素・酸素・水素の化合物の総称)として存在している。 大気中ではない、地球の岩石や土壌の主成分として、酸素の次に多い元素がケイ素、そのケイ素は、単体では自然界には存在せず、酸素と結びついてケイ石silica
stone(ケイ素・酸素・水素の化合物の総称)として存在している。石英(クオーツ)とは二酸化珪素SiO2の鉱石、水晶とは石英の一種、一般的には石英のうち、透明で結晶の形をしているものを水晶と言うが、透明でなくとも不透明でも水晶、中でも、無色透明で六角柱状の美しく結晶した天然水晶を、特に『クリスタル』と呼ぶ事が多い。 ケイ素という栄養素は、食生活では野菜などの根菜類・穀物などに含まれている。 人体は、これらから土の成分であるケイ素を栄養素として吸収し体内へ入れる。 カルシウムよりも、むしろケイ素の方が、骨の成長維持にとって大きな役割を担っている。 血管の主成分であるケイ素が不足すると、動脈硬化をさらに進行させる。 ケイ石を木炭などと一緒に電気炉で融解、還元する、複雑な化学反応を加えて非金属ケイ素を抜き出し、それから無機と有機の性質を兼ね備える合成樹脂を作る。それが「シリコーン」である。 その結合の主骨格がケイ素と酸素が交互に結びついたシロキサン結合(Si-O-Si)である。 その側鎖に有機基が結びついて、高温や低温の両方に強くなり、耐光性・電気絶縁性・撥水性・離型性など、様々な物性を発揮する。 「シリコーン」は、エレクトロニクスから輸送機、化学・繊維・食品・化粧品、そして建築などあらゆる分野で活用されている。 オガネソンは、超ウラン元素であり、天然界には存在しない。人工元素artificial elementのため、まだまだ不明な特性が多い。 最も重い元素、かつ最も重い同位体を含む元素である。特殊な実験でしか合成できないため、物理特性のほとんどは理論計算に基づく推定である。 希ガスと言うからには、実際初期の予測では気体と推定されていた。だが現在の予測では沸点は47℃~107℃と推定され、希ガスが液体でいる温度範囲は2~9℃と非常に狭い、しかも常温常圧では、比重4.9~5.1の固体であると推定されている。 液体は、臭素Brと水銀Hgの2個、その液体元素と気体元素以外の元素は、全部が固体である。 目次へ |
||||||||||||||||||
 |
||||||||||||||||||
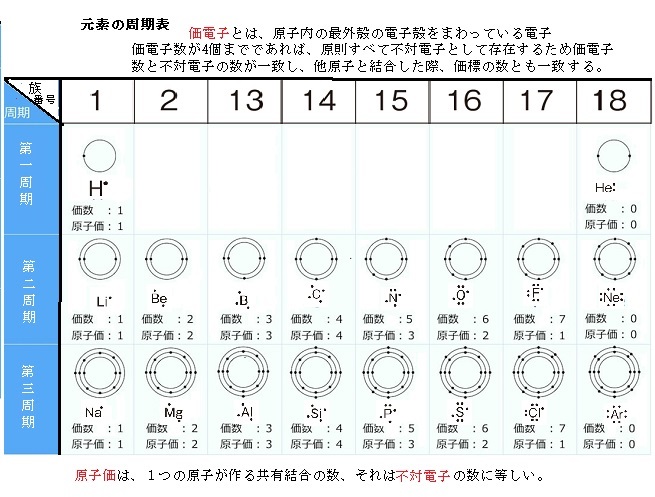
2)なぜ、元素の並び方に周期が存在するのか?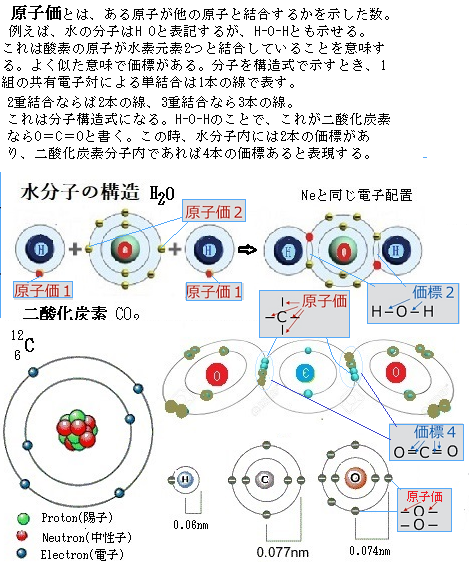 元素の周期表を考案したロシアの科学者メンデレーエフは、夢の中で元素の並び方を思いついたと言う。 原子量の小さい元素から順に左から右へ配置し、しかも同じ原子価valence(ある原子の電子が、何個の他の原子の電子と結合できるかを示す数)を持つ元素を上下に、何段にも重ねて並べた。 原子価は元素によって決まっている。 原子価1の元素は、水素・フッ素・塩素、原子価2の元素は酸素、原子価3の元素は窒素、原子価4の元素は炭素となる。 原子価は、不対電子unpaired electronの数に等しい。 原子中の価電子は、2個で対になったときに安定する。 このように2個の価電子が対になったものを電子対electron pair、対にならずに単独で存在する価電子を不対電子と言う。 価電子とは、最外殻にある電子の数で、原子がイオンになったり、他の原子と結合したりするのに使われる電子のことを言う。 通常、最外殻電子は反応に使われるので、殆どの場合は最外殻電子=価電子となる。 炭素の場合は、最外殻電子数と原子価数も同じく4個である。 |
||||||||||||||||||
 フッ素Fの場合では、最外殻電子が7個あり、電子対が3組と不対電子が1つであるため、各原子が不対電子を1個ずつ出し合って共有結合する。フッ素分子F2となる。 分子の電子式(元素記号の周囲に、最外殻電子を点・で表した式)に含まれる電子対のうち、2つの原子が電子を1コずつ出し合うことで形成される電子対を共有電子対、1つの原子が持つ電子のみで形成される電子対を非共有電子対と言う。 なぜ不対電子を出し合う必要があるかというと、原子のままだと最外殻電子が7個で不安定であるため、あと電子が1個あれば、電子的に安定な希ガス元素のネオンNeと同じ電子配置、つまりオクテットoctet(八つ一組)となり安定する。 そのため、フッ素原子同士で不対電子を出し合い共有する。 炭素と結合して有機分子を構成する窒素、酸素、あるいは原子価1個のハロゲンhalogen(第17族元素)も最外殻が 8 電子で満たされた状態が安定する。 これをオクテット則Octet rule(8 電子則)と呼び、有機化合物の成り立ちを考える上でも最も基本的な規則である。 なお第17族元素は、いずれも生体毒性が大きい。特に臭素とヨウ素は極めて揮発性が強く、化合物にも揮発性のものが多い。しかも化学的な反応性は非常に高い。 |
||||||||||||||||||
 ハロゲンを含む化合物はハロゲン化物と呼ばれる。その中のアスタチンastatineは人工元素であり、1947年、ギリシア語のastatos(不安定の意)にちなんで命名された。 十数種類の同位体が人工的に作られているが、すべて放射性があり短寿命のものが多い。 常温で固体、化学的性質はヨウ素に類似している。やがて、第16族元素の原子番号84のポロニウムpoloniumのβ崩壊(β崩壊は原子核中の中性子が陽子、電子および反ニュートリノに転換し、陽子だけが原子核内にとどまり、電子と反ニュートリノとが原子核外に放出される現象)により天然にわずかに存在することが知られた。 原子価とは、注目した原子から出ている価標(棒線)の本数のことである。 価電子は最外殻に存在する電子の数のことであるから、価電子数が4個までであれば、原則すべて不対電子として存在するため価電子数と不対電子の数が一致し、他原子と結合した際、価標の数とも一致する。 例えば、炭素の価電子数が4つなので、すべて不対電子となる。 メタンCH4の場合、炭素の不対電子4つと水素4個の価電子とそれぞれ4本の共有結合し、炭素原子Cからは、価標(棒線)が4本出ている。 カルシウムも、最外殻電子数2個でそれが価電子数となる。 最外殻に存在する電子の数、原子価とは、注目した原子から出ている価標(棒線)の本数、価電子数が4個までであれば、原則すべて不対電子として存在するため価電子数と不対電子の数が一致し、他原子と結合した際、価標の数とも一致する。 基本的に不対電子だけが共有結合などに関与し、電子2個が対になっている、他の元素と共有されていないものを非共有電子対と呼ぶ。 アンモニアNH3の窒素原子では、電子がペアとなっておらずに各辺で一つになっている部分がある。この対になっていない2つの電子のことを不対電子と呼ぶ。 |
||||||||||||||||||
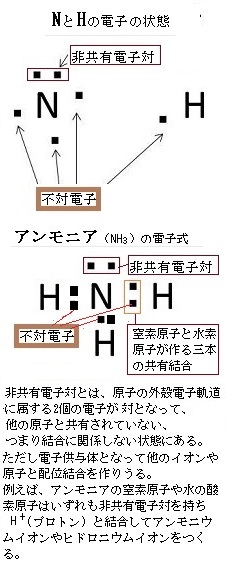 例えば、価電子数が5個以上であれば、不対電子以外に非共有電子対unshared electron pairが表れるため、価電子数と不対電子の数が一致しなくなる。 そのため、窒素の価電子数5つ、そのうち3つが不対電子となるアンモニアNH3の場合、不対電子3つと3個の水素が共有結合し、3本の共有結合が生じる。 窒素原子Nからは、価標(棒線)が3本出ている。窒素分子N2の場合も、三重結合となり、同様に窒素原子Nからは、価標(棒線)が3本出ている。 よって、Nの原子価は3、価電子数5とは一致しない。 目次へ |
||||||||||||||||||
3)元素の周期律の意味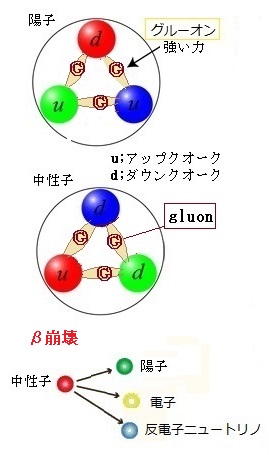 原子番号は、原子に含まれる陽子の数であり、周期表の元素は、その原子番号の順番で並んでいる。 原子番号は、原子に含まれる陽子の数であり、周期表の元素は、その原子番号の順番で並んでいる。「周期period」は原子の電子殻 electron shellの数によって分類され、陽子が一つずつ増えるにつれ、原子番号が大きくなり、それにつれて原子の質量も大きくなる。 元素を原子番号の順に並べると元素の化学的性質が一定の周期ごとに変わっていく周期律periodic lawが見られる。つまり、最外殻電子の価電子が増え、周期表の横列の周期が上位にあがり、それが縦列の「族」に共通する原子価が並び、化学的性質を共有する元素となり、それらが重層的に重なるという法則である。 最外殻の種類が同じ元素を横列にする第1周期(K殻)、第2周期(L殻)、…同周期であれば最外殻の種類は同じとなる。 陽子が一つずつ増えていくに従って、価電子の数も増えていく。価電子とは、原子内の最外殻の電子殻をまわっている電子のことである。原子価電子(げんしかでんし)とも言う。 ただし、最外殻電子がちょうどその電子殻の最大収容数の場合、または最外殻電子が8個の場合、価電子の数は0とする。つまり、第18族元素のネオンNeのK殻2個、L殻8個であるが、「価電子」8ではなく、L殻は8個で閉殻して安定しているので「価電子」とは言わず、ネオンの「価電子」の数は0となる。 第18族元素のヘリウム(K殻2個)・ネオン・アルゴン・クリプトン・キセノン・ラドンの6元素は地球の大気中に、ごくわずかながら単原子分子の気体として存在しているので、これらの元素を希ガスと呼ぶ。 「価電子」とは、最外殻にあって元素の性質と深い関わりがある電子のことで、価電子の数が周期的に変化すると、それにつれて元素の性質も周期的に変化する。つまり、原子が化合物や結晶等を構成する際に、それらの化学結合や物性は、その原子内の核外電子が深く関わってくる。 原子内の電子軌道を回る電子には、化学結合や物性に深く関わるものと、ほとんど関係しないものがある。 化学結合や物性に関わる価電子は、原子内の最外殻など外側を回っている。逆に、原子核に近い軌道にある電子(内殻電子)は、例外も存在するが、通常の物性や化学結合に寄与することはほとんどない。 これを「元素の周期律」と言う。元素の周期律に基づいて、化学的性質が似てくる原子価が同一の元素を同じ縦の列に並ぶように配列したのが、周期表と呼ぶ。 このことから、元素が周期表のどの位置にあるかによって、元素のおおよその性質を推定することができる。 目次へ |
||||||||||||||||||
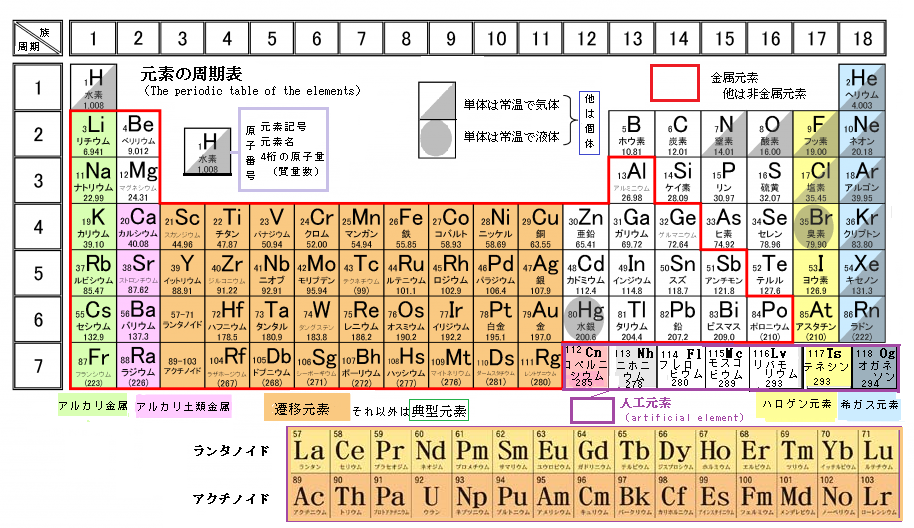
| 4)元素の分類 周期表が色分けされているのは、金属元素か非金属元素か、という分類、金属には、金属光沢と呼ばれる独特の輝きがあること、電気を通すことなどの性質がある。この周期表で赤い枠で示されているように、かなり多くの元素が含まれている。しかし、B(ホウ素)・Si(ケイ素)・Ge(ゲルマニウム)などの半金属元素は、金属元素と非金属元素の中間的な性質を持ってる。ケイ素は周期表では非金属に分類されいるが、光沢があり、まるで金属のように見える。 半導体と呼ばれているもの、その半導体の性質を実験で確かめる際には、ケイ素でできたシリコンウェハーを使う。電子オルゴールの電極を、クギなどの、電気を通すものに繋ぐと音楽が鳴る。消しゴムのように電気を通さない物体につないでも音楽は鳴らない。この電子オルゴールをシリコンウェハーにつないでみても、音は鳴らない。シリコンウェハー、ケイ素はこの状態では電気を通さない、つまり非金属。 シリコンウェハーにガスバーナーで熱を加え高温になった状態で電子オルゴールを繋ぐと、電子オルゴールが鳴る。このように、シリコンウェハーは温度が上がった状態で電気を通すと、金属の性質を示す。これは、加熱したことで、電子が移動できるようになったためである。このように物質は、電子を通す「導体」と電子を通さない「絶縁体」、そしてある条件によって電子を通す「半導体」に分かれる。 半導体の最大の特徴は、温度の変化や光の照射、不純物の添加により電気抵抗率が大きく変化することにある。この性質を利用して、電流を一方向にのみ流すダイオードや、電気信号を増幅したり電気信号の流れを高速でON/OFFにしたりするトランジスタなどの電子部品が作られている。現在ではパソコンはもちろん、携帯電話などの情報端末から家電製品、自動車、クレジットカード、電子マネーに至るまで、あらゆる分野で半導体が使われている。 SiやGeなどの物質では最外殻の電子の数は4であり、隣の原子とそれらの電子を共有結合することによって、ダイヤモンド構造の結晶を作る。半導体の材料としてゲルマニウムは、主役の座を降りたかに見えたが、近年、シリコントランジスタの高速化の限界が顕在化するにつれてゲルマニウムの高電子移動度が着目され、再び脚光を浴びつつある。 B(ホウ素Boron)は、硬くて脆い黒色の固体元素で、同じ第13族元素であるアルミニウムなどよりも第14族元素である炭素やケイ素に類似した性質を示す。結晶性ホウ素は化学的に不活性であり耐酸性が高く、フッ化水素酸にも侵されない。フッ化水素酸はその強い洗浄力により広く使用されている。その化学熱傷による皮膚症状は、骨破壊など重篤化することもある。 Bは、皮膚・目・粘膜などに激しいやけどを引き起こす。単体としての用途はあまりないが、ホウ素をガラスに混ぜると、ガラスの熱による伸び縮みが約1/3に減る性質を利用して、ホウ素を混ぜたガラスが耐火ガラス(パイレックス)となる。ホウ素の金属化合物、TiB2・ZrB3・CrB2 などは高温に耐える素材として、ロケットエンジンのノズルやジェットエンジンのタービンなどに使用されている。MgB2 は次世代の超伝導体として研究が進められている。ホウ酸(H3BO3)を水に溶かしたホウ酸水は、弱酸性の消毒液、目薬に使用されている。 周期表の横の行を「周期=横のグループ」といい、縦の列を「族group=縦のグループ」とい言い「化学的特性」、つまり「原子価」が同一の元素を縦に並べる。その同じ族に属する元素を「同族元素」と言う。さらに、同族元素の3から11族を「遷移元素」といい、遷移元素以外の、1、2族と12から18族を「典型元素」と言う。典型元素では、同じ族の価電子の数が等しく、互いに良く似た性質を示す。 「遷移元素」の性質は、その化合物の色が有色であることが多い、化学的反応性は、横(同周期)で似ている。「典型元素」の性質は、化合物の色は無色が多い、化学的反応性は、縦(同族)で似ている。 1族の「典型元素」リチウム、ナトリウム、カリウムなどのアルカリ金属が、その一例である。リチウム・ナトリウム・カリウムの3つの金属を小さく切り、それぞれ水の入った試験管に入れてみる。リチウムは、水と反応して気体が発生する。ナトリウムは水と激しく反応し、やはり気体が発生する。カリウムの反応はさらに激しく、炎を出して燃える。 このとき発生した気体は、一体何なのか。試験管の口に火を近付けると、リチウムとナトリウムは、「ポン」という音を出して燃える。このことから、発生したのが水素だと分かる。しかし、カリウムでは反応がない。実は、カリウムも水と反応して水素が発生するが、発生するとすぐに燃えてしまう。 反応した後の液体にフェノールフタレイン溶液を加えると、どれも赤い色になる。アルカリ金属と水が反応して、水溶液がアルカリ性になったことを示す。アルカリ金属と呼ばれるのは、このためである。 1族のアルカリ金属が他の元素と反応しやすいのは、一番外側の電子殻にある価電子と関係がある。価電子が一つ、それを他の元素に渡すだけだから化学反応が起きやすい。逆に安定しているのは、18族の希ガスである。この第18族元素の希ガスは、最外殻電子8個と閉殻しているから、価電子と原子価が全て0で安定し、他の元素と反応しにくい。 希ガスよりも外側の電子が一つ少ないのが、17族の「ハロゲン」。ハロゲンのフッ素、塩素、臭素などは、金属と反応して「塩」を生成するという性質がある。例えば塩素とナトリウムが反応すれば、塩化ナトリウム、つまり食塩ができる。 17族ハロゲン元素、塩素・臭素・ヨウ素などの同族元素は性質が似ている。ヨウ素の単体は、常温では固体である。 試験管の中に小さじ1杯のさらし粉を入れて、濃塩酸を1滴たらす。すると、煙のような気体が発生し、発生したのが塩素で、塩素の単体は常温で気体である。塩素とヨウ素の間に位置する臭素の単体は、常温では液体で、暗赤色である。この常温での状態は、それぞれの物質の沸点と融点に関係する。塩素とヨウ素の間にある臭素は、沸点も融点も2つの物質の中間の温度になっている。 3本の試験管に塩化カリウム水溶液・臭化カリウム水溶液・ヨウ化カリウム水溶液を用意し、それぞれに硝酸銀水溶液を加えていく。硝酸銀水溶液を塩化カリウム水溶液に加えると、白い沈殿が生じる。次に、ヨウ化カリウム水溶液に硝酸銀水溶液を加えると、これも白い沈殿が生じる。 塩素、ヨウ素、どちらの物質でも沈殿が生じた。臭素でも、臭化カリウム水溶液に硝酸銀水溶液を加えると、他の2つと同様に白い沈殿が生じる。気体、液体、固体と順に並んで、沸点も融点も順に温度が上がっていく。硝酸銀水溶液との反応ではどれも沈殿が生じている。 例えば、この臭素がもし未知の物質であったとしても、その上下にある塩素とヨウ素の性質から、未知の物質の性質を予測することができる。 単体が酸の水溶液にも強塩基の水溶液にも反応して、それぞれの塩をつくる元素を「両性元素」と言う。「酸」や「塩基」の両方と反応できるため、反応性が中間の性質を示す。周期表の非金属元素との境界付近にあるアルミニウム(Al)・亜鉛(Zn)・スズ( Sn)・鉛(Pb)などが両性元素になる。 例えばアルミニウムは、酸とも強塩基とも反応して塩を作る。酸化アルミニウムおよび水酸化アルミニウムは両性とよばれるように、酸と反応するとアルミニウムイオンを含む塩を生成し、強塩基と反応するとアルミン酸塩を生成する。 2AI + 6HCL ➡ 2AICI3 + 3H2 2AI + 2NaOH + 6H2O ➡ 2Na[Al(OH)4] 人工元素は、自然界には存在せず、人工的に作り出された元素の通称である。原子炉や加速器を利用し、陽子・中性子などを原子核に当てて人工的に作り出すことができる。通常、超ウラン元素や超重元素、人工放射性同位体などを指すが、天然にごく微量に存在する元素や、崩壊が速いために発見されにくかった元素も含まれている。 加速器や原子炉を使った核反応または核分裂により、人工的に作り出された元素には、テクネチウム(原子番号 43),プロメチウム(61),アスタチン(85),フランシウム(87),および原子番号が 93以上の超ウラン元素であるネプツニウム(93),プルトニウム(94),アメリシウム(95),キュリウム(96),バークリウム(97),カリホルニウム(98),アインスタイニウム(99),フェルミウム(100),メンデレビウム(101),ノーベリウム(102),ローレンシウム(103),ラザホージウム(104),ドブニウム(105),シーボーギウム(106),ボーリウム(107),ハッシウム(108),マイトネリウム(109),ダームスタチウム(110),レントゲニウム(111),コペルニシウム(112),ニホニウム(113),フレロビウム(114),モスコビウム(115),リバモリウム(116),テネシン(117),オガネソン(118)などがたり、いずれも放射性元素である。さらに大きな原子番号のものも作られようとしている。 目次へ |
||||||||||||||||||